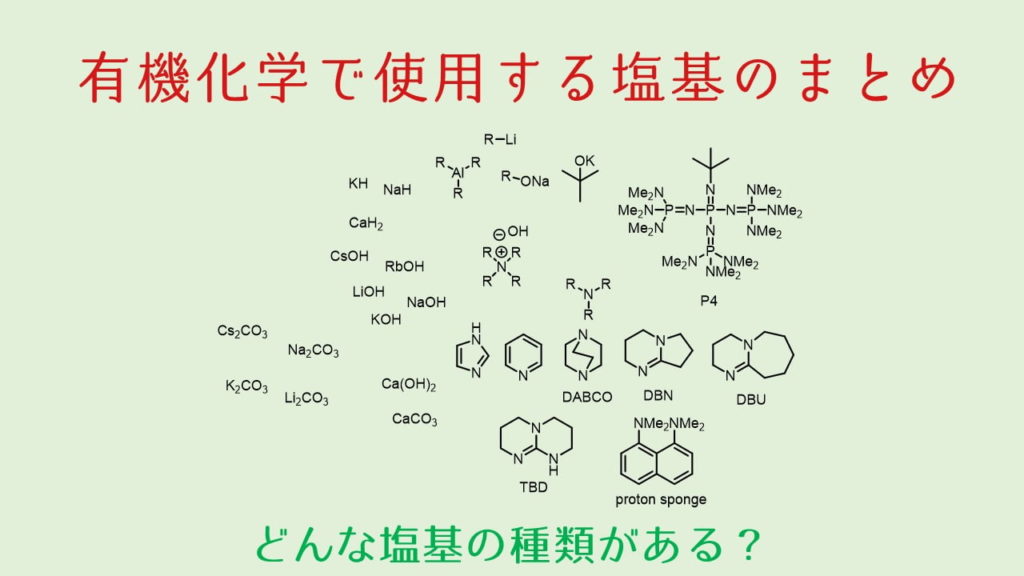
化学反応は酸・塩基が反応開始に非常に大きな役割を担っています。
極性反応、ラジカル反応、ペリ環状反応などの反応分類のうち、極性反応は酸・塩基が重要!
有機合成では、反応性の高い化学種を作ったり、酸をトラップするために塩基を使います。
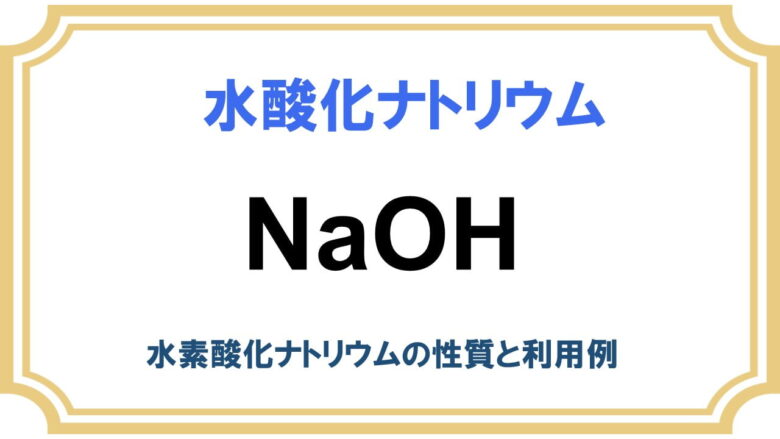
水酸化ナトリウム (NaOH)や炭酸カリウム (K2CO3)などはその代表例です。
有機化学現場では教科書などではあまり聞き馴染みはないけど有用な塩基がたくさんあります。この記事ではよく使われる塩基を紹介します。
 こめやん
こめやん
塩基とは?
塩基とは何か?を説明するのは結構大変です。なぜなら定義が複数あるからです。
しかし、有機合成では塩基と言ったら基本は「プロトンを奪う化学種」を指します。
なぜ、塩基が化学反応を進行させるのに重要なのでしょうか?
それは、中性の分子(非イオン性分子)よりもイオンの方が反応性が高いからです。
塩基はプロトンを奪うことによってアニオン(マイナスイオン)を発生させます。生じたアニオンは元の中性の分子よりも反応性が高くなっています。だから塩基を加えるのですね。
塩基の強さは塩基解離定数pKbで表され、特にpKbが0以下のものを強塩基と呼びます。
強塩基はすでにイオン性であることが多いです。水酸化ナトリウムもその例の1つです。
塩基の強さとは?
塩基の強さは構造式を見れば直感的に知ることができます。
強塩基の特徴は
- アニオン性
- 嵩高いアルキル鎖を持つ
- 電気陰性度の低い原子がイオンになっている
などの特徴があります。
嵩高さは塩基を安定に存在させるために重要であり、また求核性を下げるために重要です。嵩高い塩基は求核性が低いため、塩基自体が置換したりする副反応は起こりにくいです。小さいプロトンのみを攻撃します。
孤立電子対を持つ中性のアミンよりもアニオンを持つアミドイオンの方が塩基性が高いです。
また、酸素や窒素といった電気陰性度の高い元素にアニオンがあるよりも炭素がアニオンになっているものの方が塩基性が高いです。tert-ブチルリチウムは最も強力な塩基の1つです。
塩基は存在する環境によっても強さが変化します。有名な話がプロトン性溶媒と非プロトン性溶媒中での塩基の強さの違いです。
塩基はアニオンが多いと言いましたが、アルコールのようなプロトンを持つ溶媒を使ってしまうとアルコールのプロトンを奪ってしまう反応が起こるのはもちろんのこと、アルコールの水素はプラスに分極しているので、マイナスの塩基と水素結合して安定化(溶媒和)するので塩基性が低下してしまいます。
分極したプロトンを持たないDMSOやTHFなどは非プロトン性溶媒と呼ばれており、塩基を溶媒和しないので、アニオンの反応性が低下しません。
強塩基を使うときは溶媒は大抵この非プロトン性溶媒を使います。
有機合成で使われる塩基の種類
無機塩基
無機塩基にはアルカリ金属・アルカリ土類の水酸化物や水素化物,炭酸塩などがあります。
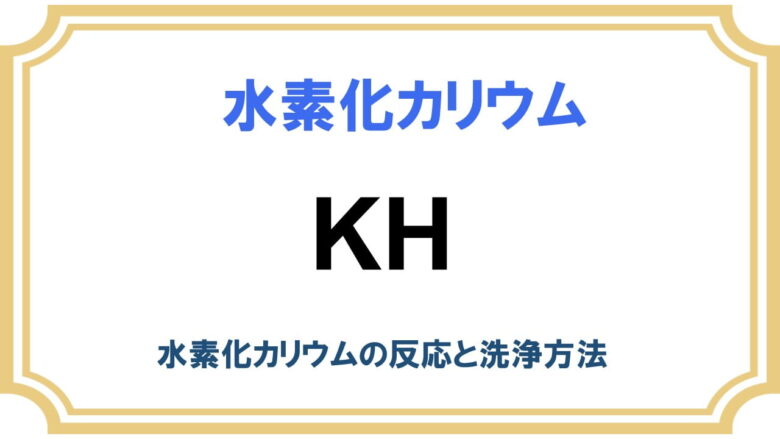
- アルカリ金属水素化物(NaH, KH)
- アルカリ土類金属水素化物(CaH2)
- アルカリ金属水酸化物(塩基性の強さは(CsOH>RbOH>LiOH>NaOH>KOH)
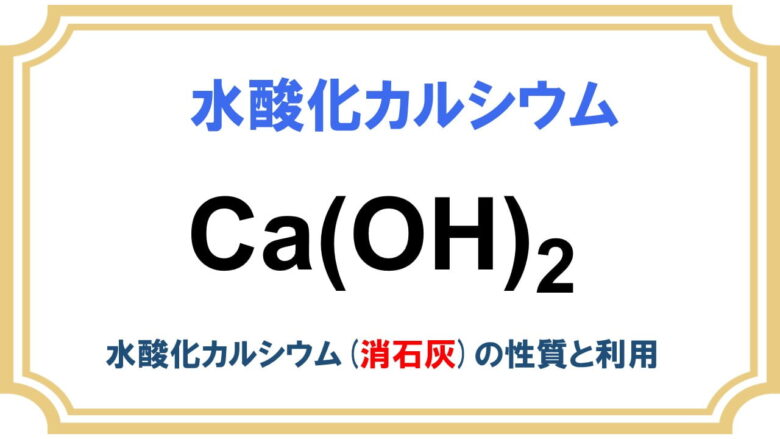
- アルカリ土類金属水酸化物(Ca(OH)2)
- アルカリ金属炭酸塩(Li2CO3, Na2CO3, K2CO3, Cs2CO3)
- アルカリ土類金属炭酸塩(CaCO3)
- フッ化セシウム(CsF)
アルカリ金属水素化物
非常に強い塩基としてアルコール、アミン、アミド、ジケトンなどのプロトンを引き抜き、水素を発生させます。

アルカリ土類水素化物
アルカリ土類金属の水素化物水酸化物、炭酸塩はアルカリ金属のそれと比べると利用例は少ないです。
アルカリ土類金属系の塩基の中では水素化カルシウムが重要です。脱水溶媒を作るのによく利用されます。

アルカリ金属水酸化物
金属水酸化物も強塩基ですが、水酸化物イオンが高い求核性を持つために、求核置換反応など、求電子剤共存下での塩基として利用すると反応してしまう恐れがあるので、利用例は限られます。加水分解などではよく利用されます。安価で取扱いやすいので多くの反応で利用されます。
アルカリ土類金属水酸化物
アルカリ土類金属水酸化物で重要なものは水酸化カルシウム Ca(OH)2 です。水酸化カルシウムは有機合成化学ではあまり利用価値はありませんが、工業的にさまざまな場所で利用されている身近な塩基です。
アルカリ金属炭酸塩
炭酸ナトリウムや炭酸カリウムといった炭酸塩は無機塩基の中では弱い塩基であり、扱いやすいために様々な用途で利用されています。有機合成でも炭酸カリウムや炭酸セシウムは塩基に弱い化合物のアルキル化、加水分解分解など広範に利用されています。単純な構造にもかかわらず炭酸リチウムは双極性障害の治療薬として利用されています。
フッ化セシウム
フッ化セシウムは他の無機塩基とは分類が異なりますので単独で消化します。フッ化セシウムはパラジウム触媒を使ったクロスカップリング反応などでよく目にします。塩基としての利用もありますが、吸湿性が小さめなフッ化物イオン源として利用されています。
有機塩基とは
有機塩基は炭素鎖を含む有機化合物からなる塩基です。無機塩基との違いはアルキル基を持つため有機溶媒に溶けやすいという特徴があります。
- 4級アンモニウム塩(水酸化テトラメチルアンモニウム)
- アルコキシド(ナトリウムエトキシド,カリウムt-ブトキシド(t-BuOK))
- 金属アミド(リチウムジイソプロピルアミド(LDA)、カリウムヘキサメチルジシラジド(KHMDS)、リチウム2,2,6,6,-テトラメチルピペリジド(LiTMP))立体障害の大きさ順
- 金属アルキル(アルキルリチウム,アルキルアルミニウム)
- ピリジン系(ピリジン、DMAP)
- 非ピリジン系複素環アミン(DBU, DBN,イミダゾール)
- リン系[フォスファゼン塩基](BEMP,グアニジノホスファゼン,P2塩基,P5塩基,)
アルコキシドは極性有機溶媒には溶けやすいです。アルコキシドは、t-BuOK以外では求核性が高く求電子剤と反応してしまうことが多いです。
金属アミドは求核性が低く,塩基性が高いです。また、有機溶媒にも溶けやすいです。
ピリジン系塩基は求核性を有しますが,非ピリジン系の複素環アミン塩基は求核性が低く,塩基性が高いです。
より求核性が低く強い塩基性を有するものはフォスファゼン塩基と呼ばれるリン系の塩基である.P5塩基は最も強い有機塩基として知られています。