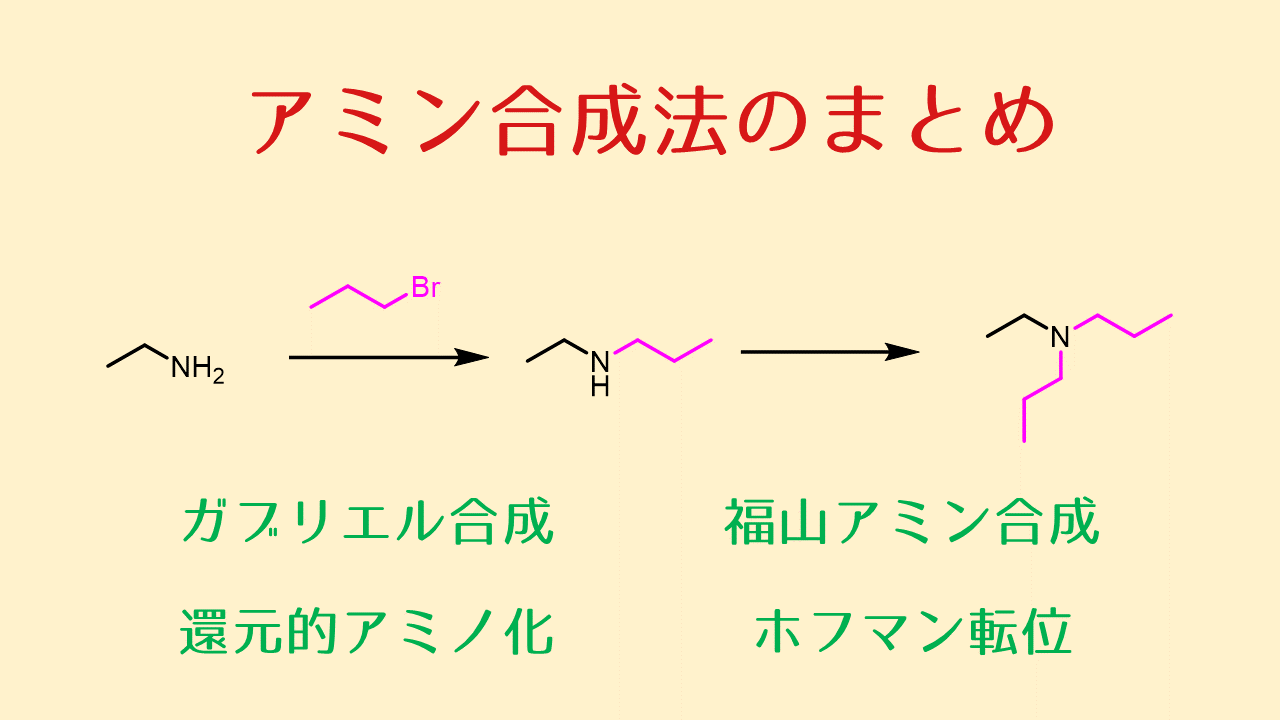
福山アミン合成はノシル基(2-nitrobenzenesulfonyl group)を用いてスルホンアミド化したアミンをアルキル化することにより第1~2級アミンを合成する方法です。
福山アミン合成とは?
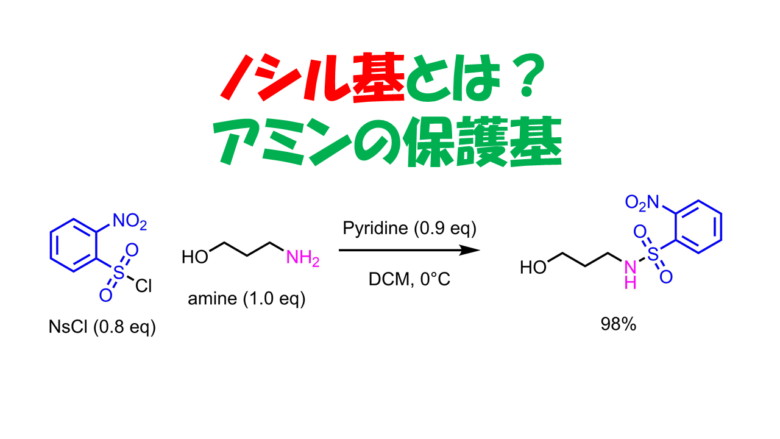
ノシル基はアミンの保護基としても使われるニトロスルホニル基です。
2-ニトロスルホンアミドはニトロベンゼンスルホン酸による電子吸引効果によってアミンプロトンの酸性度が上昇し、炭酸カリウムなどの塩基より引き抜かれて生じたアニオンがハロゲン化アルキルに攻撃するためアルキル化が可能です。ノシル保護された状態ではこれ以上のアルキル化は起こりません。
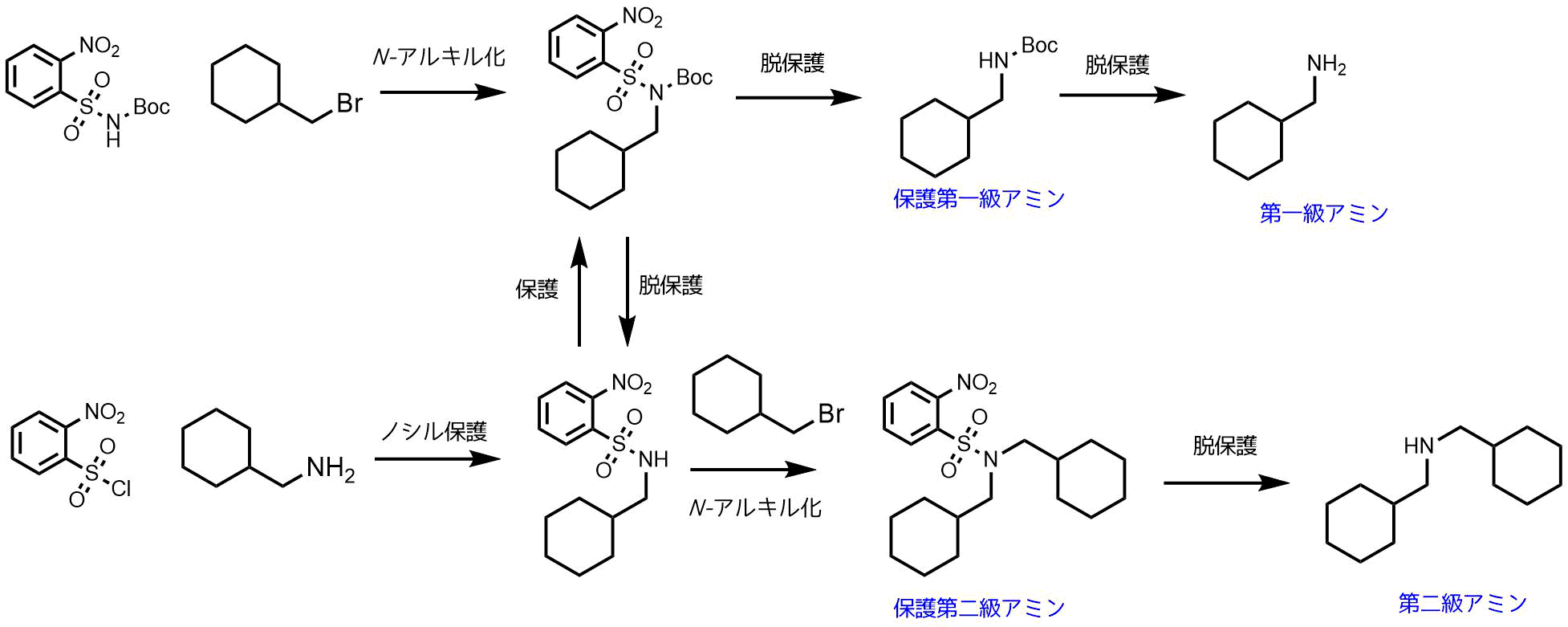
ノシル基はチオフェノールによって容易に切断され、第二級アミンを得られます。
ノシル基の保護・脱保護条件は穏和なため保護基としても有能です
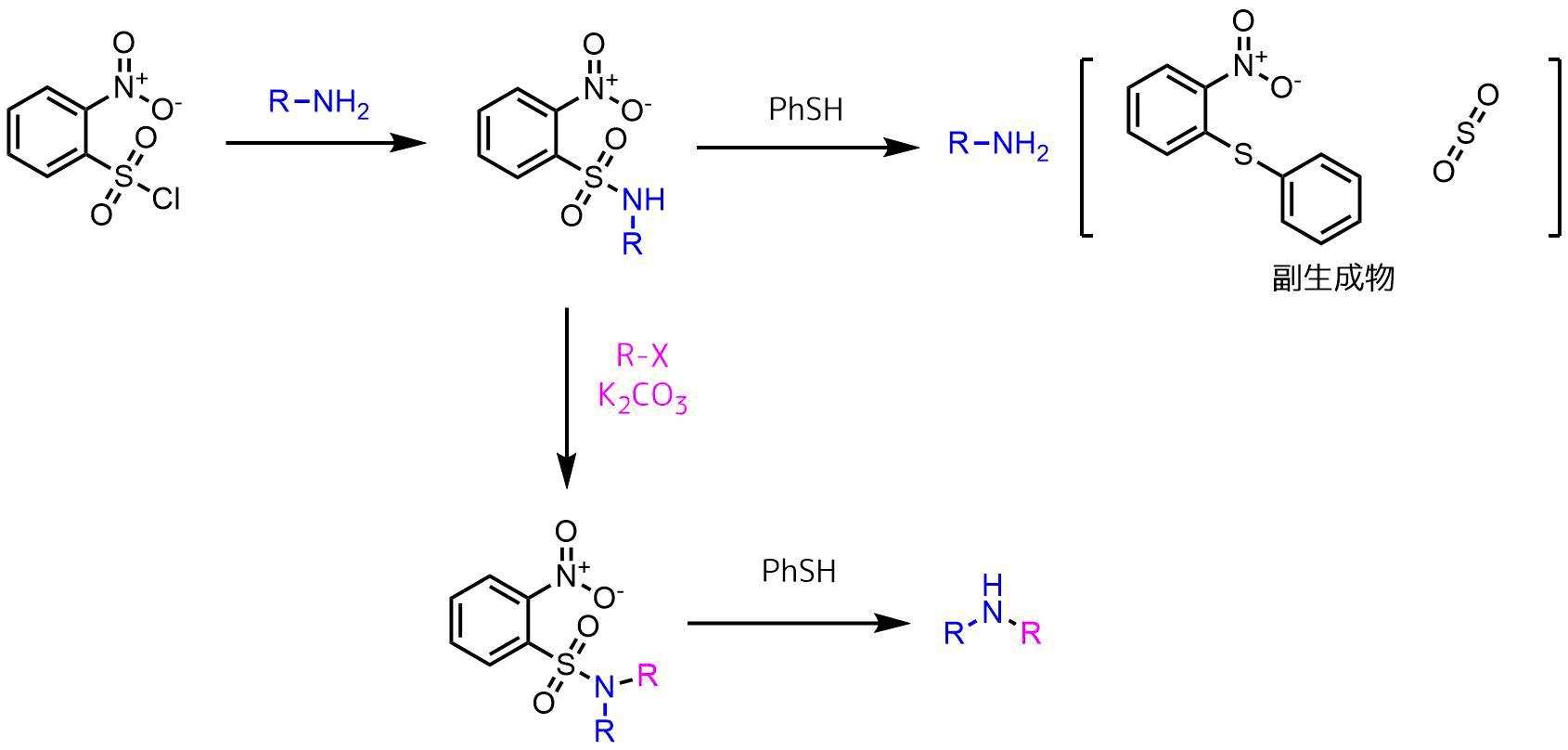
福山アミン合成の戦略
第一級アミンを合成したいときは、第一級スルホンアミドをアルキル化すると過剰アルキル化が進行する可能性があるため、保護されたスルホンアミドを利用する方法が便利です。
あらかじめスルホンアミドにBoc基やAlloc基、Cbz基を導入しておくことによってこれをハロゲン化アルキルでアルキル化すればこれ以上はアルキル化は進行せず、さらにノシル基を脱保護すれば対応する保護アミン体が得られます。このような保護アミンを得る合成方法は少ないです。

福山アミン合成の戦略1
Boc基保護のスルホンアミドを脱保護すればBoc保護された第一級アミンを合成することができます。
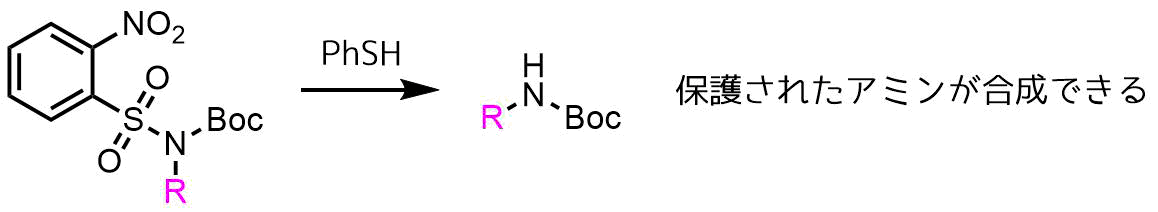
ノシル基で保護アミン体
ノシル法はアミン導入から保護までこなせるのでアミン合成のなかでは優秀な方法です。個人的にはアミンを導入する際は福山アミン合成法かアジドを用いることが多いです。保護基としてもガブリエルアミン合成法で利用されるフタルイミドよりも扱いやすいです。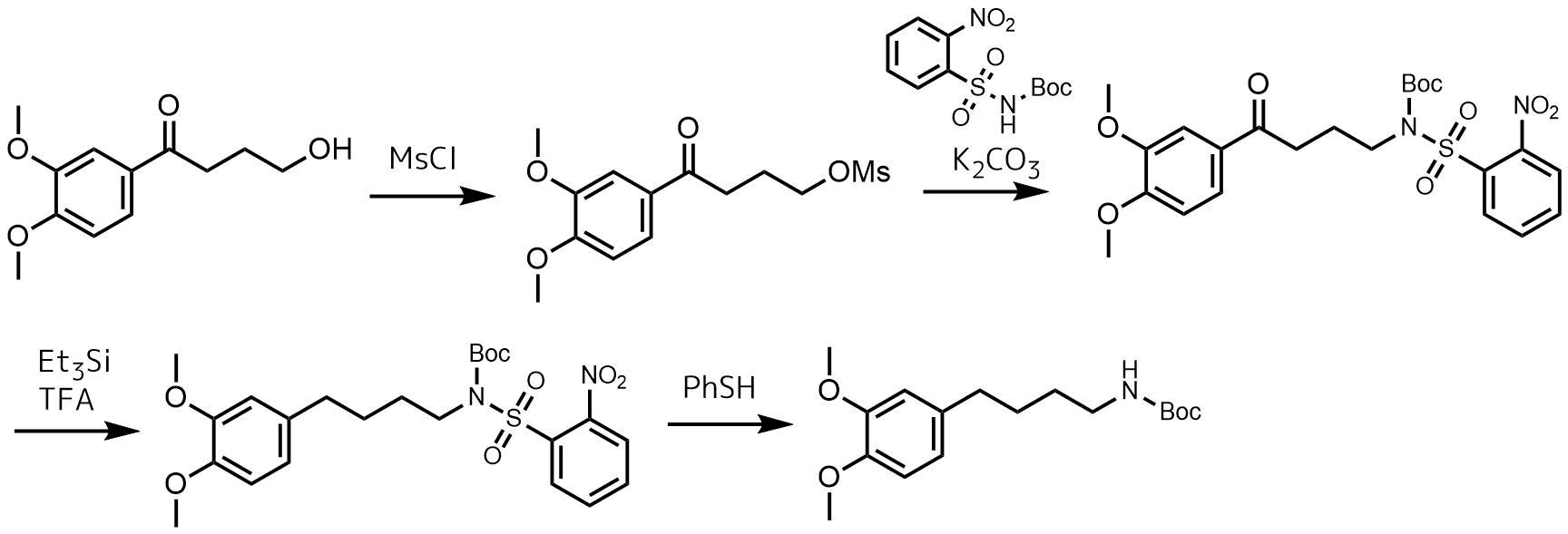
ノシル基で合成経路例福山アミン合成法では2-ニトロベンゼンスルホンアミドのアルキル化、アミンをスルホニルクロリドでスルホンアミド化して変換するなどの経路が考えられます。何を原料とするか?は合成経路によって変化しますね。
ノシル保護を使った合成経路例
ノシル基脱保護の反応機構
ノシル基の脱保護はチオフェノールを用いることが多いです。塩基性条件下、チオフェノキシドがスルホンアミドのイプソ位を攻撃してマイゼンハイマー錯体を形成後、二酸化硫黄の発生を伴ってアミンが生成します。
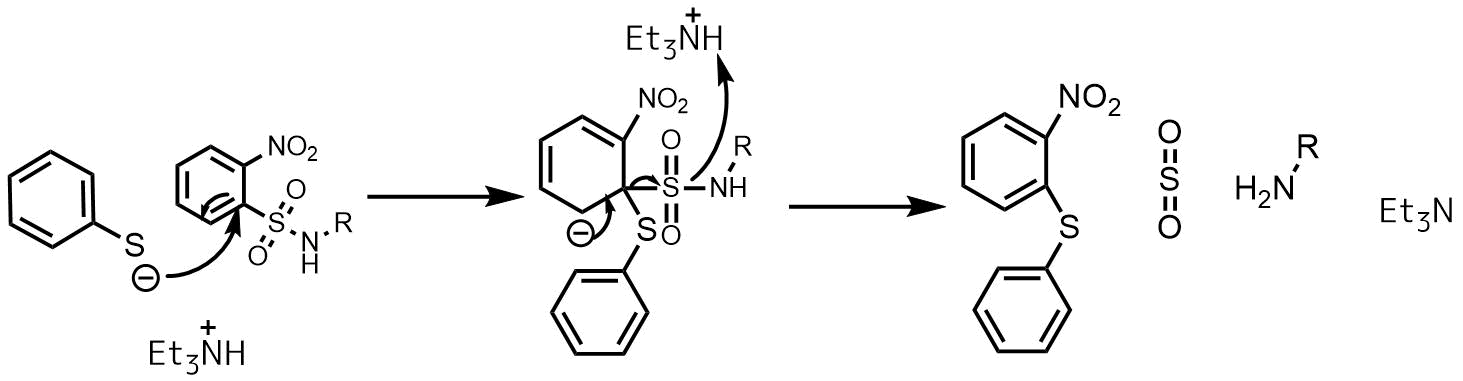
ノシル基脱保護の反応機構
ノシルアミドの種類
ノシルアミドは2-ニトロベンゼンスルホンアミドやそれをBoc基等で保護したものが主流ですが、他にもあります。
p-Nsは4位にニトロ基がついたスルホンアミドです。NMRはp-置換体のほうが見やすく、芳香族領域のNMRピークを汚さないですむメリットがあります。また、二つのニトロ基が入ったDNsはNs基よりも外れやすく、Ns基存在下DNs基のみをチオグリコール酸を使って脱保護可能です。
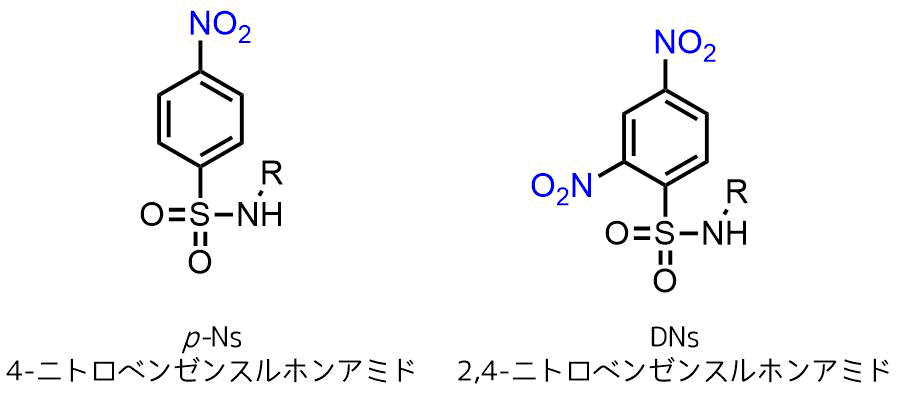
他のスルホンアミド誘導体
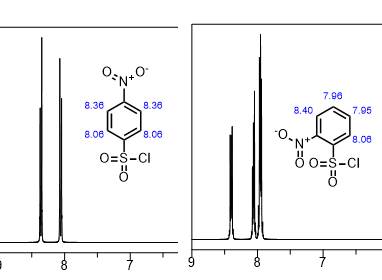
ノシルのNMR
pNs基のデメリットは少々高価である点と脱保護時にニトロとチオフェノールが置換する副反応が起こる可能性がある点です。
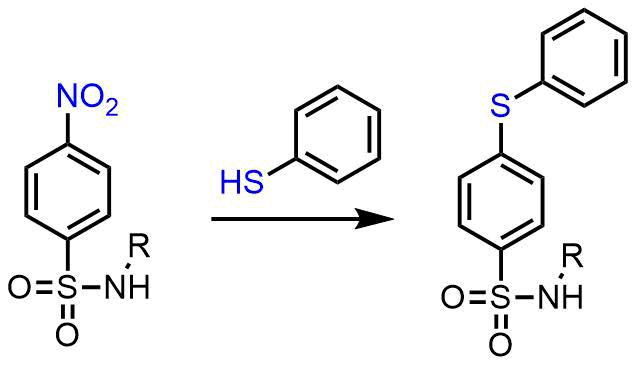
4-Nsの副反応 Wuts, Peter GM, and Jill M. Northuis. “A cautionary note on the use of p-nitrobenzenesulfonamides as protecting groups.” Tetrahedron letters 39.23 (1998): 3889-3890.
臭くないチオフェノール
チオフェノールは強烈な臭気があるため、大スケールでは使いにくい試薬です。それを避けるためにカルボン酸で置換されたチオールを用いることもできます。4-メルカプト安息香酸は臭くないチオフェノールであり、ノシル基の脱保護にも利用できることが報告されています。
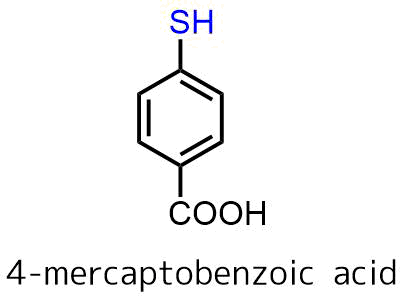
Matoba, Manabu, Tetsuya Kajimoto, and Manabu Node. “Application of Odorless Thiols for the Cleavage of 2‐and 4‐Nitrobenzenesulfonamides.” Synthetic Communications 38.8 (2008): 1194-1200.