フタロイル基(Phth基)とは
フタロイル基(Phth基)はイミド系のアミンの保護基です。
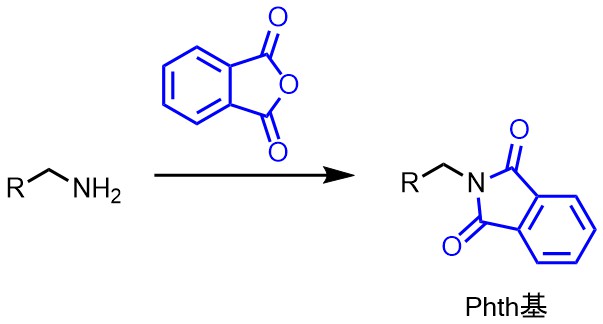
フタロイル基は2つのカルボニル基でつまむようにして保護するため、第一級アミン選択的で第一級アミンの反応性を完全に抑えたいという場合に有用です。
また、フタロイル基は比較的安定で、酸や塩基性条件にもある程度耐え、酸化条件にも強いです。MeLiやグリニャール試薬等の求核剤やLAHとは反応してしまいます。
脱保護には過激な酸・塩基加水分解条件やヒドラジンを用いて行います。フタルイミドカリウムなどを求核剤として光延条件下アルコールと反応させることによってアルコールを第一級アミンに変換できます(ガブリエルアミン合成)
特徴・利点
フタロイル基の利点や特徴は
- アミノ基の水素を無くして完全に保護可能
- 第一級アミン選択的に保護可能
- 試薬が安価
フタロイル基は窒素上に水素を残さないため、水素引き抜きなどによって起こる副反応を避けられます。
第二級アミン存在下、第一級アミン選択的に保護可能で、原料の無水フタル酸も安価で低コストです
欠点としては
- 脱保護条件が過激
- 脱保護後の精製が面倒
安定な保護基であるため脱保護条件は過激です。
- 酸・塩基加水分解 → 高濃度、高温条件
- ヒドラジン → ヒドラジン水和物で加熱
ヒドラジンによる脱保護は信頼性が高いですが、エステル等が分子内にあると副反応を起こす可能性があります。脱保護後に生じるフタル酸ヒドラジドはうまく結晶化を利用することで除去することが可能です。
反応機構
反応機構ー保護
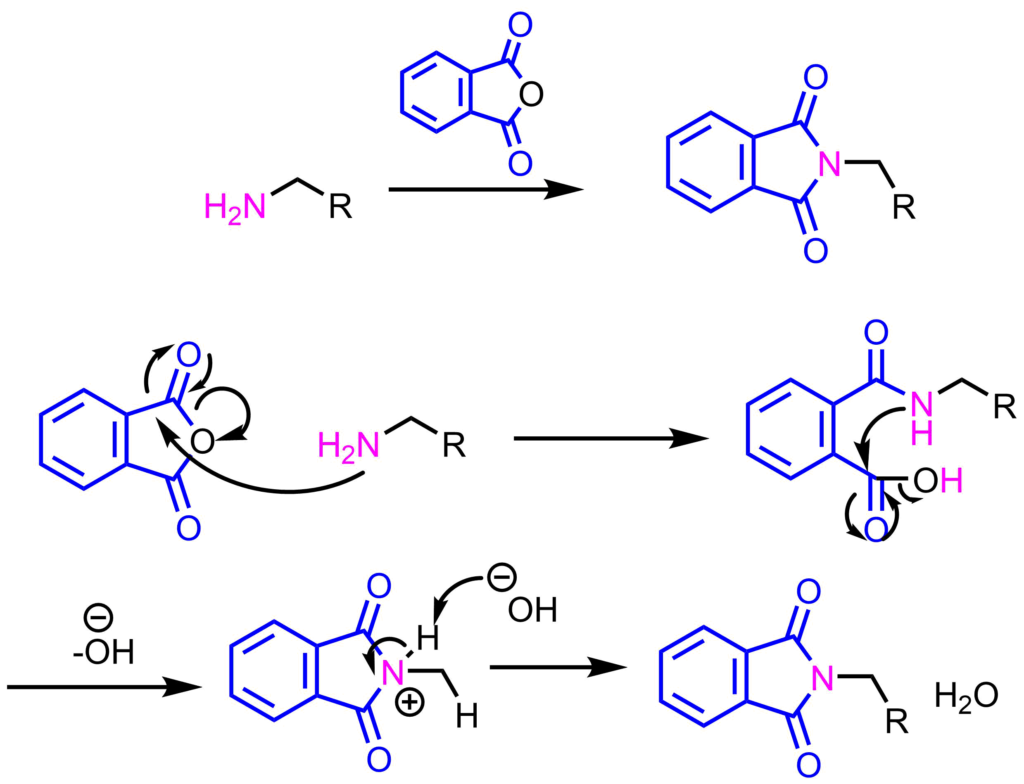
アミンが無水フタル酸のカルボニル炭素に攻撃して進行します。
反応機構ー脱保護
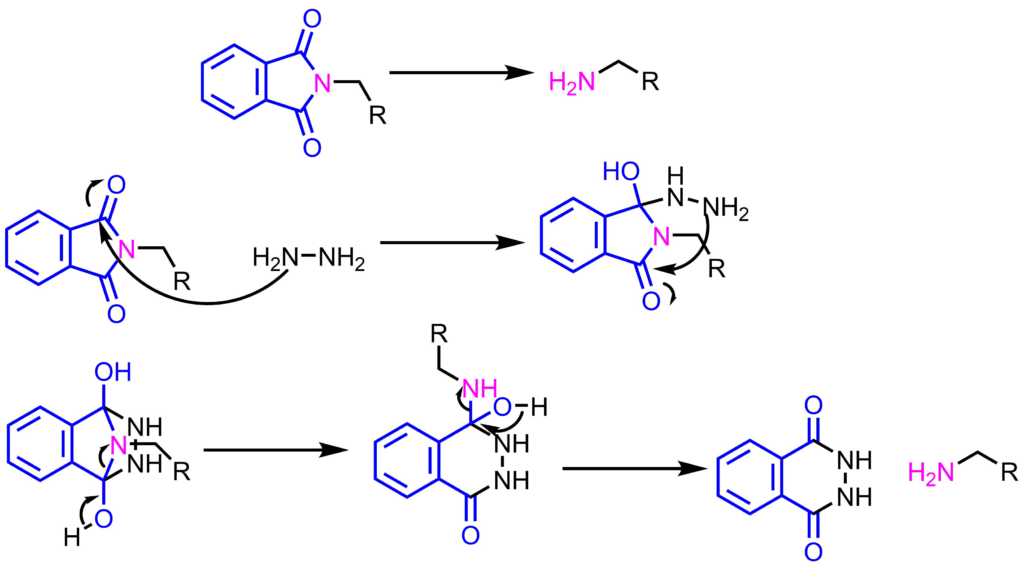
フタルイミドの酸、塩基による加水分解はアミドの加水分解と同様の反応機構です。ヒドラジンを用いて脱保護するとフタル酸ヒドラジドが生成し、アミンの脱保護体が得られます。
反応条件-保護
フタロイル保護は無水フタル酸とアミンを脱水縮合して得ます。
保護条件例1
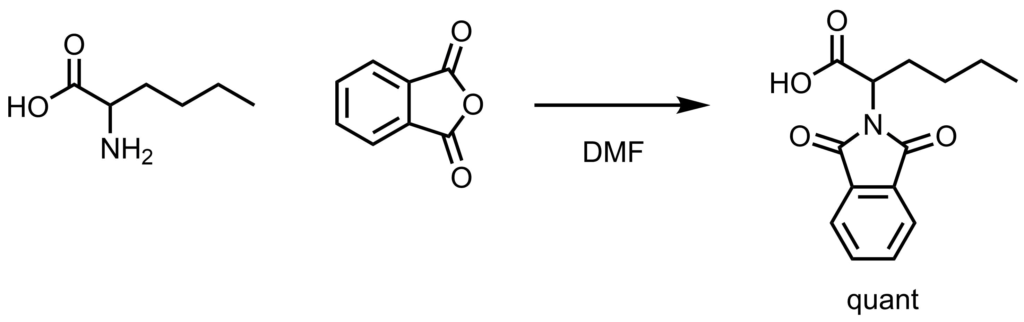 デシケーターで乾燥させた25mLフラスコに、アミン (1 eq, 7.6 mmol)、無水フタル酸(1.5 eq, 11.4 mmol)、DMF(15 mL)を加えて溶解し、155℃で12時間撹拌した。反応物を室温に冷却し、50mLの1N HClに注ぎ入れ、20分間0℃で冷却した(沈殿が生じない場合は、単離するためにジエチルエーテルで抽出した)。吸引ろ過により目的物を得た(quant)。Quinn, R. K., et al. J. Am. Chem. Soc. 2016, 138, 702. より引用。フタロイル保護は脱水縮合のため高温条件で実施されることが多いです。60℃くらいでも反応は進行しますが、収率が低くなります。
デシケーターで乾燥させた25mLフラスコに、アミン (1 eq, 7.6 mmol)、無水フタル酸(1.5 eq, 11.4 mmol)、DMF(15 mL)を加えて溶解し、155℃で12時間撹拌した。反応物を室温に冷却し、50mLの1N HClに注ぎ入れ、20分間0℃で冷却した(沈殿が生じない場合は、単離するためにジエチルエーテルで抽出した)。吸引ろ過により目的物を得た(quant)。Quinn, R. K., et al. J. Am. Chem. Soc. 2016, 138, 702. より引用。フタロイル保護は脱水縮合のため高温条件で実施されることが多いです。60℃くらいでも反応は進行しますが、収率が低くなります。
保護条件例2
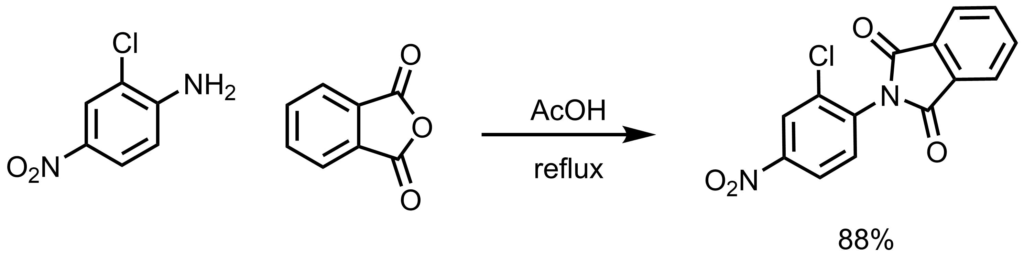
フラスコに、200 mg (1.622 mmol, 1.2 eq)の2-クロロ-4-ニトロアニリンおよび280 mg(1.350 mmol,1.0 eq)の無水フタル酸を加え、5mLの酢酸に溶解した。混合物を24時間還流した。溶液を冷却した後、沈殿個体を濾過し、冷メタノールで洗浄し、目的物を得た(88%). Cho, H. P., et al. ACS Chem. Biol. 2014, 9, 2346. より引用。酸触媒としてトシル酸(0.05eq等)を用いたりする例もありますが、酢酸を溶媒として利用する例もあります。また、トルエンを溶媒として(ディーン・スターク装置を使ってもよい)還流する方法も使われます。塩基触媒としてトリエチルアミン(1-2eq)を用いる条件もあります。溶解性の悪いものは酢酸やDMFを用いたほうが良いかもしれません。
脱保護反応例
フタロイル基の脱保護法には1.酸、2.塩基、3.ヒドラジン水和物の方法があります。塩酸を用いる場合は過剰量の濃塩酸(4eq)を100-200℃で3-6時間加熱する過激な条件であるため適応性は低いです。塩基加水分解は10%KOH水溶液などを用いて実施され、フタルイミドからフタルイミド酸(片側だけ外れる)が生成するが、これ以降は反応が進行しにくく加熱還流条件などが必要です。フタルイミド酸は酸に不安定であるため、塩基に引き続き、酸での加水分解(濃塩酸ーrefulx)を行うことで一級アミン体を得ます。
反応例1(ペプチド合成)
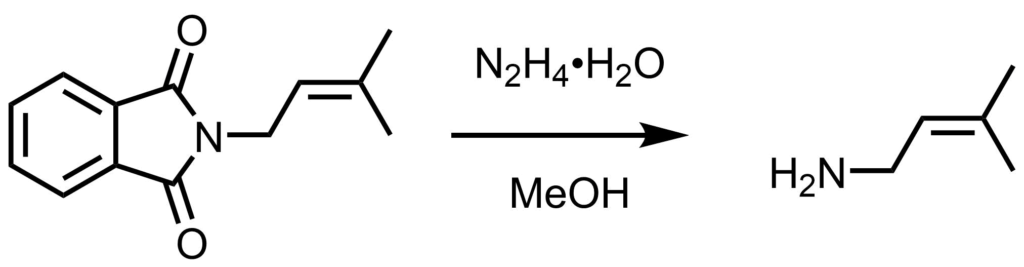 メタノール(5 mL)、保護アミン体(1.0 eq, 4.66 mmol)の撹拌溶液に、ヒドラジン一水和物(1.5eq, 7.00 mmol)を加え、30分間加熱還流した。得られた白色沈殿物を水(10mL)に溶解し、そして白色固体に濃縮した。粗製固体を水(13mL)に溶解し、濃塩酸(2mL)を滴下した。白色沈殿物を濾過し、そして水で洗浄した。ろ液を濃縮し、メタノール中で滴定した。 0.510 g (4.00 mmol, 90%)の淡黄色固体。 (R f = 0.16; 20%メタノール:DCM). Corder, A. L., et al. Biochemistry. 2013, 52, 6196. より引用。フタルイミドの脱保護はあまり収率が高くない印象があります。溶媒としてはエタノールやメタノールがよく使われます。分子内にエステルがある場合は1当量用いることで副反応を抑えることができます。
メタノール(5 mL)、保護アミン体(1.0 eq, 4.66 mmol)の撹拌溶液に、ヒドラジン一水和物(1.5eq, 7.00 mmol)を加え、30分間加熱還流した。得られた白色沈殿物を水(10mL)に溶解し、そして白色固体に濃縮した。粗製固体を水(13mL)に溶解し、濃塩酸(2mL)を滴下した。白色沈殿物を濾過し、そして水で洗浄した。ろ液を濃縮し、メタノール中で滴定した。 0.510 g (4.00 mmol, 90%)の淡黄色固体。 (R f = 0.16; 20%メタノール:DCM). Corder, A. L., et al. Biochemistry. 2013, 52, 6196. より引用。フタルイミドの脱保護はあまり収率が高くない印象があります。溶媒としてはエタノールやメタノールがよく使われます。分子内にエステルがある場合は1当量用いることで副反応を抑えることができます。
注意事項ーTips
- フタロイル基は脱保護条件が過激なものが多く、脱保護収率は他の保護基と比べて低め
- 脱保護に用いるヒドラジンは爆発性を有するので注意する
- ヒドラジン脱保護時にカルボン酸、酸アミド、スルホンアミド、ニトリルが存在していてもヒドラジンを過剰量加えても副反応が起こりにくいが、エステルは反応するので1当量、長時間反応で脱保護したほうが良い。
参考まとめ
Wuts, Peter G. M.. Greene’s Protective Groups in Organic Synthesis Fifth edition(p.1010). Wiley.
Jie Jack Li,Chris Limberakis,Derek A. Pflum, 研究室ですぐに使える 有機合成の定番レシピ, 丸善、p.225
[blogcard url=”https://www.jstage.jst.go.jp/article/yukigoseikyokaishi1943/29/5/29_5_496/_pdf/-char/en”]