Boc基とは?
Boc基はターシャリーブトキシカルボニル基(tert-butoxycarbonyl group)の略で、アミンの保護基として使われます。カルバメート系の保護基で塩基や求核剤、還元条件に安定で、酸性条件では不安定です。そのため、酸性で脱保護したい時のアミンの保護基として良く使われます。
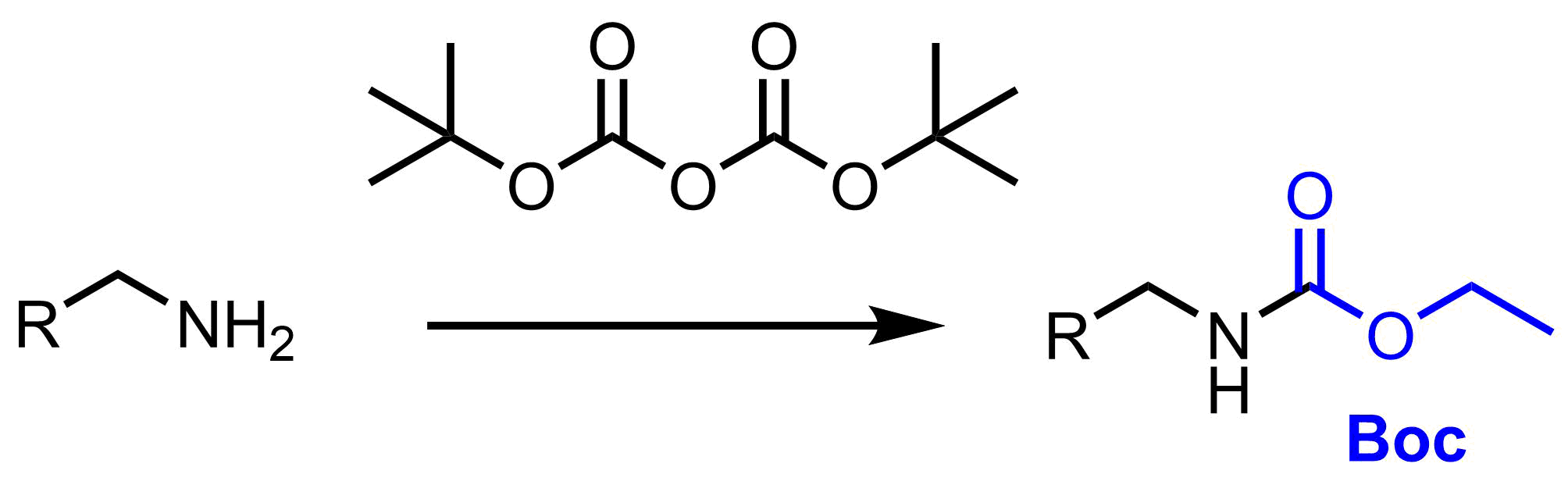
アミンのBoc化
特徴・利点
Boc基の利点や特徴は
- 脱保護時の副生成物の除去が簡単
- 酸以外の条件で安定
- 反応例が豊富
です。試薬もそこまで高価ではありません。酸による脱保護は大抵問題なく進行します。
反応機構
反応機構ー保護
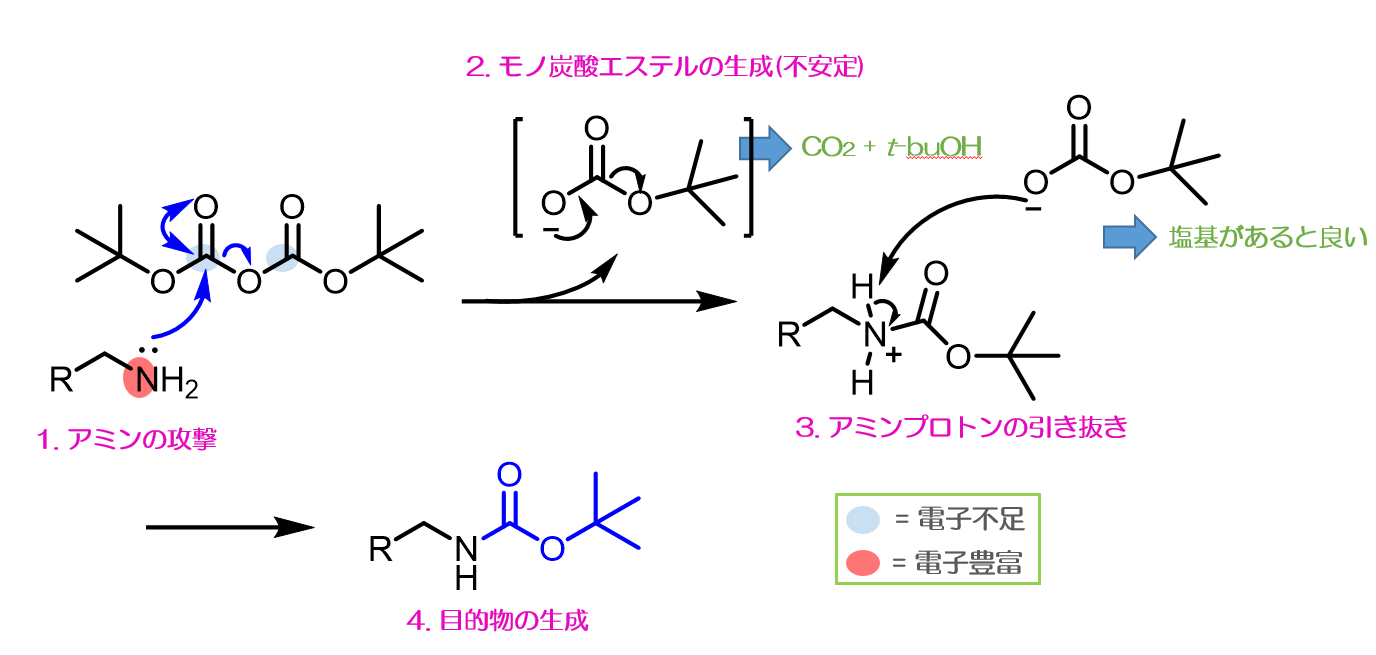
機構はシンプルなアミンと酸無水物との求核アシル置換反応です。塩基は入れなくても進行します。DMAPを入れると酸無水物と反応して活性中間体を作るため反応が早く進行します。モノ炭酸エステル紙面上では描くことができますが、実際は不安定で二酸化炭素とアルコールに分解しやすいです。
反応機構ー脱保護
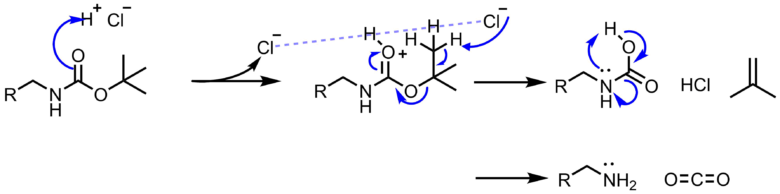
酸によってアミドの窒素がプロトン化されるとtertブチル基のプロトンの脱離と脱炭酸を伴い脱保護されます。生成したアミンは酸との塩として得られるため、塩酸で脱保護したときなどは塩酸塩の固体として得られることがよくあります。脱保護により生成する副生成物は全て気体であるため、脱保護後の精製が不要であることがわかります。tertブチル基は酸条件においてカルボカチオンを生成しやすいため、カルボカチオンが生成するような反応機構を描くことも可能です。
反応条件-保護
保護条件例1 (tertブチルアミン)
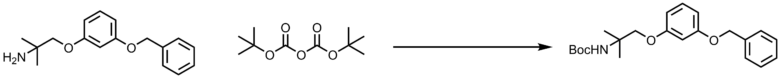
アミン(1eq, 3.68mmol)および(Boc)2O (1.5 eq, 5.52mmol)を無水ジクロロメタン(10 mL)に溶解し、室温で窒素雰囲気下18時間撹拌した。 減圧除去して得たクルードをカラムクロマトグラフィー(ジクロロメタン)により精製して目的物を100%の収率で得た。
保護条件2(環状第二級アミン)
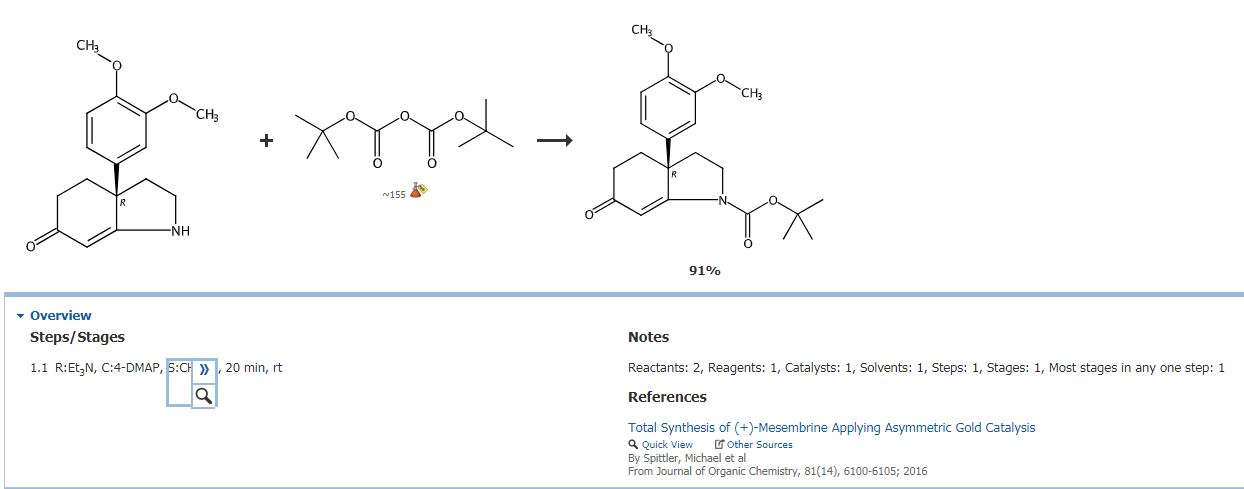
アミン (1eq, 0.494mmol)を脱水ジクロロメタン(6mL、0.1M)に溶解し、DMAP(0.14 eq, 0.069mmol)、トリエチルアミン(1.4eq, 0.68mmol)および (Boc)2O(1.38eq, 0.684mmol)を加えた。 20分撹拌後、混合物を水、ブラインで洗浄後、水層をジクロロメタンで分液した。有機層を合わせて、水:ブライン(1:3)で洗浄後、溶媒を除去、真空乾燥させた。 シリカゲルカラムクロマトグラフィーで精製して目的物(0.449mmol、91%)を得た。
保護例3(第一級アミン ショッテンバウマン条件)
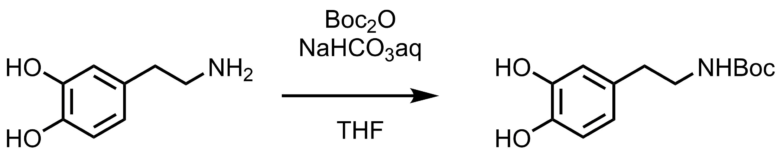
(Boc)2O(1.1 eq, 5.00mmol)を、THF(10 mL)と飽和NaHCO 3水溶液(6 mL)、アミン(1 eq, 4.53mmol)の溶液に添加した。反応混合物を室温で2時間撹拌した後、水層をEtOAc(3×10mL)で抽出した。 合わせた有機抽出液を食塩水で洗浄し、MgSO4で乾燥し、減圧下で濃縮し、目的物を白色固体として得た(1.15g、quant)。
保護例4 (不活性アミン)
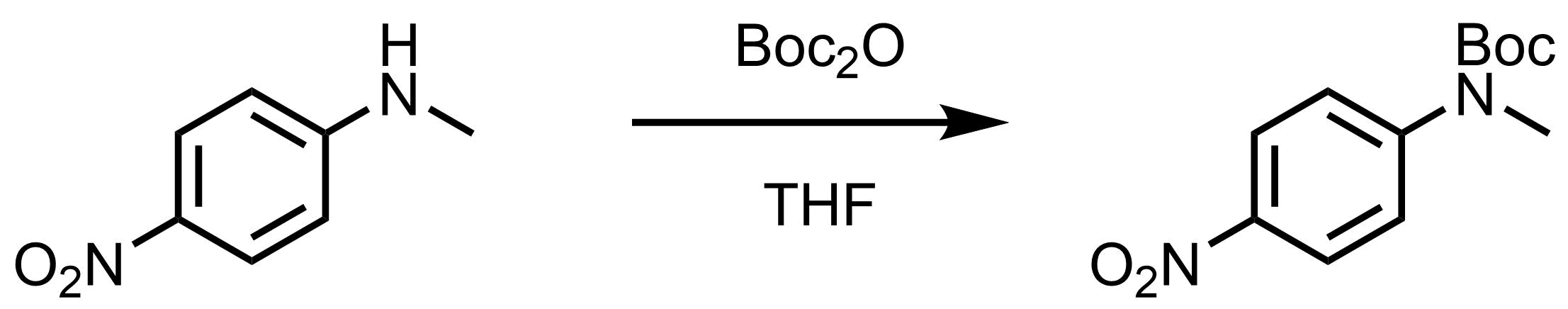
DMF (380mL)中のN-エチル-4-ニトロアニリン (1eq, 30mmol)の溶液に、水素化ナトリウム(1.5eq、45mmol、鉱油60%)を加えて水素の発生が止むまで混合物を撹拌した。 (Boc)2O(1.5 eq、45mmol)を加え、反応物を2時間撹拌した。 混合物を250mLのH2Oで希釈し、酢酸エチル(250mL)で抽出した。 有機層を水(200mL、3回)で洗浄し、濃縮、目的物(91.5%)で得た。
反応例1のようにアミン周辺が嵩高い場合は、(Boc)2Oを高濃度で反応させると進行しやすい。溶解するなら溶媒無しのニートで反応をかけても反応が進行する。DMAPを加えても良い。共役したアミンなど反応性が低下したものも同様にDMAPを加えると反応が加速する。反応例3のように水溶性の高いアミンの場合は炭酸水素ナトリウム水溶液中で反応させるショッテン・バウマン条件を使うことが多いです。アミノ酸のBoc保護の条件としてよく使われます。
脱保護
塩酸を加える方法もあるが、酸加水分解等の副反応を抑えるには、HCl-AcOEtやHCl-dioxaneなどの有機溶媒中にHClが溶けたものが有用です。
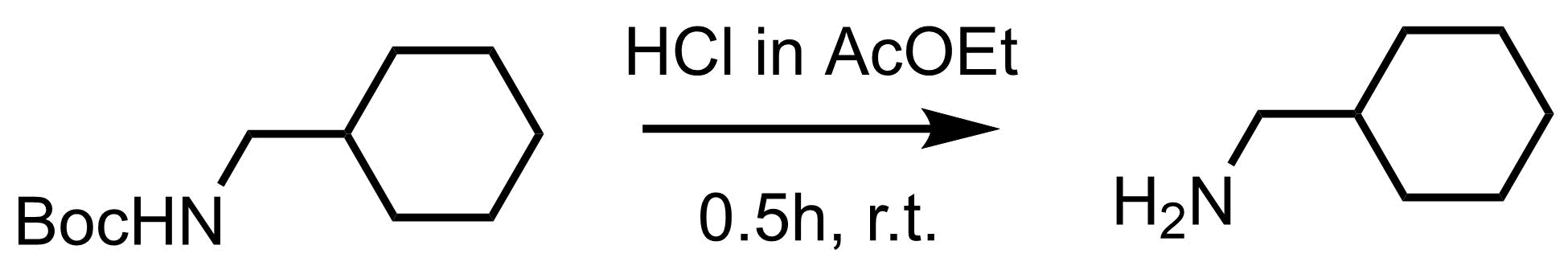
TFAを1-2eq加えて脱保護する方法も一般的です。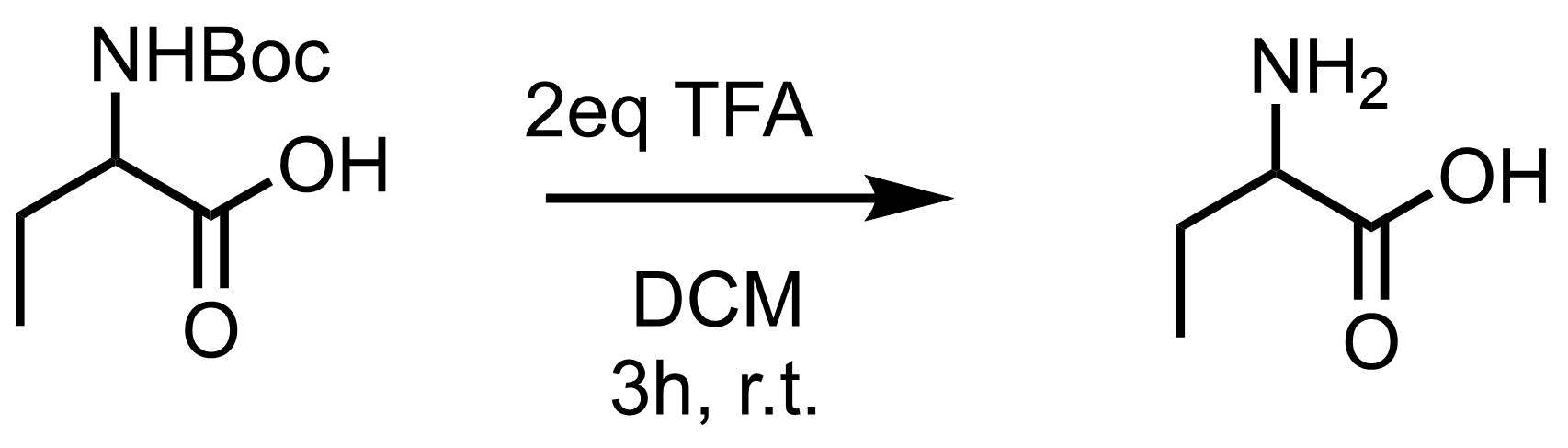
一般的な脱保護のやり方
アルゴン雰囲気下、溶媒中のアミンを0℃で冷却・撹拌しながら酸を滴下して加えます。
その後、室温に戻しながら1-3h程度撹拌します。原料の消失と副反応のモニタリングをTLCで行い、反応が終わったら、そのまま濃縮してカラムクロマトグラフィーを行います。
濃縮すると酸で壊れてしまう可能性がある場合は炭酸水素ナトリウム水溶液等を加えて中和、分液しても良いです。
極性の高いアミン類はシリカゲルにひっつきやすいので、アミン修飾シリカゲルやトリエチルアミン0.1-1%添加した展開溶媒を使うとテーリングしにくく、分離しやすいです。
TLCでいろんな条件を検討してみましょう。また、カラムに頼らずに塩酸塩など固化させて回収しても良いです。
注意事項
- 脱保護時に強酸を使うので酸に弱い官能基を含む場合は使用できない。
- ほかに求核性の高い部位が存在するとBoc基の転移が起こる可能性がある。
- 嵩高いアミンの保護は進行しくく、イソシアネートを経由してウレアを形成する可能性がある。
過剰な(Boc)2Oの除去方法
過剰に加えた(Boc)2Oは微妙な極性・沸点を持っているため除去が難しい場合があります。
この過剰な(Boc)2Oはトリフルオロエタノール(TFE)を用いることによってtert-ブタノールとCO2に分解できます。
操作方法としては、反応後の溶液に対して1 eqのTFEと0.1 eqのDMAPを加えて5分位撹拌した後分液をすることで除去できます。
 こめやん
こめやん
参考文献
反応例1) GILDAY, Lydia C.; WHITE, Nicholas G.; BEER, Paul D. Shielded alkyl-functionalised rotaxane host cavities for improved anion recognition. Supramolecular Chemistry, 2016, 28.1-2: 62-83.
反応例2) SPITTLER, Michael; LUTSENKO, Kiril; CZEKELIUS, Constantin. Total synthesis of (+)-mesembrine applying asymmetric gold catalysis. The Journal of organic chemistry, 2016, 81.14: 6100-6105.
反応例3) Khalil, Iman M., David Barker, and Brent R. Copp. “Bioinspired syntheses of the pyridoacridine marine alkaloids demethyldeoxyamphimedine, deoxyamphimedine, and amphimedine.” The Journal of organic chemistry 81.1 (2015): 282-289.
反応例4) Liu, Gang et al, U.S. Pat. Appl. Publ., 20060089398, 2006
参考書籍) 佐藤信裕. “最新有機合成法 設計と戦略, GS ツヴァイフェル, MH ナンツ著, 檜山為次郎訳, 化学同人 p.62-63
参考書籍2)
[blogcard url=”https://www.organic-chemistry.org/protectivegroups/amino/boc-amino.htm”]
[blogcard url=”https://en.wikipedia.org/wiki/Tert-Butyloxycarbonyl_protecting_group”]
[blogcard url=”http://commonorganicchemistry.com/Rxn_Pages/Boc_Protection/Boc_Protection_Index.htm”]
[blogcard url=”https://blogs.yahoo.co.jp/deebsky2009/5248259.html”]
[blogcard url=”http://fchem.4rm.jp/log/yuki/258.html”]
[blogcard url=”https://www.jstage.jst.go.jp/article/yukigoseikyokaishi1943/36/9/36_9_740/_pdf”]
[blogcard url=”http://www.ekouhou.net/%EF%BC%AE%E2%88%92%EF%BC%A2%EF%BC%AF%EF%BC%A3%E5%8C%96%E5%90%88%E7%89%A9%E3%81%AE%E8%84%B1%E4%BF%9D%E8%AD%B7/disp-A,2009-143918.html”]