ルミノールといえば、血痕を見つける試薬として有名です。このルミノールはどうやったら作れるか?
できるだけ簡単で安価な方法を考えてみました。
ルミノール液の作り方・実験方法
ルミノールはアミノフタル酸ヒドラジドという物質です。
ルミノールを作る上でのポイントとなる試薬はヒドラジン水和物です。
ヒドラジンは聞き慣れない物質かもしれませんが、N2H4という単純な分子です。
水素をたくさんもっているので還元性を持ち、酸素と爆発的に反応するためロケット燃料にも使われています。
濃度の高いヒドラジンは爆発性があるために注意が必要です。濃縮などもしないように気をつけましょう!
ルミノールの合成経路!有機化学実験の練習実験にも最適?!
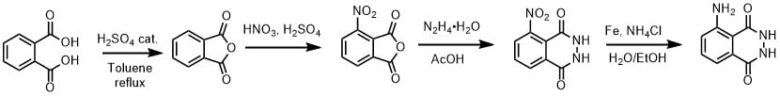
合成は無水フタル酸からスタートしてもよいですが、フタル酸から酸無水物を作るという方法も教育的にも良いかもしれません。
ルミノールはフタル酸から4ステップで合成できます。
ステップ1:分子内脱水縮合で無水フタル酸の合成
フタル酸はベンゼン環に2つのカルボキシル基が存在する芳香族カルボン酸で、これを分子内脱水縮合させて酸無水物を作ります。
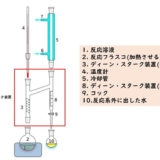
この反応は脱水反応なので、反応容器中から水を取り除くこと、脱水させる必要があります。この目的に利用するのがディーン・スターク装置です。ディーン・スターク装置を使うことによって、反応溶液中から水がなくなることで反応が無水物生成に偏っていきます。
こうしてできた無水フタル酸は1M NaOHなどの塩基性水溶液ですばやく分液すれば抽出操作だけで無水フタル酸が入手できると思います。
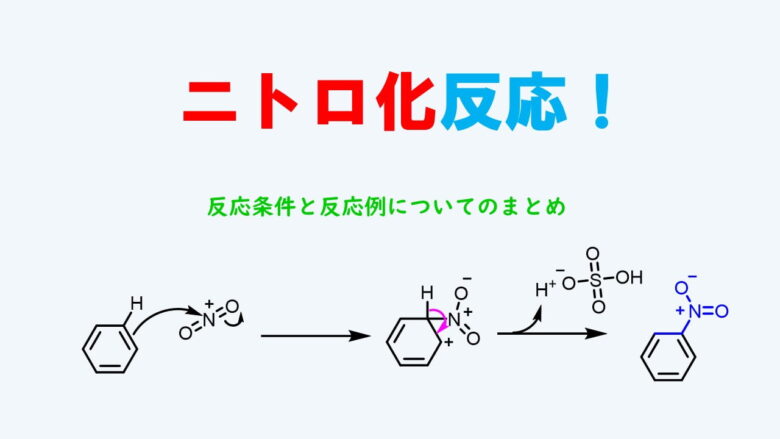
ステップ2:ニトロ化
その後、混酸(硝酸と硫酸)を使ったニトロ化を行います。硝酸1に対して硫酸を10~20倍体積分加えるのが一般的でしょうか?
温度を上げないように氷浴につけて(-20~0℃)、短い時間(1時間程度)でニトロ化します。ニトロ化の後処理は氷が入ったビーカーに反応液を注いで、出てきた結晶をろ過すればニトロ体が得られます。氷は入れすぎないように反応液の体積の2~3倍くらい。
結晶が出てこない場合は分液しましょう。
ステップ3:ヒドラジドの合成
酢酸を溶媒として、ヒドラジンを加えて70℃くらいまで温めて酸無水物とヒドラジンを反応させます。アミド化と同じですね。
フタル酸ヒドラジドは生成しやすいと思います。
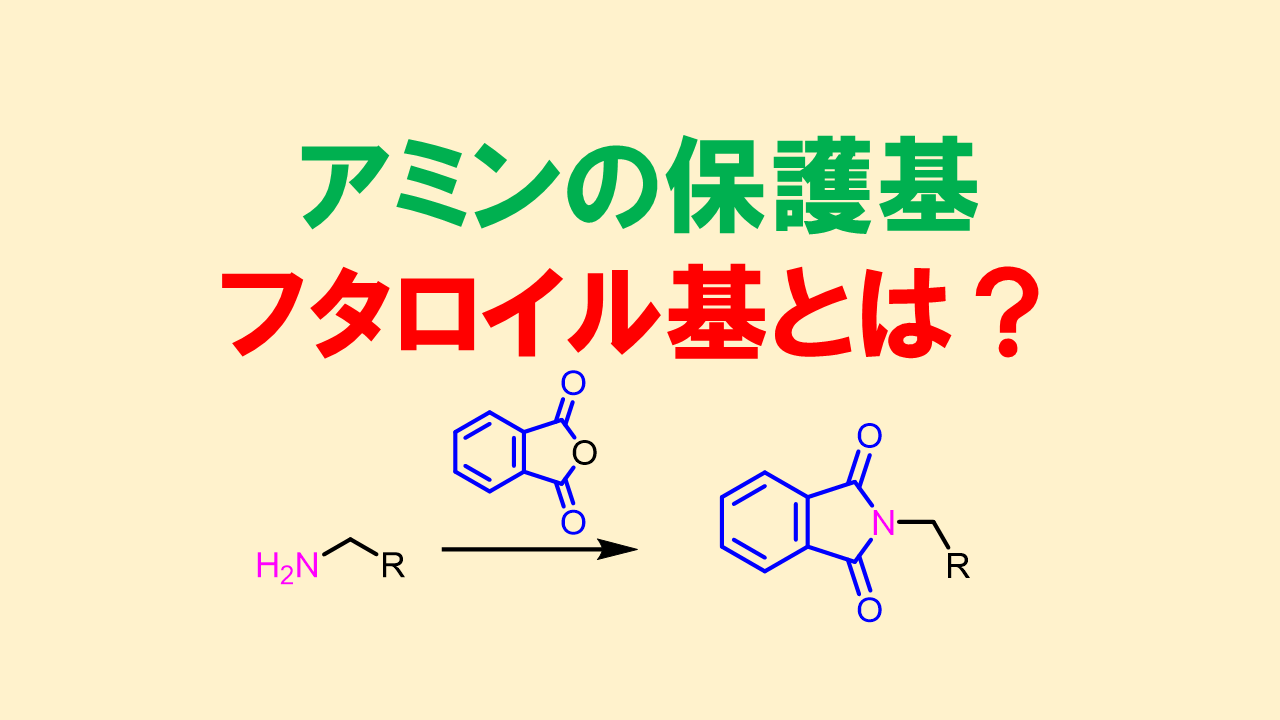
フタル酸ヒドラジドはアミンの保護基であるフタロイル基をヒドラジンで脱保護する時に副生成物として生成します。
ステップ4:べシャンプ還元でアミンに還元
最後にニトロ基をアミノ基に還元します。還元反応は信頼性と安全性が高い鉄を使ったべシャンプ還元で行います。経済的かつ収率もよいのでおすすめです。塩化アンモニウムといった弱酸でも反応が進行します。反応が進みにくければ熱を加えたり、酢酸を添加したりします。うまく行けばろ過、分液でルミノールが得られます。
まとめ
ルミノール自体の合成を考えてみたら意外と教育的な反応経路になりました。
ヒドラジンの潜在的な危険性が気になるところでもありますが、各反応は単純かつ基本的な反応であるため実験も簡単にできます。
基本的な反応で構築できるので高校の科学部でもできますね。試薬を揃えるのも簡単です。
初めて有機合成を学ぶ人に向けての練習実験としても結構意義がありそうです。
合成したルミノールを使って光らせてみるというのも面白いし、有機化学で重要な吸光・蛍光の概念を考えるきっかけにもなりますね!
最近はスーパーグローバル政策で留学生が多いらしいので、こういう実験をやってみて有機合成の基礎を楽しんで学んでもらうのもありですね。



ルミノールを作った後はそのまま反応させて問題ありませんか?
ご覧いただきありがとうございます。
そのまま使っても問題ないですが、再結晶して純度を挙げたほうが良いと思います