TLCやカラムクロマトグラフィーを行う上で、溶媒の極性を調べたいことがありますよね!
溶媒の極性を表す指標には誘電率があります。誘電率が高いほど極性が高いといえます。
溶媒の沸点や水への溶解度をまとめた表を作成しました。
溶媒の極性や沸点の表まとめ
| 溶媒 | 分子式 | 分子量 | 沸点(°C) | 融点(°C) | 密度(g/mL) | 溶解度(g/100g) | 比誘電率 | 引火点(°C) |
|---|---|---|---|---|---|---|---|---|
| ヘキサン | C6H22 | 86.18 | 69 | -95 | 0.655 | 0.0013 | 1.89 | -23.3 |
| ヘプタン | C7H16? | 100.2 | 98 | -90.6 | 0.684 | 0.01 | 1.92 | -4 |
| シクロヘキサン | C6H12? | 84.16 | 80.7 | 6.6 | 0.779 | <0.1 | 2.02 | -20 |
| ジオキサン | C4H8O2? | 88.11 | 101.1 | 11.8 | 1.033 | ∞ | 2.21 | 12 |
| テトラクロロメタン | CCl4? | 153.82 | 76.7 | -22.4 | 1.594 | 0.08 | 2.24 | -- |
| p-キシレン | C8H10? | 106.17 | 138.4 | 13.3 | 0.861 | Insoluble | 2.27 | 27 |
| ベンゼン | C6H6? | 78.11 | 80.1 | 5.5 | 0.879 | 0.18 | 2.28 | -11 |
| m-キシレン | C8H10? | 106.17 | 139.1 | -47.8 | 0.868 | Insoluble | 2.37 | 27 |
| トルエン | C7H8? | 92.14 | 110.6 | -93 | 0.867 | 0.05 | 2.38 | 4 |
| トリエチルアミン | C6H15N | 101.19 | 88.9 | -114.7 | 0.728 | 0.02 | 2.4 | -11 |
| o-キシレン | C8H10? | 106.17 | 144 | -25.2 | 0.897 | Insoluble | 2.57 | 32 |
| ジエチルエーテル | C4H10O | 74.12 | 34.6 | -116.3 | 0.713 | 7.5 | 4.34 | -45 |
| CPME | 106 | -140 | 0.86 | 1.1 | 4.76 | -1 | ||
| クロロホルム | CHCl3? | 119.38 | 61.7 | -63.7 | 1.498 | 0.795 | 4.81 | -- |
| クロロベンゼン | C6H5Cl | 112.56 | 131.7 | -45.6 | 1.1066 | 0.05 | 5.69 | 29 |
| 酢酸エチル | C4H8O2? | 88.11 | 77 | -83.6 | 0.895 | 8.7 | 6 | -4 |
| 酢酸 | C2H4O2? | 60.05 | 118 | 16.6 | 1.049 | ∞ | 6.15 | 39 |
| ジメチルエーテル | C2H6O | 46.07 | -22 | -138.5 | NA | NA | 6.18 | -41 |
| Me-THF | 80.2 | -136 | 0.85 | 14 | 6.97 | -11 | ||
| 1,2-ジメトキシエタン | C4H10O2? | 90.12 | 85 | -58 | 0.868 | ∞ | 7.2 | -6 |
| ジエチレングリコールジエチルエーテル | C6H14O3? | 134.17 | 162 | -68 | 0.943 | ∞ | 7.23 | 67 |
| THF | C4H8O | 72.11 | 66 | -108.4 | 0.886 | 30 | 7.6 | -21 |
| ジクロロメタン | CH2Cl2? | 84.93 | 39.8 | -96.7 | 1.326 | 1.32 | 9.08 | 1.6 |
| 1,2-ジクロロエタン | C2H4Cl2 | 98.96 | 83.5 | -35.3 | 1.245 | 0.861 | 10.42 | 13 |
| ピリジン | C5H5N | 79.1 | 115.2 | -41.6 | 0.982 | ∞ | 12.3 | 17 |
| t-ブチルアルコール | C4H10O | 74.12 | 82.2 | 25.5 | 0.786 | ∞ | 12.5 | 11 |
| 2-ブタノール | C4H10O | 74.12 | 98 | -115 | 0.808 | 15 | 15.8 | 26 |
| 1-ブタノール | C4H10O | 74.12 | 117.6 | -89.5 | 0.81 | 6.3 | 17.8 | 35 |
| 2-プロパノール | C3H8O | 88.15 | 82.4 | -88.5 | 0.785 | ∞ | 18.3 | 12 |
| 3-ブテン | C4H8O | 72.11 | 79.6 | -86.3 | 0.805 | 25.6 | 18.5 | -7 |
| 1-プロパノール | C3H8O | 88.15 | 97 | -126 | 0.803 | ∞ | 20.1 | 15 |
| アセトン | C3H6O | 58.08 | 56.2 | -94.3 | 0.786 | ∞ | 20.7 | -18 |
| エタノール | C2H6O | 46.07 | 78.5 | -114.1 | 0.789 | ∞ | 24.6 | 13 |
| HMPA | C6H18N3OP | 179.2 | 232.5 | 7.2 | 1.03 | ∞ | 31.3 | 105 |
| ジエチレングリコール | C4H10O3? | 106.12 | 245 | -10 | 1.118 | 10 | 31.7 | 143 |
| NMP | CH5H9NO | 99.13 | 202 | -24 | 1.033 | 10 | 32 | 91 |
| メタノール | CH4O | 32.04 | 64.6 | -98 | 0.791 | ∞ | 32.6 | 12 |
| ニトロメタン | CH3NO2 | 61.04 | 101.2 | -29 | 1.382 | 9.5 | 35.9 | 35 |
| DMF | C3H7NO | 73.09 | 153 | -61 | 0.944 | ∞ | 36.7 | 58 |
| アセトニトリル | C2H3N | 41.05 | 81.6 | -46 | 0.786 | ∞ | 37.5 | 6 |
| エチレングリコール | C2H6O2? | 62.07 | 195 | -13 | 1.115 | ∞ | 37.7 | 111 |
| グリセリン | C3H8O3? | 92.09 | 290 | 17.8 | 1.261 | ∞ | 42.5 | 160 |
| DMSO | C2H6OS | 78.13 | 189 | 18.4 | 1.092 | 25.3 | 47 | 95 |
| 水 | H2O | 18.02 | 100 | 0 | 0.998 | -- | 78.54 | -- |
| MTBE | C5H12O | 88.15 | 55.2 | -109 | 0.741 | 5.1 | - | -28 |
| 石油エーテル | -- | -- | 30-60 | -40 | 0.656 | -- | - | -30 |
| HMTP | C6H18N3P | 163.2 | 150 | -44 | 0.898 | ∞ | - | 26 |
エクセル版を下のリンクに貼っておきます。沸点順に並び替えたりできるので、便利だと思います。
溶媒の極性とは?
有機合成をする上で、極性の理解は非常に重要です。
極性を理解していないと反応の進行を調べるTLC(薄層クロマトグラフィー)や「精製」で利用するカラムクロマトグラフィーがうまく出来ないからです。
極性の高い溶媒は水のような溶媒
極性の低い溶媒はヘキサンなどの油です。
極性が生じるのは電子の偏りによるものなので、電気陰性度の高い原子が含まれていると極性が高くなることが多いです。極性の高い水やエタノール、アンモニアなどは、酸素や窒素といった電気陰性度の高い元素が入っています。
反対に極性の低い溶媒はヘキサンやトルエンといった炭化水素類で、電気陰性度の高い酸素や窒素などが入っていません。そのため、溶媒の極性が高いかどうかを知るにはその物質の構造が頭に浮かべば分かるようになってきます。
よく使用する有機溶媒の紹介!
ヘキサン(ノルマルヘキサン)
ヘキサンは研究室で最もよく利用する低極性溶媒です。
有機化学系の研究室ではアセトン、酢酸エチルとともに購入量トップ3の溶媒です。
使用用途は展開溶媒やオイル落とし
ヘキサンは酢酸エチルとともにカラムクロマトグラフィーやTLCの展開溶媒に用いることが多いです。
ヘキサンは極性が低いので油分をよく溶かすので、オイル落としに使います。
- オイルバスに浸かったフラスコのシリコンオイルの拭き取り
- 鉱油につかったナトリウムや金属水素化物の洗浄
オイル拭き取り性能はアセトンよりもヘキサンのほうが高いです。
また、アセトンは反応性が高いので反応利用するナトリウム等の洗浄には向いていません。
反応溶媒としての出番は少ない
極性官能基がなく化学的に安定なヘキサンですが、反応溶媒としての出番は少ないです。
- 極性が低すぎる(溶かせる分子の幅が狭い)
毒性があるので代替品の利用が進む
ヘキサンは代謝物の毒性があることから、ペンタンやシクロヘキサンなど他のアルカン類への代替がすすんでいます。
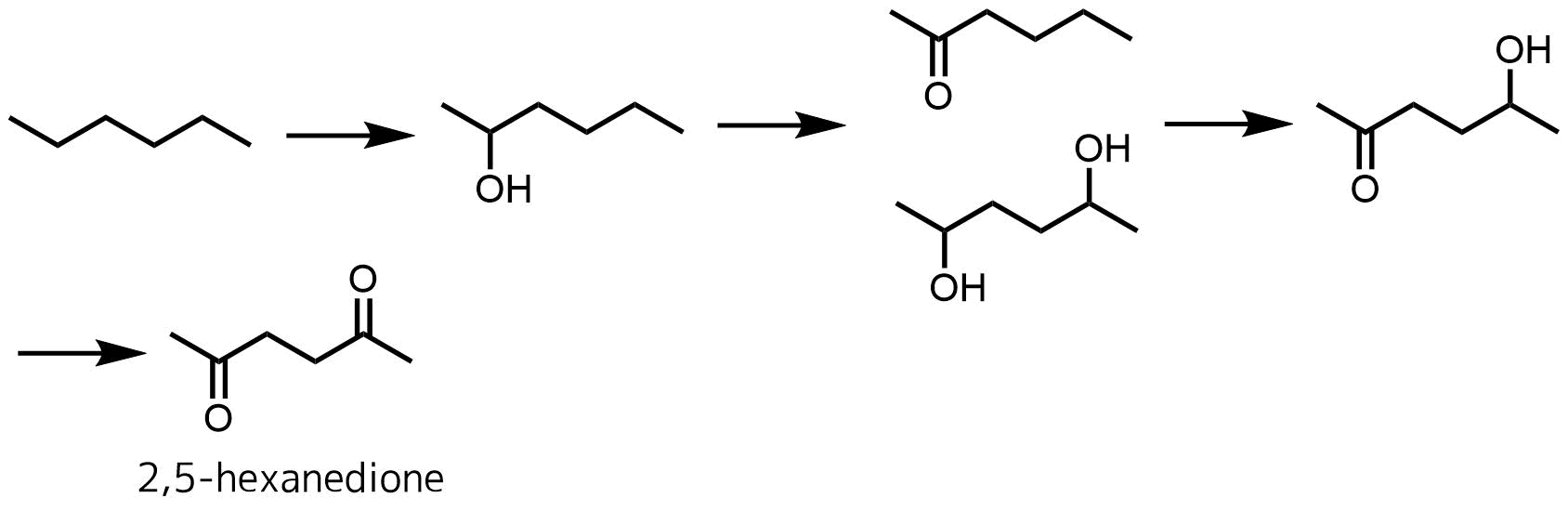
ヘキサンの代謝経路
Salamon, Fabiola, et al. “Urinary Levels of free 2, 5-hexanedione in Italian subjects non-occupationally exposed to n-hexane.” Applied Sciences 9.24 (2019): 5277.
ヘキサンの代謝物である2,5-ヘキサンジオンには神経毒性があることが知られています。
ヘキサン中毒の症状としては手足の末端部のしびれ、麻痺などのいわゆる末梢神経障害が見られます。
よく換気していれば問題は起こらないと思いますが、比較的大量に利用することが多いので吸入には注意したいところですね。
Couri, D., and M. Milks. “Toxicity and metabolism of the neurotoxic hexacarbons n-hexane, 2-hexanone, and 2, 5-hexanedione.” Annual Review of Pharmacology and Toxicology 22.1 (1982): 145-166.
代替品としては同じアルカン類のヘプタンやシクロヘキサンが利用できると思います。
ジオキサン (1,4-ジオキサン)
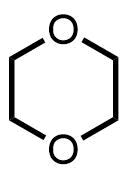
ジオキサンの構造
ジオキサンは環状エーテル類でテトラヒドロフラン(THF)と同じ仲間です。
ジオキサンの特徴は誘電率が低いにも関わらず、水と混和する点です。
ジオキサンは対称構造なので分子全体では双極子モーメントが0に近いですが、局所的な極性を有するために水と混和します。
分かりやすく言うと「水に溶けるヘキサン」というような感じです。
水との混合溶媒を極性調整可能な溶媒として利用
水とジオキサンの混合溶媒はジオキサンの比率を変化させることで混合溶媒の極性を任意に変化させることができます。
例えば、分子の周辺環境によって分子の吸収・蛍光波長・強度が変化するソルバトクロミック色素は油分中の水分量測定や生体環境中の分子周辺環境を知ることができるため有用です。
ジオキサンの濃度を10%, 30%, 50%…と変化させることで極性を自由に設定できるためソルバトクロミック色素の機能評価に用いることができます。
Åkerlöf, Gösta, and Oliver A. Short. “The dielectric constant of dioxane—water mixtures between 0 and 80.” Journal of the American Chemical Society 58.7 (1936): 1241-1243.
加藤亮, et al. “有機蛍光色素のソルバトクロミズムを利用する油中水分の測定.” 分析化学 60.6 (2011): 521-526.
非プロトン性溶媒としての利用
ジオキサンはプロトンを持たない非プロトン性溶媒として有用です。
どちらかというと同じ環状エーテルのTHFのほうが出番は多いと思います。ジオキサンはTHFと同様に過酸化物を形成したり、湿気をよく吸収するので脱水が難しいです。
ジオキサンは特定の金属カチオンと配位して錯体をつくる性質があります。例えば、グリニヤール試薬でジオキサンを溶媒に使用しないのは、グリニャール試薬と反応して錯体を形成するためです。
Fischer, Reinald, et al. “Structure–Solubility Relationship of 1, 4‐Dioxane Complexes of Di (hydrocarbyl) magnesium.” Chemistry–A European Journal 25.55 (2019): 12830-12841.
ベンゼンとトルエン
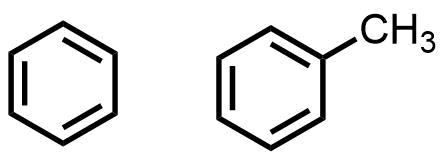
ベンゼンとトルエンは代表的な芳香族炭化水素系の溶媒です。
ベンゼンの毒性の高さは有名で現在はほとんど使用されることは無く、より毒性の低い代替のトルエンを利用することが多いです。
ヘキサンとは違って同じ炭化水素系の溶媒ですが、試薬を溶解能が高いので分液やクロマトグラフィーに使用したり、反応によっては溶媒として利用することもあります。
ジエチルエーテル
ジエチルエーテルは沸点が低く体温ほどの温度で沸騰します。
可燃性が非常に高いので、消防法で特殊引火物に認定されています。化学実習などでも溶媒として利用することが多いですが、引火性の高さから利用は注意します。
独特な甘く強い匂い、いわゆるエーテル臭があります。沸点が低いこともあり揮発しやすく室内に充満すると気分が悪くなることがあるので換気には注意し、ドラフト内で扱いましょう。
反応溶媒としては適度な極性を持ち、非プロトン性溶媒として優秀な面もありますが、沸点が低いため高い熱がかけられない点がデメリットです。一方で、加熱還流で高い温度をかけたなくない場合に使用すると良いでしょう。
分液時には揮発性の高さで容器内の圧力が高くなるで吹き出しに注意しましょう。
クロロホルムとジクロロメタン
クロロホルムは睡眠薬?のイメージが高く比較的有名な有機溶媒でしょう。反応でも用いることがありますが、3つの塩素によって比較的酸性度の高い水素があるため、強塩基性条件では使えません。同じことはジクロロメタンでも言えます。
クロロホルムは毒性の問題からクロロメタンへの代替が進んでいます(ジクロロメタンにも毒性があります)。
ジクロロメタンは試薬溶解能力が高く、化学的安定性も高いため反応溶媒として頻繁に利用されます。ジエチルエーテルと同様に沸点が低いため熱はあまりかけられませんが、ジエチルエーテルのような可燃性はないため安全性が高いです。
アセトン
アセトンはケトン類の溶媒でカルボニル基を持つため求電子性が高く反応しやすいため、反応溶媒として利用することは稀です。
水と混和し、多くの有機化合物を溶解するため洗浄用の溶媒として実験室でよく利用します。
DMF
ジメチルホルムアミドはアミド系の溶媒です。
極性の高い非プロトン性極性溶媒として反応によく利用されます。
ジクロロメタンやトルエン、エーテルに溶解しないような極性の高い有機化合物を溶解できるため反応溶媒としてよく利用します。
吸湿しやすいので脱水してから使います。
沸点が高いですが、ギリギリ蒸留することができます。同じく非プロトン性極性溶媒として利用されるDMSO(ジメチルスルホキシド)やNMP(N-メチル2-ピロリドン)は200℃近い沸点であるため蒸留が難しいのでこの点はDMFは有利です。
アセトニトリル
アセトニトリルはHPLCの移動相としてよく利用されますが、反応にも利用できます。
非プロトン性極性溶媒として利用されますが、THFと比べて利用頻度は落ちると思います。
DMFと比べて沸点が低いので扱いやすい非プロトン性極性溶媒です。
DMSO
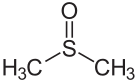
ジメチルスルホキシド(DMSO)は水を除く溶媒中で最も高い誘電率をもつ非プロトン性極性溶媒です。溶解力が大きく塩類など高極性な化合物も溶かします。求核置換反応の溶媒として優れていますが、DMSO自体にも反応性があるので注意します。
- 高極性
- 高沸点(189℃)
- 沸点付近で分解、(酸存在中では分解が加速してformaldehyde生成)
- 還元される(Zn, SnCl2)
- 強酸との反応(硫酸、塩酸)
- 求核性がある(無水酢酸などと反応)
佐藤武雄. “ジメチルスルホキシドの有機反応における溶媒および試薬としての応用 (その 1).” 有機合成化学協会誌



大変だと思いますが、続きを書いてほしいです!
ご覧いただきありがとうございます。
若干書き足しました!
DMSOの構造式は違っていますよ。
(CH3)2C=Sではなく、(CH3)2S=Oはずです
ありがとうございます。
DMSOの構造式が間違っていたので修正しました。