目次
野依不斉水素化について
野依不斉水素化は野依らが開発したキラルルテニウム触媒を使ったカルボニル化合物の不斉水素還元法です。
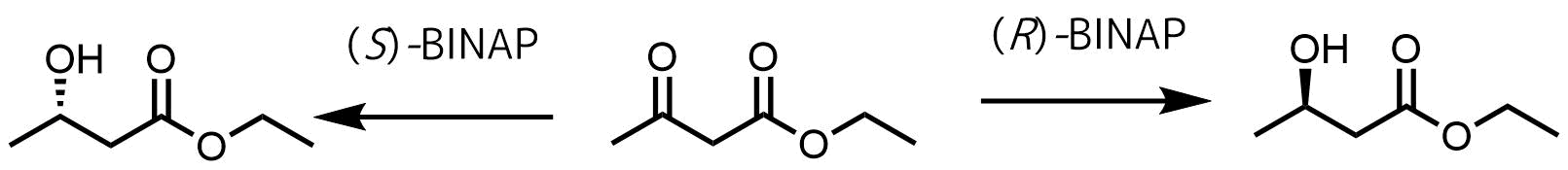
野依不斉水素化の概要
不斉水素還元触媒として、BINAP-Ru(II)錯体があります。
野依不斉水素化の特徴
BINAP-Ru(II)錯体を用いた不斉水素還元は触媒量で十分であり、高いエナンチオ選択的に還元が可能な触媒です。選択性は被還元化合物の置換基の影響を受けることが知られています。
目次
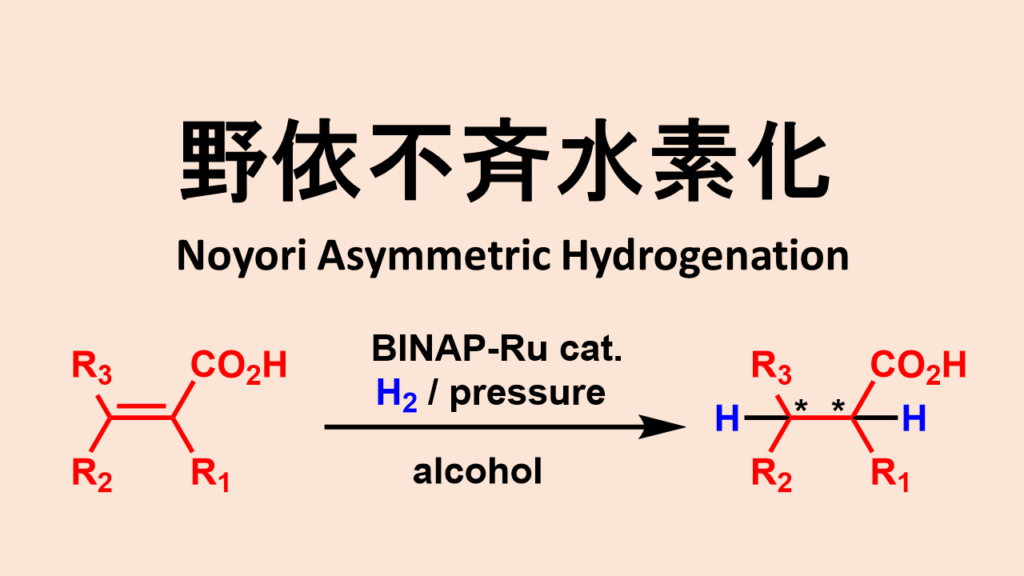
野依不斉水素化は野依らが開発したキラルルテニウム触媒を使ったカルボニル化合物の不斉水素還元法です。
野依不斉水素化の概要
不斉水素還元触媒として、BINAP-Ru(II)錯体があります。
BINAP-Ru(II)錯体を用いた不斉水素還元は触媒量で十分であり、高いエナンチオ選択的に還元が可能な触媒です。選択性は被還元化合物の置換基の影響を受けることが知られています。