目次
ロビンソン環化について
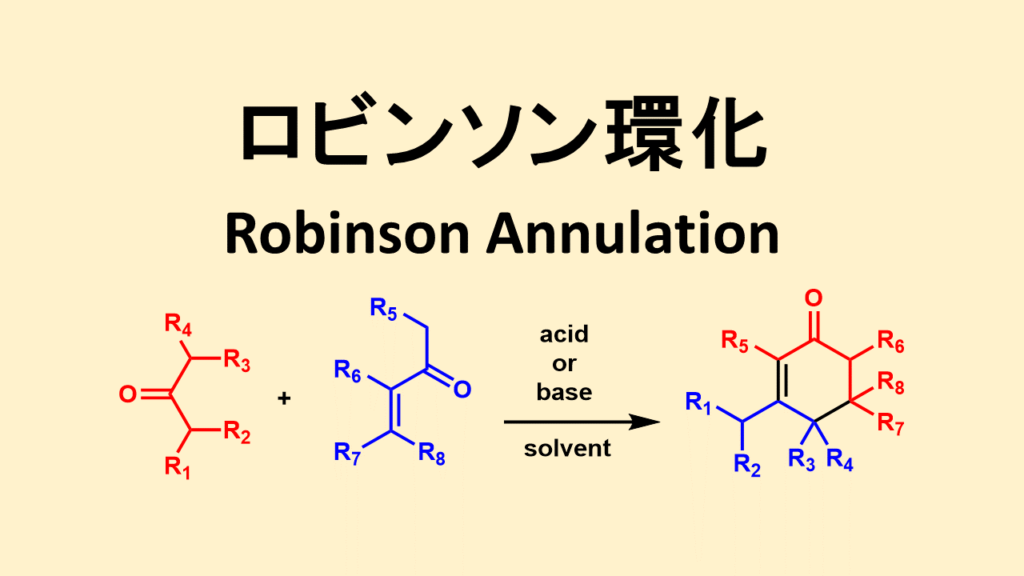
ケトン(主に環状ケトン)とα、β-不飽和ケトンから置換シクロヘキセノン誘導体が得られる反応はRobinson環化と呼ばれています。
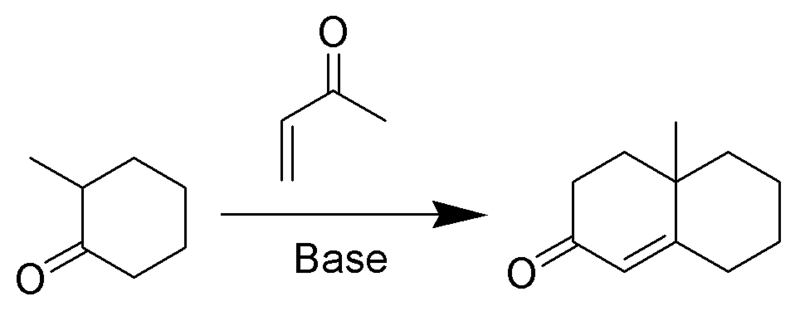
ロビンソン環化の概要 from wikipedia PD
ロビンソン環化は段階的な反応です。
ロビンソン環化は1935年にR. RobinsonとW. S. Rapsonにより報告されました。彼らはシクロヘキセノンから生じるエノラートが不飽和カルボニルと反応してシクロヘキセノンを生じることを発見しました。今日では環化反応として多用されています。
ロビンソン環化の特徴
ロビンソン環化はしばしば二環性の六員環化合物(シクロヘキセノン)の合成に利用されています。ロビンソン環化反応は大きく分ければマイケル反応とアルドール反応の二種類で構成されています。
触媒としては塩基の他、酸を用いることもできますが、塩基がよく用いられます。
ワンポットでも合成可能ですが、収率向上のため、Michael付加体を単離した後にアルドール反応を別に行うほうがきれいに進行することが多いです。
反応機構
Robinson環化は塩基によりエノラートが生成するところが第一段階です。エノラートはαβ不飽和カルボニルに対して1,4付加反応(マイケル反応)を起こします。再度塩基によってエノラートが生成し、ケトンに対してアルドール反応を起こします。ケトンが再生し、シクロヘキセノンが生成します。
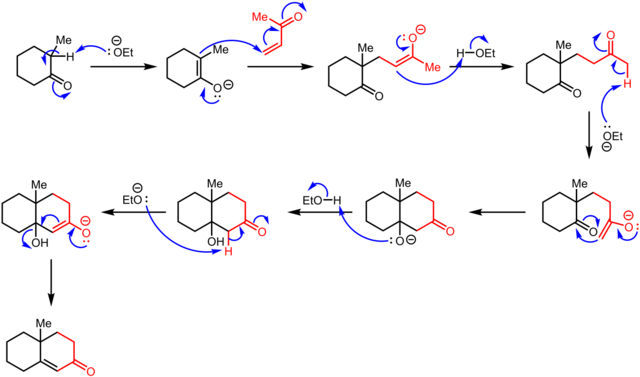
ロビンソン環化反応の機構 by English Wikipedia user Alsosaid1987 CC3.0