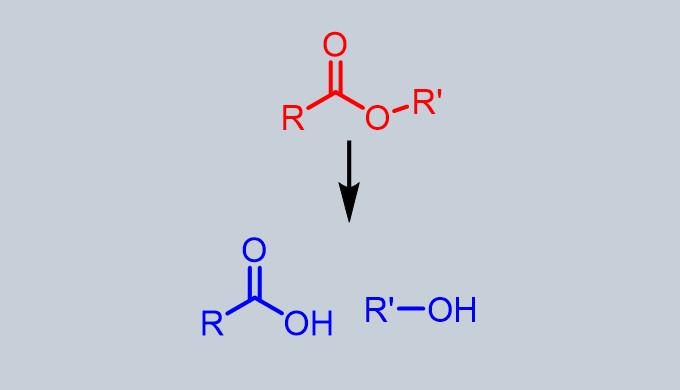
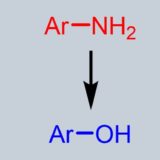
エステルの加水分解でアルコールとカルボン酸が生成します。
エステルの加水分解でアルコール合成
エステルの加水分解はアルコール側に着目すれば、アルコール合成に、カルボン酸側に着目すればカルボン酸合成が可能です。
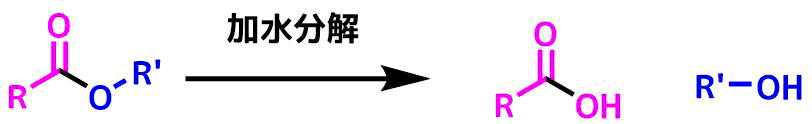
エステルの加水分解でアルコールの合成
エステルを原料にアルコールを合成するというパターンはどちらかと言えば少ないかな?という印象です。
アルコールをアセチル保護した場合がこの例に当たります。
エステルの加水分解は通常容易に進行します。
炭酸カリウムーアルコールや水酸カリウム、ナトリウム、リチウムを使ったりします。反応が進行しにくければ加熱還流します。
塩基に弱い場合は還元的に外したりもできる。
通常アルカリ条件がつかわれますが、
- 塩基性に弱い基質
- t-Buエステル
などでは酸性条件が使われます。
またベンジルエステルなどでは接触還元など還元的に外します。
単純なアルキル・フェニルエステルの加水分解
メチル・エチルエステルやアセチル基などの加水分解はアルカリ金属の水酸化物やアルカリ炭酸塩などで加水分解します。溶媒はアルコールやTHFをよく使用します。
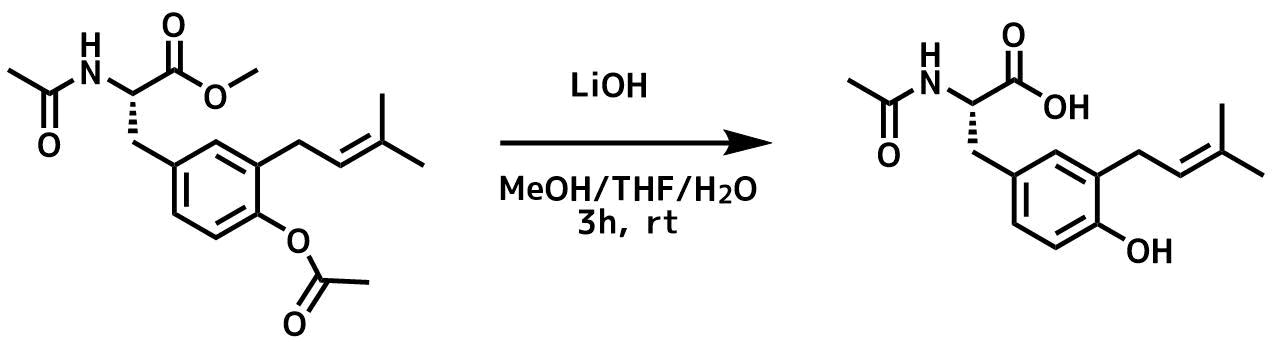
Mansha, M. et al Synthetic Communications, 45(5), 609-614; 2015
水酸化リチウム一水和物(0.096g、2.3mmol)をエステル(0.16g、0.46mmol)のTHF/MeOH/H2O=3:1:1(10mL)の溶液に加え、室温で3時間撹拌した。濃縮、クロロホルム、1MHClで分液して精製操作を行って目的物を69%で得た。
LiOHはKOHやNaOHよりも加水分解が効率的に進行するようです。
塩基としてはナトリウムメトキシド/MeOHなども使います。酸(HClやAcOH、Dowex)でも加水分解可能ですが、通常は塩基を使います。
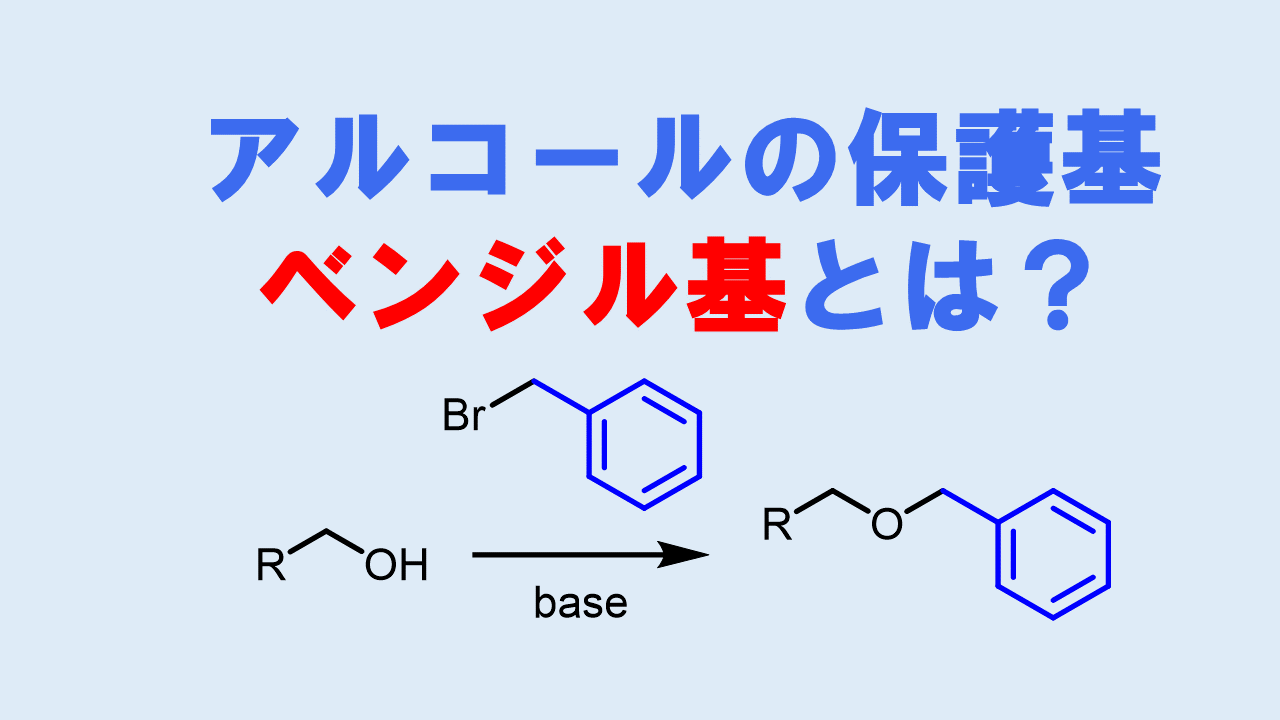
ベンジルエステルの加水分解
ベンジルアルコールのエステルは通常の塩基性条件による脱保護は進行しにくいです。ベンジルアルコールはPd/Cによる接触還元により効率的に脱保護できます。
ベンジルエステルはPd/CやPd(OH)2などのパラジウム触媒を用いた接触還元により容易に外せます。
ベンゾイルエステルの加水分解
ベンゾイルエステルは脂肪族カルボン酸エステルよりも頑丈で加水分解しにくいです。酸には結構強いです。塩基性条件では加水分解しますが、温度が必要な場合があります。
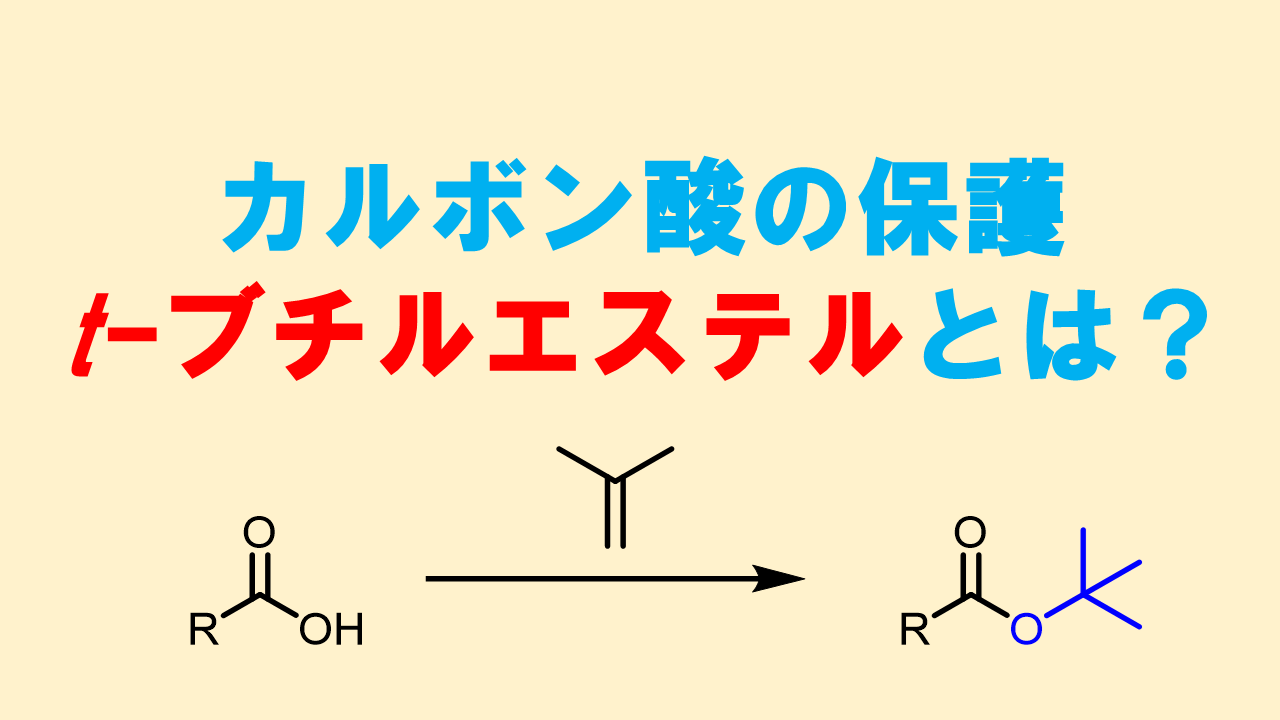
t-Buエステルの加水分解
t-Buエステルは嵩高いので塩基による加水分解は進行しにくいですが、t-Bu基は第三級アルキル基のため、酸性条件ではカルボカチオンを生成しやすく加水分解します。