キサントプロテイン反応はタンパク質を検出する呈色反応です。キサントプロテイン反応では、タンパク質中に含まれる芳香族アミノ酸であるチロシンとトリプトファンがニトロ化することで黄色に変化する現象をりようします。濃硝酸が手につくと黄色く変色するのはこのキサントプロテイン反応が起きているからです。
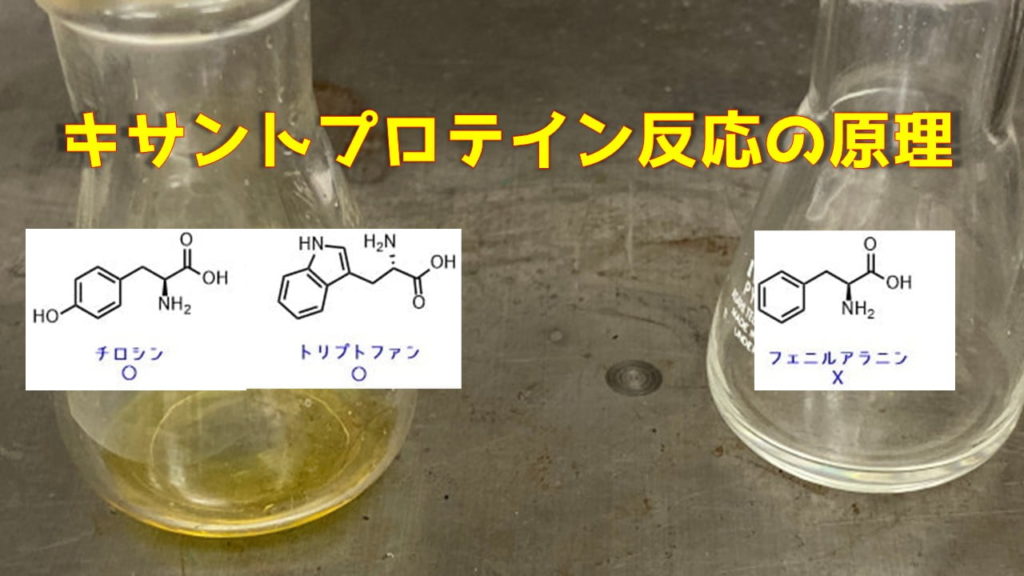
キサントプロテイン反応の原理
キサントプロテイン反応はタンパク質の検出方法です。
タンパク質に濃硝酸を少量加えると黄色に変色する反応を利用します。
 こめやん
こめやん
キサントプロテイン反応は言い換えると「芳香族のニトロ化反応」です。
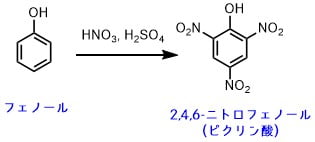
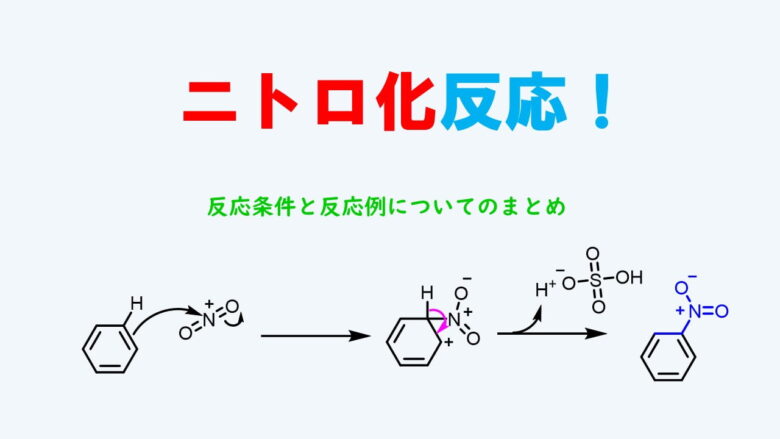
ニトロ化反応
上の反応が典型的なニトロ化です。反応前のフェノールは無色です。

フェノールの結晶 by Bartłomiej Bulicz [CC BY-SA 3.0 (https://creativecommons.org/licenses/by-sa/3.0)]

ピクリン酸の結晶 Indiamart,Powder Picric Acid https://www.indiamart.com/proddetail/picric-acid-4884454055.html
このようにニトロ化すると色が黄色に変色します。これはニトロ基(-NO2)が発色団といって芳香環に結合すると呈色する構造であるからです。
 こめやん
こめやん
タンパク質はアミノ酸がたくさん連なってできた「高分子」ですが、このアミノ酸の中には芳香族(ベンゼンとか)を持つアミノ酸があります。
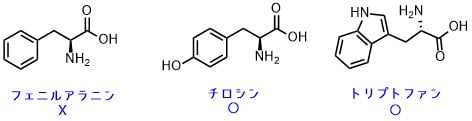
芳香族アミノ酸一覧
これらの芳香族アミノ酸の芳香環がニトロ化することによって黄色に変化します。つまり、タンパク質ではなくてもアミノ酸のチロシンだけでも黄色に変色するので、芳香族アミノ酸を検出する方法ともいえます。
 adeno
adeno
芳香族アミノ酸が含まれなければニトロ化が起きないので、黄変しません。例えば、コラーゲン及びゼラチン(変性コラーゲン)には芳香族アミノ酸はほとんど含まれないので変色しにくいです。
また、芳香族アミノ酸でもヒスチジン(イミダゾールを含む)やフェニルアラニンは呈色されません。それはニトロ化反応が進行しにくいからです。
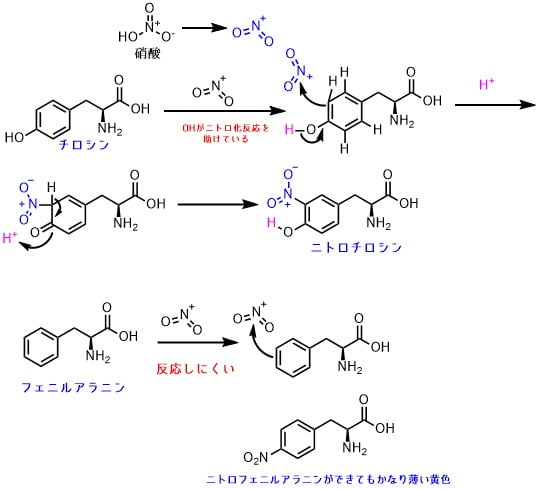
芳香族アミノ酸のニトロ化
チロシンの芳香環は水酸基があるフェノールです。水酸基の電子がベンゼン環に流れることによって、電子が豊富になるので、電子不足のニトロニウムイオン(+NO2)に対しての攻撃性が増します。これによってニトロ化反応は進行しやすくなります。
一方、フェニルアラニンは水酸基が無いため環の反応性が落ちています。そのためニトロ化反応が進行しにくいです。また、フェニルアラニンがニトロ化しても生成物の色は薄い黄色で検出しにくいです。

左 チロシン、右:フェニルアラニンのキサントプロテイン反応。フェニルアラニンは着色が殆どないのがわかる
 こめやん
こめやん
アンモニアや水酸化ナトリウムを入れると色が変化(橙色)する理由
ニトロ化した後にアンモニアや水酸化ナトリウムを加えて色の変化をみる実験をやることがあります。これによって、色が変化するのですがなぜしょうか?
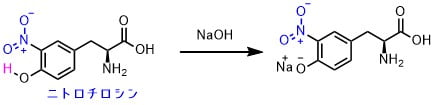
塩基性条件におけるニトロチロシンの構造変化
これは、ニトロチロシンを例に上げると、酸性中ではフェノールがOHになっていますが、中和、塩基性にするとフェノールが塩基と反応してナトリウムフェノキシドに変化します。このように構造が塩基性と酸性ではことなるので色の変化が起こります。
ニトロ化反応で混酸(硫酸と硝酸)を使わない理由は?
ニトロ化反応のファーストチョイスは硝酸に硫酸を加えたいわゆる「混酸」を使った条件です。
キサントプロテイン反応では濃硝酸しか使用していませんが、なぜでしょうか?その理由としては、
- チロシンやトリプトファンでは濃硝酸で十分ニトロ化が進行する
- 濃硫酸は扱いにくく危険
- 混ぜる操作が面倒
- フェニルアラニンをニトロ化させたところで着色は薄いので意味ない
というような理由が考えられます。
検出方法を開発するときはなるべく簡単でシンプルなほうが良いですから、色の薄いニトロフェニルアラニンを作らなくてもよいってことですかね?



質問なのですが、『化学の新研究』という文献で、チロシンの発色の理由について調べたところ、ニトロチロシンからo-キノン型構造を生成し、そのキノン型構造が発色団であるから、この物質は発色するんだとありました。ナトリウムフェノキシドが発色するというのは可能性としてはあるかもしれませんが、アンモニアだとナトリウムフェノキシドは生成しないと考えています。どう思われますか。参考文献として『化学大事典2』のp.770も用いました。
アルカリ溶液中ではフェノールが脱プロトン化された構造に変化し、これはいわゆるフェノールの酸素をドナー基、電子求引性のニトロ基をアクセプター基とするドナー-アクセプター発色系と呼ばれ、一般的に知られる多くの染料や顔料はこの形をとっています。
脱プロトン化されたあとの構造については詳しく言及していませんでしたが、共鳴構造中でo-キノイド型をとり、こちらの構造が発色に寄与しているという考察はキノン類の発色例を見ればそうと言えそうです。話はそれますが、ニトロチロシンの部分構造であるニトロフェノールは発色機構を研究するための好例で今に至っても研究が行われています。
1) Reichelt, Hendrik, Chester A. Faunce, and Henrich H. Paradies. “Structures of the 2-nitrophenol alkali complexes in solution and the solid state.” The Journal of chemical physics 143.4 (2015): 044307.
2) Nielsen, Steen Brøndsted, Mogens Brøndsted Nielsen, and Angel Rubio. “Spectroscopy of nitrophenolates in vacuo: effect of spacer, configuration, and microsolvation on the charge-transfer excitation energy.” Accounts of chemical research 47.4 (2014): 1417-1425.