水素化カリウムはアルカリ金属の水素化物で強塩基です。有機合成ではプロトンの引き抜きに利用されます。同じくアルカリ金属水素化物の水素化ナトリウムと比べて利用頻度は少なめです。
水素化カリウム (KH)とは?
水素化カリウムはカリウムの水素化物で、水素化ナトリウム (NaH)
と同じくOH、NH、SH、CH等の水素を引き抜くのに利用される強塩基です。水素化ナトリウムと比べて水素化カリウムのほうが塩基性が高いです。
水素化カリウムは水と反応すると失活して水酸化カリウムと水素になります。水と激しく反応するため、水との接触は避けて保存しましょう。空気中の水蒸気と反応するため取扱は不活性ガス雰囲気下で行います。
水素化カリウムのプロパティ
- 分子量 : 40.11
- 化学式 : KH
- 密度 : 1.47
- 溶解性 : 水・アルコールは分解する。多くの有機溶媒に不溶
水素化カリウムの失活を確かめる方法
水素化カリウムも失活しやすいので失活していないか確かめる必要があります。簡単な方法はミクロスパーテルにごく少量とって、それを水の中に入れることです。水に入れた時に音を立てて反応すれば失活していません。何も起こらなかった場合は失活している可能性が高いので、再購入しましょう。
水素化カリウムの洗浄方法
水素化カリウムも反応性を抑えるために鉱物油に混じった状態で市販されています。鉱物油が気になる場合は脱水ヘキサン等で洗浄してから反応に利用します。洗浄方法は不活性ガス雰囲気下で脱水ヘキサンを加えて上澄みのヘキサンを捨てます。詳しい方法は水素化ナトリウムの記事に載せているのでそちらを参照してください。

水素化カリウムは反応性が高いので取扱いは注意します。
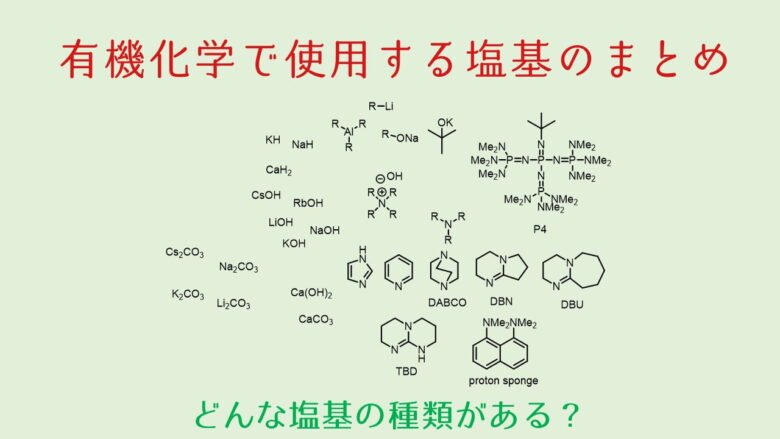
水素化カリウムを使用する有機化学反応
水素化カリウムは基本的に水素化ナトリウムと似たような使い方ができます。逆に言えば、水素化ナトリウムが使用できるタイミングで水素化カリウムを使用するメリットはあまりないかもしれません。水素化カリウムが使用される反応例としては、
- Williamsonエーテル合成
 ウィリアムソンエーテル合成: Williamson Ether Synthesis
ウィリアムソンエーテル合成: Williamson Ether Synthesis
などがあります。
水素化カリウムを利用する時は、水素化ナトリウムでは十分に反応が進行しなかった場合などです。例えば、嵩高いアルコールをアルコキシドに変換する場合などが当てはまります。脂肪族第三級アルコールや、2,6-tBuフェノールなどの嵩高いアルコール・フェノール類の脱プロトン化は進行しにくいですが、水素化カリウムでは進行します。水素化ナトリウムでは反応の進行が遅いような場合でも水素化カリウムを使用すると改善することがあります。
 こめやん
こめやん
水素化ナトリウムと水素化カリウムとで、反応性の差が生じる例としては、ジメチルスルホキシドの脱プロトン化があります。ジメチルスルホキシドのCH3のプロトンは水素化ナトリウム (NaH)では脱プロトン化が起こりませんが、水素化カリウム (KH)では脱プロトン化が進行します。
また、水素化ナトリウムとでは、立体選択性が異なることがあるので、試してみても良いかもしれません。
参考リンク
1) EROS Potassium Hydride
2) wikipedia 水素化カリウム


水素化カリウムは水と反応すると失活して「水酸化ナトリウムと水素になります。」ではなく、「水酸化カリウムと水素になります。」だと思われます。
ご指摘ありがとうございます。
水酸化カリウムに修正いたしました。