ペーパークロマトグラフィーは最も古いクロマトグラフィーの一種で、安価で簡便ですが、性能面では不利なので実際の実験の現場で用いられることは少ないですが、学習実習や自由研究などではよく利用されると思います。
ここではペーパークロマトグラフィーのやり方や原理や結果に対する考察を紹介していきます。
ペーパークロマトグラフィーとは?
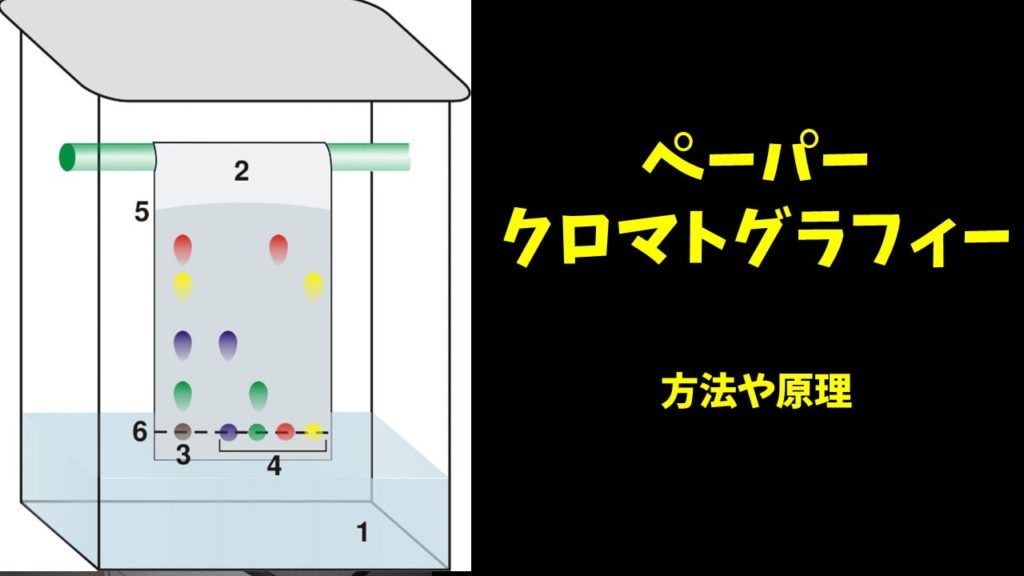
ペーパークロマトグラフィーは紙(ろ紙)を固定相、有機溶媒を展開溶媒として分離する方法です。
混合物はろ紙との相互作用の大きさの違いによって、複数のスポットに分離します。
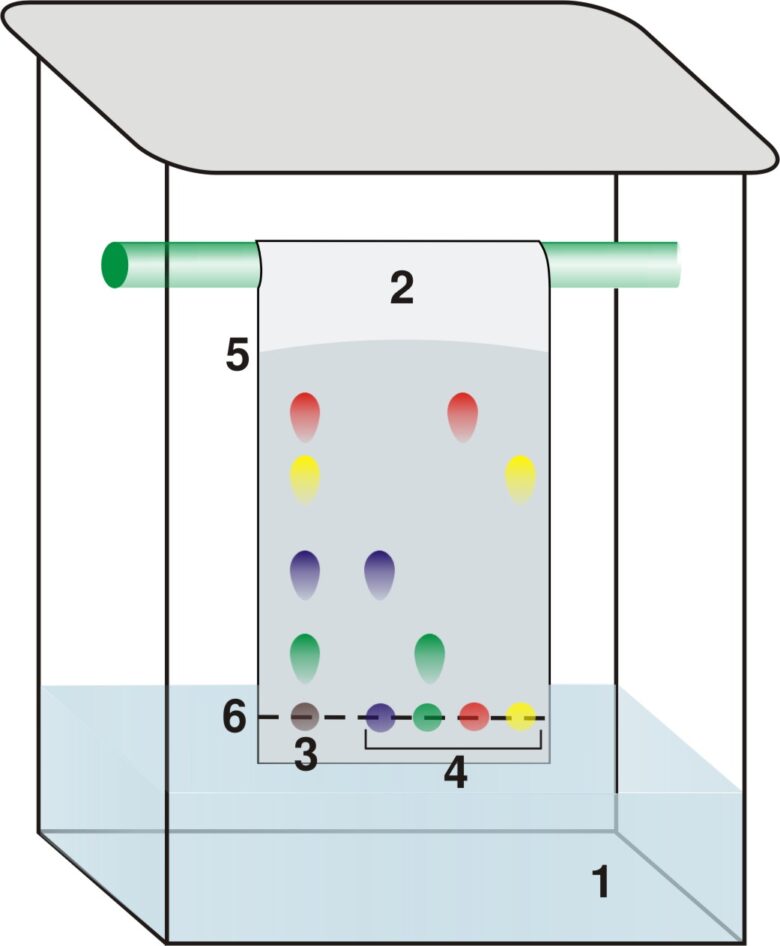
ペーパークロマトグラフィー from wiki (public domain)
ペーパークロマトグラフィーは1944年Martinらによって開発されました。
ペーパークロマトグラフィーを構成する要素
展開溶媒
極性の高い生体物質(アミノ酸や糖類)は水系の溶媒を使います。
- アルコール系(n-ブタノール、エタノール、メタノール、ベンジルアルコール、イソアミルアルコール)
- フェノール系 (フェノール、m-クレゾール)
- ピリジン系 (ルチジン、コリジン)
がよく利用されます。展開溶媒に水を何割か加えることも多いです。また、イオン性の化合物の場合は酸やアルカリ(HCl、AcOH、NH3など)を添加することもあります。
親水性無い化合物の場合は、
- アルコール系 (メタノール、エタノール)
- ベンゼン系(ベンゼン、トルエン、キシレン)
- ケトン (アセトン)
などあらゆる有機溶媒が利用可能です。
ろ紙
ろ紙は基本的に有機化合物であれば、Whatman No.1が汎用的です。濾紙 No.2も良いです。
無機分析の場合は、No.3やNo.5Aが使われます。
ペーパークロマトグラフィーの操作
- 濾紙似試料は下端3cmくらいの所に毛細管を使って直径2mmくらいにスポッティングする。試料が薄いときは複数回に分けて重ね塗りする。複数試料があるときは間を3cmくらいあける。
- 展開槽に予め展開溶媒を加えて5分くらい待ったものに下端を下にして濾紙を入れる
- 20-30cmくらい展開したら取り出して乾燥させる
- UV吸収があればUV検出、それ以外はニンヒドリンやドラーゲンドルフ試薬、DNPなどの検出試薬を利用する
原理と展開結果の考察
ペーパークロマトグラフィーによって展開された結果をどのように考察したらよいでしょうか?
成功すれば、混合物を分離すると異なるRf値(高さ)を与えるスポットが観察できます。
ペーパークロマトグラフィーの担体、固定層はセルロースです。
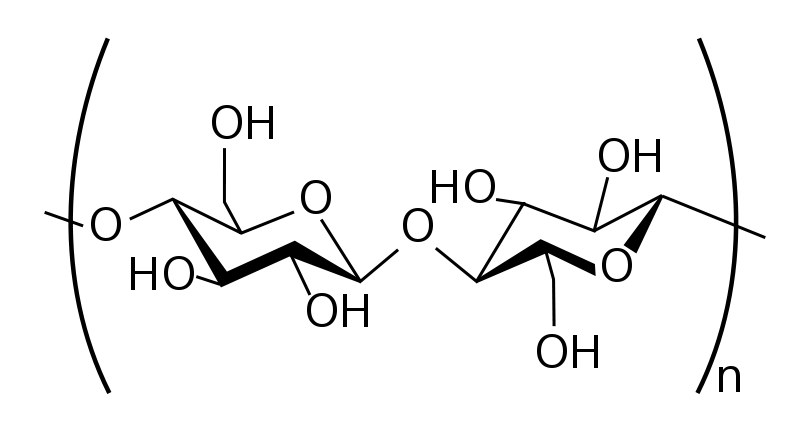
セルロースの構造 from wiki (public domain)
セルロースは糖類からなる化合物で表面には極性の高い水酸基があります。
このセルロースに対して親和性が高ければ紙に張り付きやすく上には上がりにくくなります。
その点では親水性の化合物のほうが吸着しやすいと考えられますが、実際のペーパークロマトグラフィーでは展開溶媒への溶解性が結構影響します。
展開溶媒への親和性のほうが固定相への吸着力よりも大きな影響を与えるようです。