ドラーゲンドルフ試薬は主に第3,4級アミンを検出することができるアミンの検出試薬です。スコポラミンやニコチンなどアルカロイドは第三級アミンを持つことが多いためアルカロイド検出試薬としてドラーゲンドルフ試薬は使われます。ドラーゲンドルフはTLCの発色試薬としてもよく利用されます。
ドラーゲンドルフ試薬 (Dragendorff reagent)は第三級アミンを検出するTLC発色試薬
ドラーゲンドルフ試薬はニンヒドリンに次いで有名なアミン検出を検出する発色試薬です。ドラーゲンドルフ試薬は化学者Georg Dragendorff(1836-1898)によって開発され、天然物抽出液中のアルカロイド(窒素原子を含む塩基性の天然化合物)の検出に利用されました。
Dragendorff G(1866) Ueber einige neue Reagentien auf Alkaloide. Pharm Zschr Russl 5: 82–85.
初期のドラーゲンドルフ試薬は硫酸ビスマスと小過剰のヨウ素をガラス管中で加熱して調製したヨウ化ビスマスと濃厚なヨウ素カリウム水溶液と混合させて調製しています。
ドラーゲンドルフ試薬の検出感度0.01 ~ 0.1 ug/mLと高いため微量でも検出可能です。
検出感度が高いことから、未知試料天然物中に含窒素化合物が含まれるかを調べるのに使われています。
ニンヒドリンは第一級アミン、第二級アミンなど級数が小さいアミンのほうが濃く発色しますが、ドラーゲンドルフ試薬は第三級アミン、第四級アミンのほうが良く発色します。第二級アミンは発色しても薄く、第一級アミンは色がつかないです。これはニンヒドリンの発色機構がアミンのニンヒドリンへの求核攻撃によるものに対して、ドラーゲンドルフ試薬がビスマスとの錯体形成によるものであるため、塩を形成しやすい第四級や第三級アミンのほうが反応しやすいからです。逆にニンヒドリンでは求核性の低い第三、第四級アミンは呈色しにくいです。
沈殿の形成
ドラーゲンドルフ試薬はtlc発色試薬として用いる以外に溶液に添加して沈殿の有無によりアミン類を検出する方法もあります。
アミンがドラーゲンドルフ試薬と反応すると橙色の沈殿が生じます。これは水溶性のアミンが不溶性の錯体を生じるためです。錯体の色はアミンの種類によって微妙に変化し、橙色、黄色、赤、赤黒、紫、ピンクと様々です)1。
1) Coe, F. G., & Anderson, G. J. (1996). Screening of medicinal plants used by the Garifuna of Eastern Nicaragua for bioactive compounds. Journal of Ethnopharmacology, 53(1), 29-50.
ドラーゲンドルフ試薬でアミンのアルキル化を検出する
第一級アミンをアルキル化して第二級、第三級アミンを合成する時に目的のアミン体が合成できたかどうかをドラーゲンドルフ試薬とニンヒドリンを組み合わせて使用すると分かりやすいのでおすすめです。
ニンヒドリンは第一級アミンとよく反応するのに対してドラーゲンドルフ試薬は第三級アミンとよく反応するからです。アミンのTLCは綺麗に展開されない事もあるので発色試薬と組み合わせると同定がスムーズになります。
ドラーゲンドルフ試薬が呈色や沈殿を生じる原理
ドラーゲンドルフ試薬は古くからアルカロイド類の検出に用いられている試薬ですが、ドラーゲンドルフ試薬の原理はまだ完全には解明できていないようです。
推定される機構は以下のようになります。
ドラーゲンドルフ試薬には次硝酸ビスマス、酸(酒石酸、酢酸、塩酸等)、ヨウ化カリウムが入っています。これらが反応して活性種であるKBiI4が生成します。
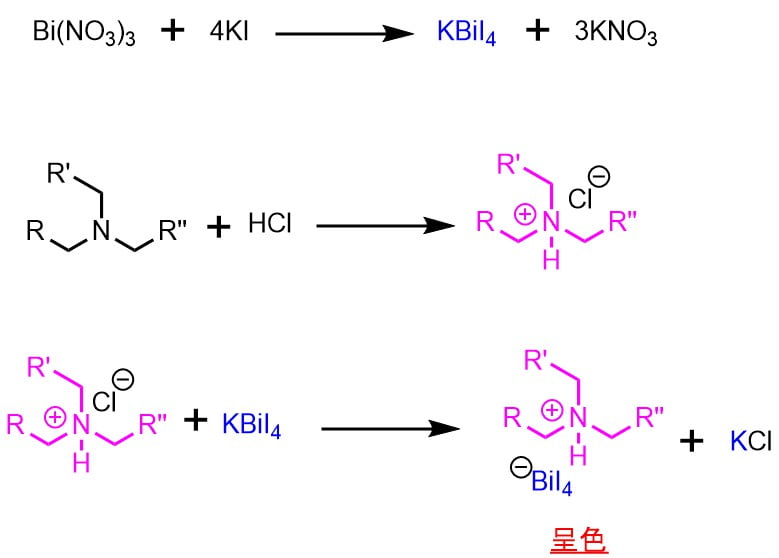
次硝酸ビスマスがヨウ化カリウムと反応してKBiI4が生成します。アミンはドラーゲンドルフ試薬中の酸と反応してアミン塩を生成します。このアミン塩にKBiI4が反応してアミン錯体を形成します。これが沈殿呈色します。
ドラーゲンドルフ試薬で検出するアミン類
上記の原理に基づけば、アミン塩となればドラーゲンドルフ試薬で呈色・沈殿を生じると考えられます。実際にドラーゲンドルフ試薬はアルカロイド、すなわち含窒素化合物の検出に用いられています。
アルカロイドの代表例であるニコチンは第三級アミンを含むため反応して沈殿が生じます(ドラーゲンドルフ試薬陽性)。ニコチンのような第三級アミンを含む塩基性の高いアルカロイドはカチオン種と反応して安定した塩を形成しやすいため、呈色や沈殿が生じやすいです。
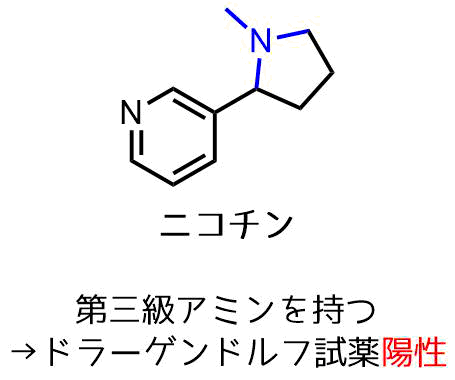
ニコチンはドラーゲンドルフ試薬陽性
一方で、アルカロイドといってもアミンを含まない含窒素化合物もあります。例えば、ピペリン、カフェイン、テオフィリン、リシニンなどが挙げられます。
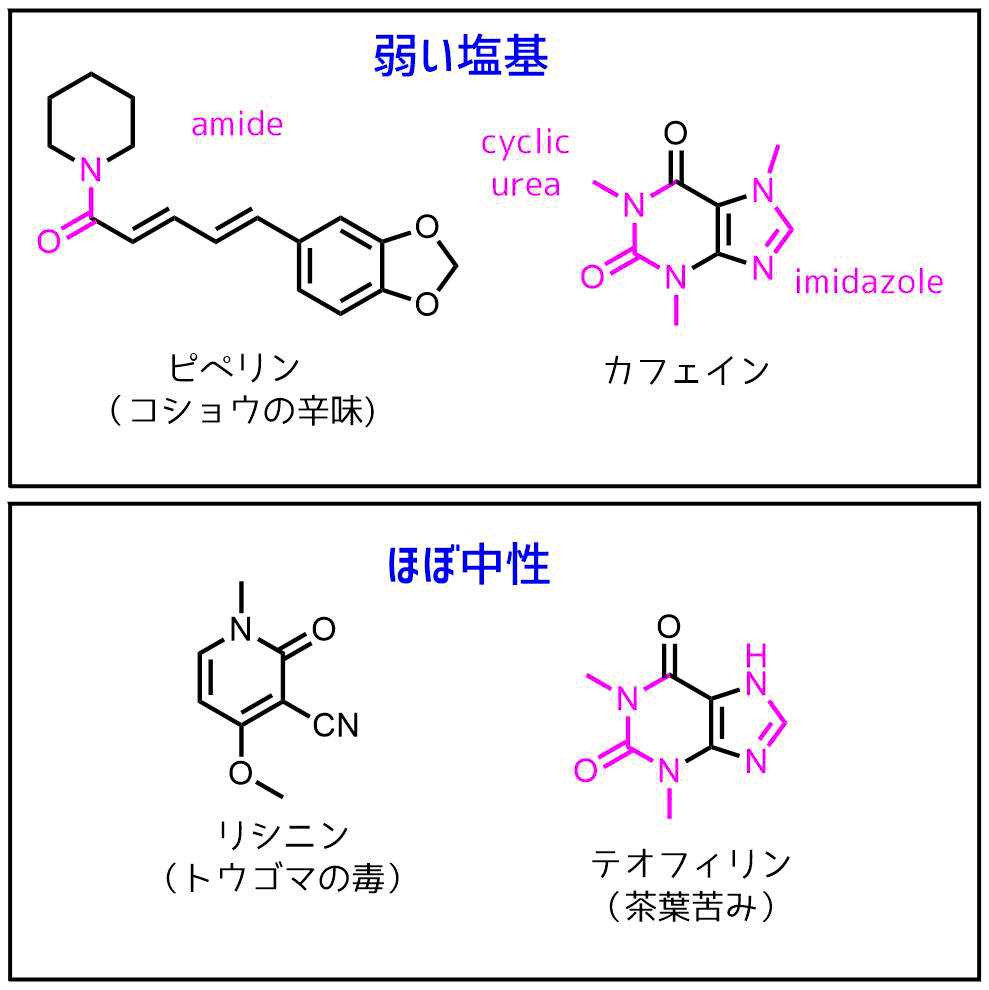
塩基性の低いアルカロイドの例
これらの化合物はアミドやウレアなど塩基性の低い窒素原子を含むため安定した塩を作りにくいです。安定した塩を作るためには溶液の酸性度を高くする必要があります。
一般的にドラーゲンドルフ試薬ではカフェインなどの塩基性の低いアルカロイドでも沈殿が生じるとされていますが、試薬の調製方法や操作手順によっては沈殿が生じないこともあるので注意が必要です。下記動画ではカフェインはドラーゲンドルフ試薬を用いても沈殿が生じていません。
上記の動画はBisbuth oxynitrate、AcOH、KI、水を用いたレシピです。この方法で作るドラーゲンドルフ試薬はあまり感度が高くないため、カフェインやテオフィリンは検出されないようです。
ドラーゲンドルフ試薬は調製法がたくさんあり、塩酸や硝酸を加えたり、酒石酸を使用する例、試薬を加えたのち加熱して生じた沈殿をろ過する例、調整後に時間を置く例など多数報告されています。
塩基性の低いアルカロイドでは塩酸や硝酸を加えたバージョンのドラーゲンドルフ試薬あるいはあるいは硫酸や硝酸によって強酸塩を用いたほうがよいです。
Beale, Robert, and G. Chandlee. “Volumetric Determination of Bismuth as Caffeine Tetraiodobismuthate (III).” Industrial & Engineering Chemistry Analytical Edition 14.1 (1942): 43-44.
KIや塩酸の量を増やしすぎると沈殿が溶解してしまうという報告もあり、対象の物質に合わせたレシピを用いる必要があるでしょう。この辺りは論文を参考に目的の物質を検出しやすいレシピを選択する必要があるかもしれません。
濃度等条件によっては錯体形成が起こっても沈殿が生じない場合もあります。
三井利幸, and 藤村義和. “ドラーゲンドルフ試薬作製条件の検討.” 衛生化学 21.4 (1975): 183-187.
ドラーゲンドルフ試薬の調製には酢酸がメインで使われることが多いですが、酢酸の代わりに硝酸を用いた試薬はModified ドラーゲンドルフ試薬、Kraut’s試薬として知られています。
Kumar, Sunil. “Alkaloidal Drugs-A Review.” Asian Journal of Pharmaceutical Science & Technology 4.3 (2014): 107-119.
このkrauts試薬はカフェインの検出に最適です。
Stephenson, Charles Henry, and Charles Edwin Parker. Some Microchemical Tests for Alkaloids. JB Lippincott, 1921.
ドラーゲンドルフ試薬の偽陽性に注意
ドラーゲンドルフ試薬は簡便な溶液中のアルカロイド検出に用いられることが多いですが必ずしもアルカロイド、含窒素化合物のみを検出するわけではないことに注意しましょう。
特に天然物抽出物を検体に用いる場合には試料中に含まれるアミノ酸などが反応します。
また、ドラーゲンドルフ試薬は選択性が低く窒素を含まないアルカロイド以外の共役ケトン・アルデヒドあるいはラクトンとも反応することが報告されています。
Habib, Abdel-Azim M. “False-positive alkaloid reactions.” Journal of Pharmaceutical Sciences 69.1 (1980): 37-43.
偽陽性を抑えるためには感度の低いドラーゲンドルフ試薬を用いたり、クロマトグラフィーで分離した後に検出するなどの工夫が必要ですね。
天然物から抽出した検体などサンプルが純粋でない場合は沈殿形成が必ずしもアルカロイドの存在を示す根拠にはならないので、アルカロイド検出では複数の検出試薬・手法を用いたほうが無難です。
ちなみにカフェインなどのキサンチン誘導体は「ムレキシド試験」という方法で検出できます。この試験法ではカフェインのほかテオフィリンやテオブロミンなどのキサンチン誘導体を検出することが可能です。
アルカロイドについてはこちらの記事を

ドラーゲンドルフ試薬の調製法
ドラーゲンドルフ試薬は試薬を混ぜるだけで簡単に作ることができます。濃度や酸の種類によって調製法が多少異なります。この調製法の違いによって検出感度は変化します)2。
今回は簡単に調整できて高感度なドラーゲンドルフ試薬の調整方法について紹介します。
ドラーゲンドルフ試薬のレシピ
- 硝酸水酸化ビスマス(III) 1 g
- 塩酸 2 mL
- ヨウ化カリウム 3 g
- 70%酢酸水溶液 45 mL
- 水 3 mL
ビスマス1g、HCl 2 mLの溶液を作り KI 3 g を 水 3 mLに溶解した溶液を加えて、70%酢酸水溶液 45 mLを加えて調整します。
硝酸水酸化ビスマス(III) 1gの代わりに水酸化ビスマス 0.9 gを使っても調製できます。
ドラーゲンドルフ試薬の保存法
ドラーゲンドルフ試薬は室温で数ヶ月間経っても使用可能です。
ドラーゲンドルフ試薬は購入可能
ドラーゲンドルフ試薬は有名な発色試薬の一つなので、自前で調整しなくても購入することができます。購入できるところは、関東化学、Sigma-Aldrichなどがあります。自分で作った方が安上がりではありますが、関東化学では\4,500でそんなに高くもないので頻繁に使わないのであれば購入してもよいですね。
2)桑山健次, 辻川健治, 宮口一, 金森達之, 岩田祐子, 井上博之, … & 角田紀子. (2005). 薄層クロマトグラフィーにおけるドラーゲンドルフ試液調製法の違いによる検出感度への影響. 日本法科学技術学会誌, 10(2), 127-133.
3) 三井利幸, and 藤村義和. “ドラーゲンドルフ試薬作製条件の検討.” 衛生化学 21.4 (1975): 183-187.
全てのTLCの記事は以下のリンクから!