目次
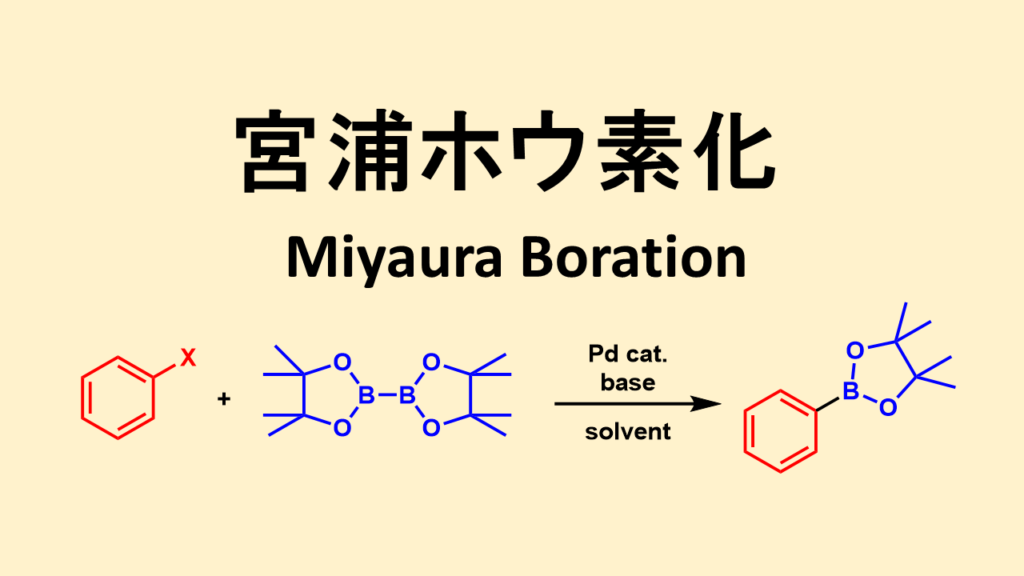
宮浦ホウ素化について
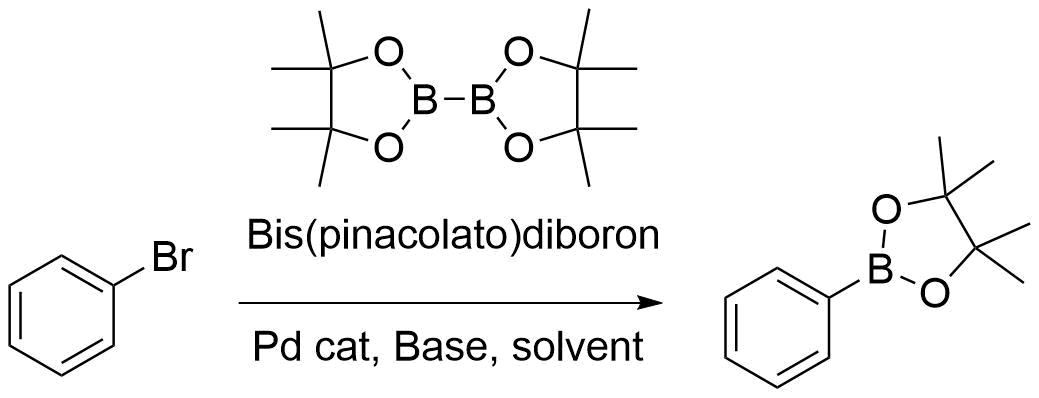
宮浦ホウ素化の概要
アリールハライドに対してビスピナコラートジボロンをパラジウム触媒下でカップリングさせる反応を宮浦ホウ素化と呼びます。
この方法では鈴木宮浦カップリング反応で有用なホウ素化合物であるボロン酸ピナコールエステル体を得ることができます。ビスピナコラートジボロンが少々高価ですが、鈴木宮浦カップリング反応の原料を調達する合成方法として非常に有用な反応です。
宮浦ホウ素化の特徴
ボロン酸の合成方法としては温和・簡便です。
アリールブロミドなどのアリールハライドは市販品があるので入手しやすいのも利点です。温和な反応であるため、ボロン酸エステルを得る方法として第一選択的に用いられます
基質としては、I, Br, OTfなどが使えます。ヨウ素と臭素が共存する場合、ヨウ素体のほうが早く反応するため選択的なホウ素化が可能です。
塩基としては酢酸カリウムが有用で、よく使います。
宮浦ホウ素化は宮浦らによって1993年に発見されました