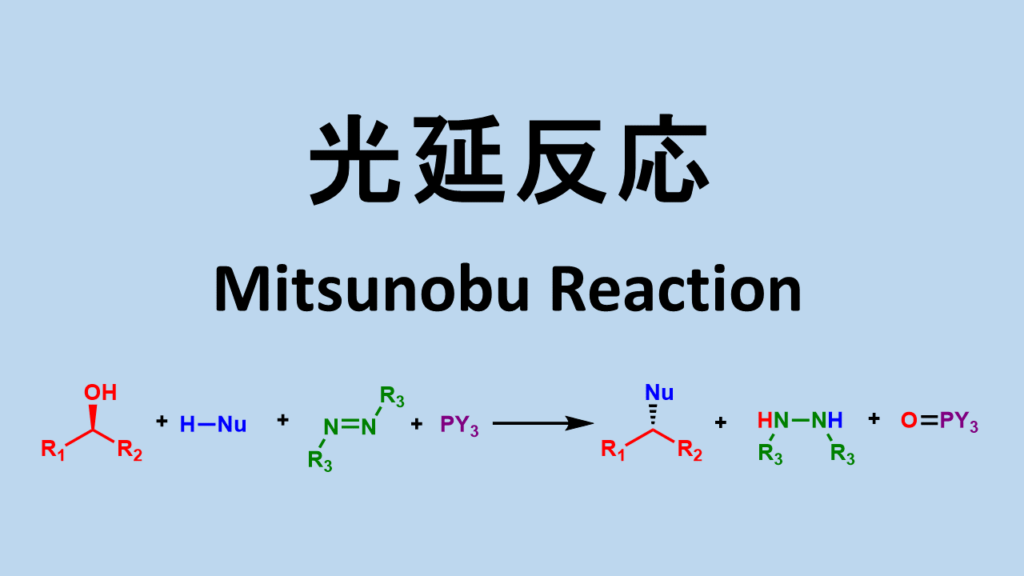
光延反応とは?
光延反応は1967年に光延らによって発見されました。エステル化をDEADとトリフェニルホスフィンにより達成した研究が始まりです。
光延反応とは、アゾジカルボン酸ジエステルおよびホスフィン存在下、第一級、第二級アルコールに対して求核剤を反応させる置換反応です。
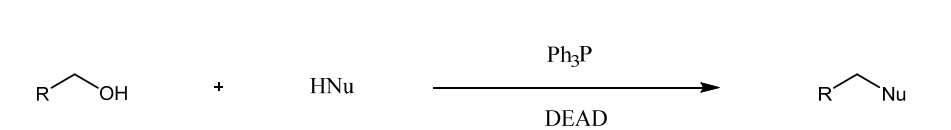
この反応は第一級、第二級アルコールが最もよい反応基質で、第二級アルコールでは立体反転を伴います。
第三級アルコールの場合は反応が進行しませんが、第三級のプロパルギルアルコールであれば進行する場合があります。
光延反応のすごいところ
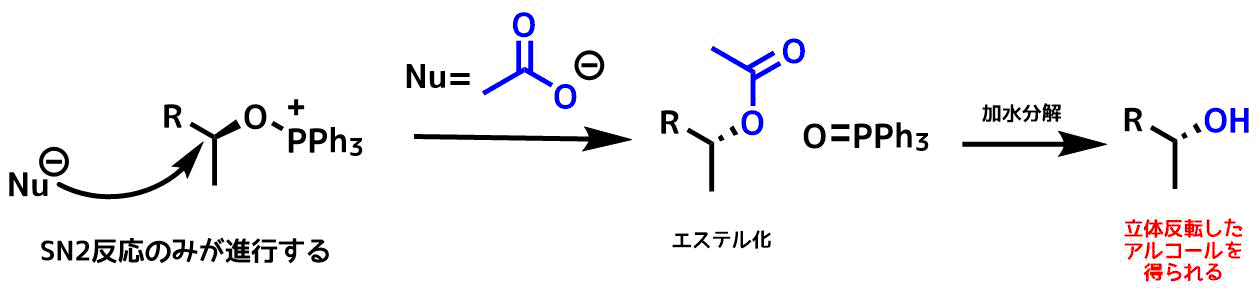
光延反応はアルコールの水酸基を脱離しやすくして、他の求核剤とSN2反応させる反応です。
SN2反応のため、光学活性の分子は立体が反転します(ワルデン反転)。
光延反応の優れている点は
- 中性条件でアルコールを活性化可能(水酸基を脱離基に変換可能)
- SN2反応が進行する
- キラルアルコールは立体が反転する
- 反応が穏やかで速い
欠点は
- 操作手順がやや煩雑
- 副生成物のトリフェニルホスフィンの除去が面倒
- 使用できる求核剤が限られる
など問題があります。
光延反応のキーポイントはトリフェニルホスフィンとアルコール及びアゾ試薬との間で生成する「アルコキシホスホニウム塩」です。
アルコールの水酸基は脱離しにくいためそのままでは求核剤と反応しません(下図)。
そこで、アルコールの脱離能を上げるためにハロゲンやスルホン酸エステルに変換します。これらは容易に求核剤と反応します。
しかし、第二級アルコールの場合、SN2反応だけでなく、SN1反応や脱離反応などが進行することがあり、純度の高い立体反転体が得られないことがしばしばあります。
光延反応はSN2反応が優先して進行するので立体反転体を高純度で得られます。これが光延反応の最大の利点です。
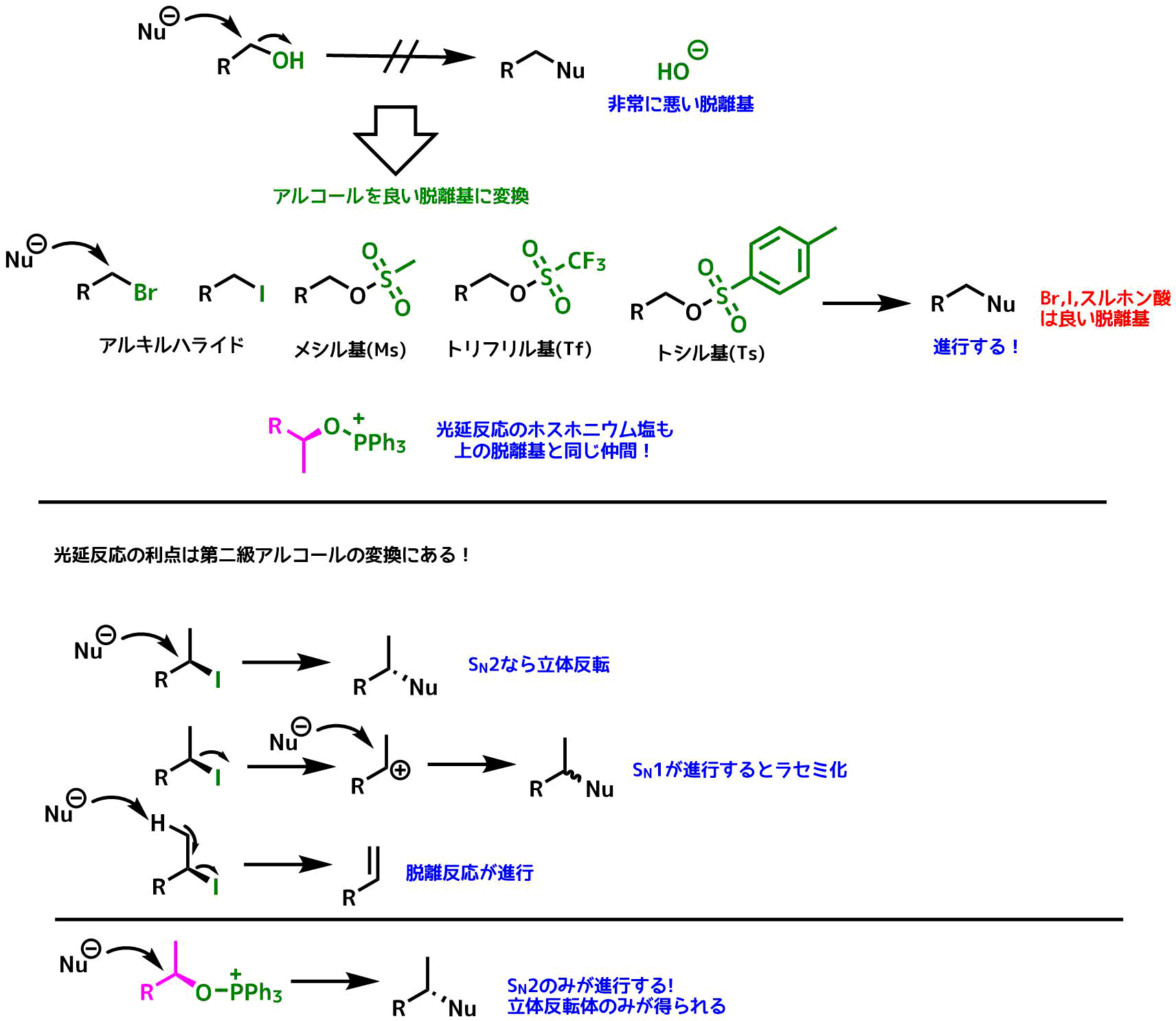
光延反応で水酸基を活性化
利用できる求核剤の種類や特徴
光延反応では使用できる求核剤が限られています。
これは求核剤の水素をDEADが引き抜いて活性種のアニオンを生成するのですが、DEADはあまり強い塩基ではないため、ある程度酸性度の高い水素しか引き抜けません(DEADのベタインはpKa13なのでpKa11以下:反応機構の第二段階を参照)。
単純なアルコールは水素を引き抜くのに強い塩基性がを使ってエーテルを合成するというのは光延反応では難しいということです(MeOHはpKa15.5)
求核剤に関しては比較的強い酸性プロトンを持つ化合物が必要です(pKa11~15以下)。
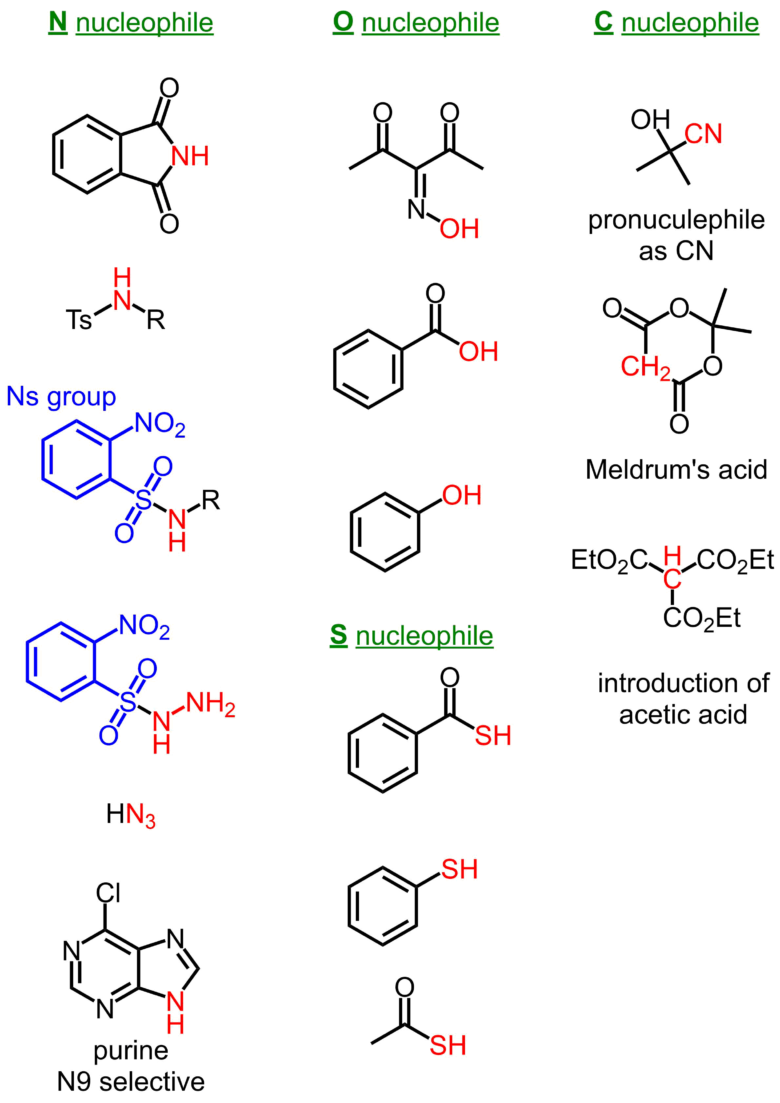
使用できる求核剤と得られる生成物は
- チオール・チオフェノール→チオエーテル
- カルボン酸→エステル
- フェノール→エーテル
- イミド
- ヒドロキサム酸
- 環状ヘテロ化合物(フタルイミド等)
- アジ化水素
- 活性メチレン化合物(メルドラム酸等)
DEAD/PPh3とともにハロゲン化物イオン源(例: ハロゲン化アルキル、ハロゲン化アシル、ハロゲン化亜鉛)を用いるとアルコールから対応する第一級、第二級ハロゲン化アルキルが得られます。
反応条件
最も標準的な条件は、DEAD/トリフェニルホスフィンをTHF中で行う条件です。
多くの場合はこの条件で事足ります。アゾ試薬・ホスフィンを変えるときは主に酸性度の低い求核剤を使用する時に変えます。
反応は通常0℃から25℃で進行し、特に立体的に混んている基質ではより高い温度が必要です。
反応時間は比較的早く、短時間(~3h)で反応進行が終わって長時間反応かけても反応が進行しないような印象があります。
溶媒
反応は主にTHF中で行いますが、ジオキサンやDCMも使うことができます。
ホスフィン
ホスフィンとしてPPh3やP(n-Bu)3が最もよく使われます。
アゾ試薬
アゾジカルボン酸エステルとしてDEAD、DIADが最もよく用いられ、どちらを用いても良いです。
実験操作
一般的な手順はホスフィン、アルコール、求核剤を溶解させ、アゾジカルボン酸エステルの溶液を滴下します。
または、まずアゾジカルボン酸エステルとホスフィンとを反応させて、アルコールと求核剤の溶液を滴下します。
光延反応を成功させる鍵は少しずつ反応を行うことです。そのためゆっくりと滴下させましょう。
アゾ試薬を滴下させる方法もあります。光延反応は反応が早い印象があります。滴下させ終わって30-1h位で反応が終了して、長く反応させても変化がないような気がします。
重要な改良法として向山らが開発した2,6-ジメチル-1,4-ベンゾキノンを用いた反応系内で調整されたアルコキシジフェニルホスフィンを経由する光学活性な第三級アルコールからの立体反転を伴ったカルボン酸第三級アルキルエステルの合成法があります。
反応機構
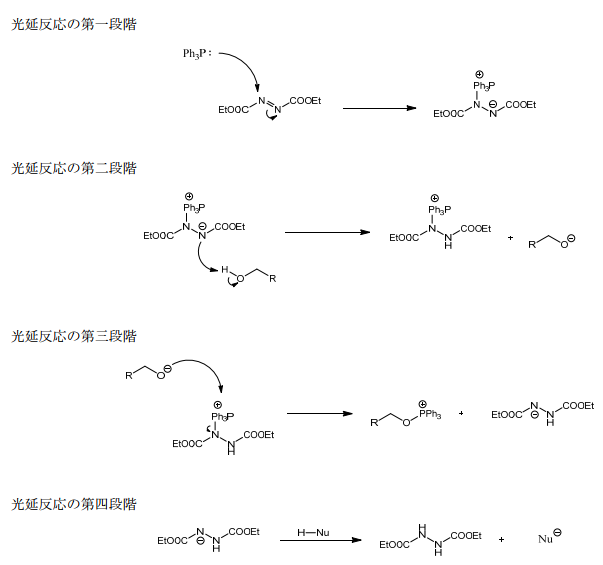
・第一段階
光延反応ではまず、トリフェニルホスフィンがアゾ試薬の求電子的窒素に攻撃してベタインが生成する。
・第二段階
生じた窒素アニオンがアルコールのプロトンを奪いアルコキシドが生成する。
・第三段階
アルコキシドがリンに攻撃してホスホニウム塩と窒素アニオンが生じる。
・第四段階
アゾ試薬の窒素アニオンが求核剤の水素を引き抜く
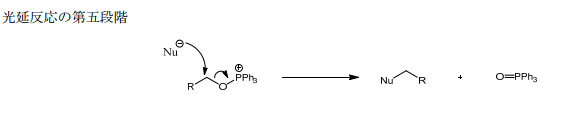
・第五段階
活性化された求核剤がアルコールを攻撃してトリフェニルホスフィンオキシドの生成と立体反転を伴った置換生成物が得られる。