血液に反応して蛍光を発するルミノール液ってなぜ光るのか疑問に思ったことはありませんか?血液を落として掃除してもルミノールで光ってしまうから、証拠隠滅できないなどといわれています。刑事ドラマでも度々登場するルミノールですが、今回はそのルミノールがなぜ光るのかを科学的に紹介していこうと思います。
ルミノールを使ったの犯罪捜査はドイツで始まる
化学の世界には「ものを光らせる」ことを研究している人がたくさんいます。例えばある物質と接触したときにだけ光るような物質を作れば、それがどこに、どのくらいあるのかを光の強さで把握できます。そんな仕掛けを利用したのがルミノールです。
ルミノールを血痕にふりかけると、見えなかったはずの血痕が青白く浮かびあがるという光景は映画などで警察が犯罪捜査で使っているイメージがあると思います。
このルミノールは「ドイツ」生まれです。
1930年代のドイツで血痕予備捜査用として開発されました。その当時、画期的だった血痕捜査方法は、その高い実用が認められて、世界にあっという間に広がりました。、実際に現在の日本においても、殺人、傷害事件において、目視不可能な血痕を探し出す方法として使われています。
ルミノールって何?なぜ光るのか?
ルミノールというのは化学物質です。化学物質の名前は(3-アミノフタル酸ヒドラジド)です。これをアルカリ性水溶液(炭酸ナトリウム水溶液)に溶かしたものに過酸化水素を加えたものをルミノール溶液として血痕にふりかけると、血液中に含まれている鉄分(ヘム鉄)がルミノールを光らせる反応を加速させるため光らせることができるといわけです。
実はルミノールによる光は、血液以外の漂白剤や金属イオンにも反応してしまうために、100%血痕のみによって光るわけではありません。さらに信頼度を上げるにはDNA鑑定や血液型診断などを合わせて行います。
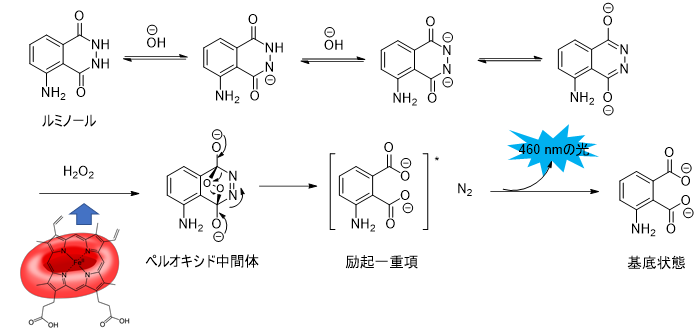
上の図はルミノールの反応機構です。ルミノールは塩基によって脱プロトン化されてジアニオンが生成します。このジアニオンに過酸化水素と血液中に含まれるヘム鉄が入ると反応が加速されペルオキシド中間体を経て窒素の脱離とともに励起状態(活性化したエネルギーが高い状態)の3-アミノフタラートが生成し、これがエネルギーを光として放出して基底状態(安定した元の状態)に戻ります。
ルミノールのような発光現象を化学発光とよんでいます。
ルミノールは血液中の鉄があると壊れやすくなります。ルミノールが壊れたときに出てくるエネルギーを利用して青い光が放出されます。
ルミノールを使わない血痕捜査方法
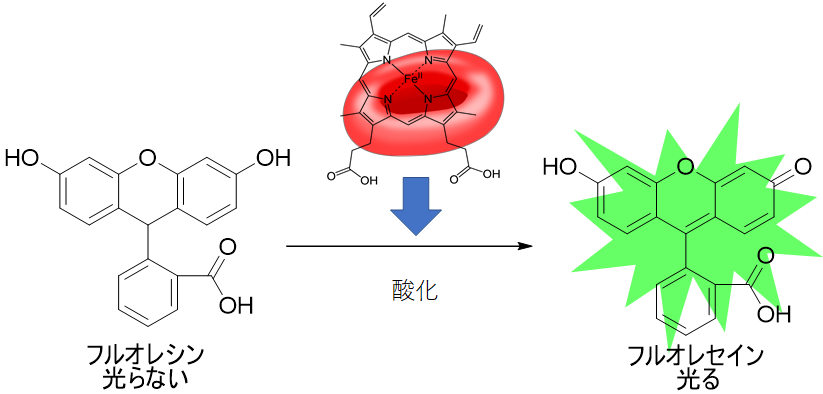
ルミノールを使わない方法も使われています。それはフルオレセインという蛍光物質を使った方法です。
方法はフルオレセインが還元された無色のフルオレシンを血液中のヘムタンパク質と鉄イオンによりフルオレセインに酸化させる方法です。酸化されたフルオレセインは蛍光物質であるため、485nmの光を勝者することによって黄緑色の蛍光がでます。この蛍光は化学発光とは違ってフルオレセインがあれば光を当てれば蛍光を何度でもみることができるので便利です。この方法はアメリカでは一般的に用いられています。
ルミノールによる犯罪捜査を妨害できるか?
ルミノールによる血痕捜査は血痕を拭いて取り除いても欺くことはできません。もしかしたらある種の漂白剤や鉄などの金属によって妨害できるかもしれません。しかし、犯罪捜査に使われている科学は何もルミノールだけではありません。むしろ変な妨害をすることによって現場の不自然さがまして、怪しまれてしまうかもしれません。
一番良いことは犯罪を犯さないことですね!
ルミノールを使った血痕捜査の動画です。英語ですがわからなくても大丈夫です。
ルミノールの作り方はこちら