カラムクロマトグラフィーのやり方を確認したい場合は「カラムのやり方!シリカゲルの量、詰め方、注意点」を参照してください。
カラムクロマトグラフィーとは?どんな種類があるの?
カラムクロマトグラフィーはクロマトグラフィーの一種で薄層クロマトグラフィーやペーパークロマトグラフィーの仲間です。
クロマトグラフィーは固定相(シリカゲルなどの固体)と移動相(固定相の間を流れる気体や液体)との間におかれた化学物質の化学的、物理的性質の違いによって、目的物の分離を行う手法です。
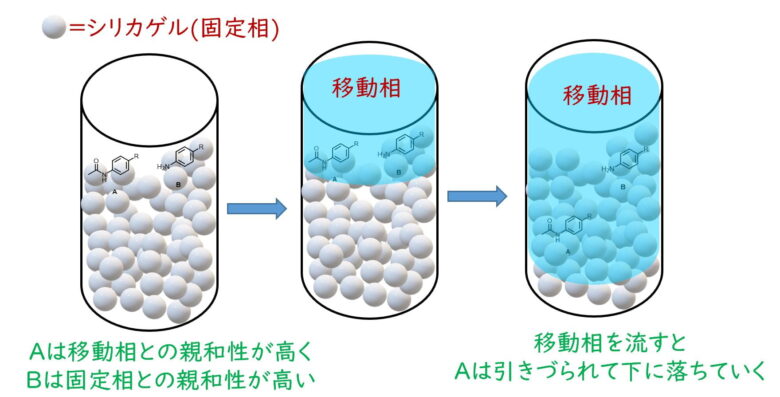
カラムクロマトグラフィーの特徴
固定相はシリカゲルが最もよく利用されます。
他のクロマトグラフィーと比べて有利な点は、数ミリから数グラム以上の量の化合物を処理することができることです。そのため、mg ~ g単位の「精製」に使えます。
カラムクロマトグラフィーの流れは
- 筒状のガラス管に充填剤(シリカゲルやアルミナ等)を詰めて、
- 少量の溶媒に溶かした混合物試料を上から流した後(チャージするともいう)、
- 移動相となる展開溶媒を流して分離します。
下図は実際にシリカゲルカラムクロマトグラフィーを実施した様子の写真です。
“Coloured column chromatography” by Максим Фомич is licensed under CC BY 2.0
ここではわかりやすいように色素を分離しています。
無色透明な化合物の場合は目に見えないので、TLCを一定の間隔でとって化合物の存在を確認します。
カラムクロマトグラフィーの原理、充填剤の種類
シリカゲルカラムクロマトグラフィーは固定相であるシリカゲルと移動相である有機溶媒に対する化合物の吸着力の違いを利用して混合物を分離します。
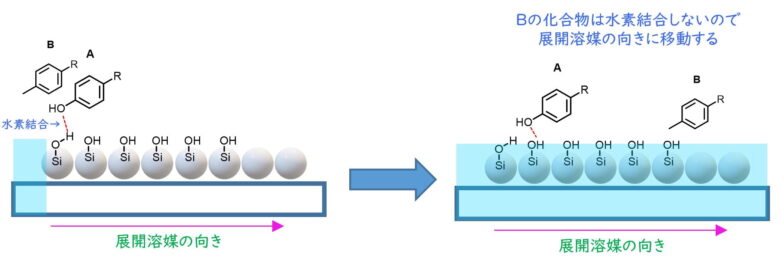
シリカゲル表面のシラノール基(~Si-OH)が化合物の極性基を引き付けます。
化合物Aの水酸基(-OH)は水素結合するため、固定相に強く吸着します。OH基などの極性基が無い化合物Bは固定相に吸着しにくいため、化合物Aよりも早く展開溶媒に流されて移動します。
充填剤の種類
充填剤(固定相)としてはシリカゲルが最もよく利用されます。次いでアルミナが使われます。
充填剤の表面官能基と化合物との相互作用によるもので「分配クロマトグラフィー」と呼ばれます。
イオン交換を利用したクロマトグラフィーは「イオン交換クロマトグラフィー」と呼ばれ、充填剤はイオン交換樹脂が使われます。
分子量や分子サイズを利用したクロマトグラフィーは「サイズ排除クロマトグラフィー」と呼ばれます。充填剤は細孔を持つものを用います。大きいサイズの分子は細孔に入り込まないので容易に通過しますが、小さい分子は細孔に入り込むので、通過が遅くなります。結果的に、大きい分子は早く展開され、小さい分子は遅く展開されます。GPC(ゲル浸透クロマトグラフィー)やゲルろ過クロマトグラフィーがあります。
シリカゲルのサイズと修飾による違い
シリカゲル粒子径によって分離能は変化します。
一般的に粒子径が細ければ細かいほど分離能が向上しますが、展開溶媒が通過しにくくなるので展開スピードが遅くなり、しばしば上から高い圧力で押す必要があります。これを「フラッシュシリカゲルクロマトグラフィー」と呼びます。
粒子径がそこまで細かくなければ、重力で十分に展開できます。これを「オープンシリカゲルクロマトグラフィー」と呼びます。
修飾シリカゲル
シリカゲルには表面がカルボキシル基やアミノ基で修飾されているものがあります。このような修飾シリカゲルは通常のシリカゲルとは性質がことなります。種類としては、
- ODS(オクタデシル基)修飾シリカゲル→逆相シリカゲルとも
- カルボキシル基修飾
- アミノ基修飾
- ジオール修飾
があります。
 化学修飾シリカゲルの種類と選び方(アミノ、ジオール、カルボン酸)
化学修飾シリカゲルの種類と選び方(アミノ、ジオール、カルボン酸)カラムのやり方!シリカゲルの量、詰め方、注意点
カラム管の下図のような形で作ります。
カラム管のサイズはオープンシリカゲルカラムクロマトグラフィーの場合、計算したシリカゲル量をカラム管に加えた時に高さが15-20cmくらいになるような半径のカラム管を使います。
使用するシリカゲルの量は精製したい混合物の重さの20倍~50倍程度の量をつかいます(アルミナの場合は50~70倍)シリカゲルの量はRf値の距離や極性、スケールによって変化しますので目安です。高さのほうが重要かもしれません。
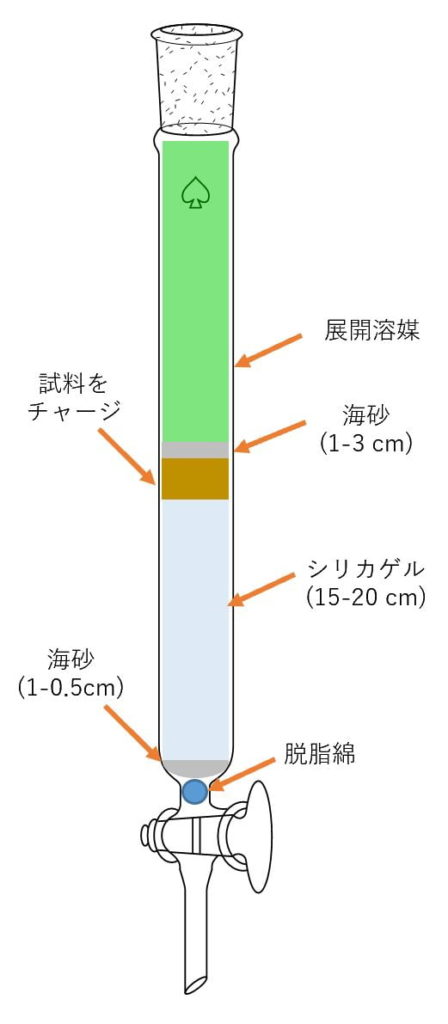
カラムサイズとシリカゲルの量が決まったら、カラム管を作成していきます。大きく解説すると、
- 脱脂綿を下に詰める
- 海沙を脱脂綿が隠れて平らになるくらいまで入れる
- シリカゲルを湿式法(or乾式法)で加える。
- 少量の展開溶媒等に溶かした試料をゆっくりと乗せて、浸透させる
- 海沙を表面にゆっくりとのせる
- 展開溶媒を加えて展開させる。
というのが概略です。各操作のポイントを説明すると
1.脱脂綿は上の海砂やシリカゲルがもれないように隙間ないようにつめますが、きつく詰めすぎると流れが悪くなるので程々にする。長い竹串やガラス棒などで詰める。
2.海砂を加えて下部表面を水平にする。海砂を加えない人もいる。
3.シリカゲルを加える手法は湿式(展開溶媒に懸濁させたシリカを加える)と乾式(シリカゲルを加えた後に展開溶媒を流す)方法があるが、湿式のほうがキレイに詰められるのでおすすめです。湿式の場合はカラムサイズの1/4程度まで展開溶媒を加えてから実施する。展開溶媒の検討については下の記事に書きました。

4.充填したシリカゲルの上表面をほんの少し乾かして固めた後に少量の展開溶媒に溶かした粗生成物をパスツールピペットを使ってカラム内壁を伝わすようにしてゆっくりと加えていきます。勢いよく加えるとシリカゲル表面がボコボコになってキレイに展開できなくなります(重要ポイント!)。粗試料が入っていた空容器に展開溶媒を少量加えて洗った液を再度チャージする(洗い込み)これをもう一度繰り返す。
試料によっては展開溶媒に全く溶けないものもあるので、その場合はもう少し極性を上げるか、トルエンやエーテルなど極性が低めで溶解力の高い溶媒に溶かしてからチャージする。それでもだめな場合は、展開溶媒を溶けやすい溶媒組成のものに変更するか(トルエン系とかハロゲン系など)、まぶしカラムをする(後述)
5.粗生成物をシリカゲルに吸着させた後、海砂を上1-3cmゆっくりとのせます。この海砂はシリカゲル表面をえぐらないようにするためにいれるもので、あまり少ないと意味が無いと思います。海砂を入れなくてもできますが、変に気を使うので時間がかかるのでのせるのをおすすめします。
6.展開溶媒を加えます。この時シリカ表面をえぐらないようにそっと加えます。えぐってしまうとキレイに展開できなくなります。
シリカゲルの詰め方、湿式法と乾式法の違いは?
湿式法のほうがより密に詰めることができるので分離能が高いと言われています。乾式法はシリカを懸濁させたりする手間がないので楽なのがメリットです。個人的には乾式が楽で結構イケると思ってますが、湿式のほうがキレイに詰められるので湿式を使うほうが無難です。(乾式なんて手抜きと怒られるかもしれません)
乾式のシリカゲルの詰め方
2.の操作の後、カラム管をゴムハンマーや木槌などで軽く叩きながらシリカゲルを少量ずつ加えていきます(あまり叩くと海砂が乱れて下のコックからもれるので注意する)。シリカゲルを加え終わったら強めにゴムハンマーで叩いて詰めてから、展開溶媒を加えて、上から圧力をかけて気泡を逃がすようにして展開溶媒を下から流してできあがり。展開溶媒は1CV(カラムボリューム)程度は流したほうがよい。
湿式のシリカゲルの詰め方
2.の操作の後、展開溶媒をカラム長の1/4程度加えておきます。量り取ったシリカゲルに2倍量程度の展開溶媒を加えて、ガラス棒や超音波洗浄機にかけてよく撹拌して気泡を取り除く。懸濁させたシリカゲルをカラムに注ぎ入れた後、下から展開溶媒を流してシリカゲルを沈降させる。湿式でもゴムハンマーで叩くと密につまる。
失敗しないための注意点!気をつけるポイント等
すぐに化合物が出てきてしまう
粗生成物を溶かす溶媒の極性が展開溶媒の極性よりも高い場合に起こることがあります。ジクロロメタン/メタノール系の展開溶媒のとき、メタノールにしか試料が溶けないときなど、極性の高い溶媒にしか溶けないときは通称「まぶしからむ」をしましょう。まぶしのときは溶ける溶媒(THFとかアルコールでも良い)に試料を溶かしたら、試料の10倍量程度のシリカゲルあるいはセライト(吸着しにくいのでおすすめ)を加えて懸濁させたあと、エバポ、真空乾燥させます。できた粗生成物が吸着された粉末(これをまぶしという?)を4.の操作の後加えて、展開溶媒を流し入れて空気を抜いたあと、海砂をのせてカラムを行います。アルコールなど沸点が高い溶媒でまぶしを作るときはきちんと乾燥させましょう。シリカ表面がぶくぶくしているうちはまだだめです。こうすることで、高極性溶媒に引っ張られてしまうことを防げます。
分離できない、すぐに出てきてしまう!
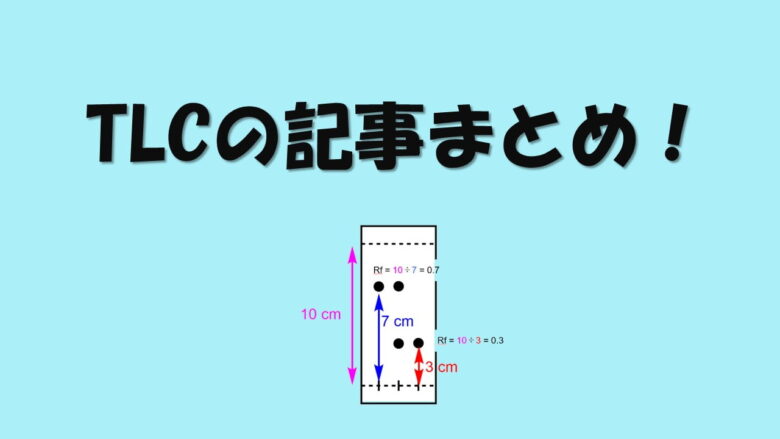
展開溶媒の設定を見直しましょう。オープンシリカゲルクロマトグラフィーの場合はRf値は0.2-0.4くらいの間に設定します。0.3くらいが良いと言われています。Rf値が高すぎるとすぐに出てきてしまうので注意です。フラッシュシリカゲルクロマトグラフィーの場合もRf値は0.2-0.3くらいです。
分離できない、すぐに出てきてしまう2
DMSOやDMFなどの高沸点溶媒を反応に使用している場合はそれらが残っていると引きづられてすぐに出てきてしまいます。きちんと減圧乾燥して取り除いてから分離しましょう。
出てくるのが遅くてやたら時間がかかる。
オープンシリカゲルクロマトグラフィー時間にして30-60分ほどで展開が終わります。3時間を超えるような時間カラムをやっている場合は、展開溶媒の選択が悪いか(Rf値が低すぎる、別の展開溶媒を試して良い条件を探す)、展開スピードが遅すぎるということです。途切れて液滴のように出てくるような状態では遅すぎます展開スピードが遅すぎる場合は上から圧力をかけましょう。手押しの空気入れやゴム二連球、電動金魚ポンプなどを使って上から圧力をかけましょう。
カラムは細い径でシリカを長く詰めるのと、太くて短いのはどっちが良い?
同じシリカゲル量の時、細い径では長く、太い径では短くなりますが、どちらに合わせるべきでしょうか?基本はシリカゲルの積む量は15-20cmくらいになるようにします。長さが短いほうが早く展開されますRf値が遠くて分けやすいものであれば短いほうが時短になります。逆にRf値が近くて分けにくい場合は長くする法がよいです。
太いカラムをあえて使う場合は、
- サンプルの粘性あるいは結晶性が高くて詰まりやすい場合
- シリカゲル等で反応してしまうような化合物の場合
- 粗生成物の溶解性が悪くてチャージする溶媒量が多くなってしまう場合
などがあります。粘性が高いとか結晶性が高い場合はカラムが詰まってでてこなくなることがあるので、太めのカラムを使います。また、シリカゲルと反応してしまうような化合物の場合は手早くやるために太く短めにする場合があります。また、粗生成物の溶解性が悪いとチャージする溶媒量が多くなりがちです。チャージするときの厚さは短いほうが分離が良いため太めを選択することがあります(まぶしをやったほうが良い場合も多い)
分離が難しいカラムは粒子径を細かくしてフラッシュでやったほうが良いです。いずれにしても、分離が難しいものはカラムを長くして保持時間を長くすることで分離しやすくなります。
フラクションには見えなかった化合物が濃縮後に見える
カラムのフラクションをTLCで確認したときは見えなかったのに濃縮後に現れるというときはしばしばあります。薄くて見えていない時やカラム後に分解している場合もあります。大抵は前者です。これを防ぐためには絡む前のサンプルのTLCをとっておき、予想目的物周辺のスポットの状況をよく確認しておく。薄いスポットが近くにあれば、フラクションのTLCを観るときは、濃いめにスポットを打っておく工夫が必要です。また、フラクションを区切って回収する方法もあります(前半、中盤、後半)などのように分ける。
参考サイト、動画、書籍
全てのTLCの記事は以下のリンクから!




お忙しいところ失礼いたします。
現在、植物由来の物質を分離・精製するという実験を行っています。その一環で、近々オープンカラムクロマトグラフィーの実験をするのですが、分からない点がありご連絡させていただきました。
粗生成物を展開溶媒により溶出させた後のシリカゲルは再利用が可能なのでしょうか。
私は酢酸エチルとヘキサンの混合溶媒を展開溶媒として用いる予定なのですが、例えば展開溶媒で粗生成物を全て溶出させた後に極性の高いメタノールを流してシリカゲルを洗浄、再び使用することはできないのでしょうか。
それとも、やはりシリカゲルは使い捨てる方が無難なのでしょうか。
もう一つ質問させてください。
分取TLCという実験手法がありますが、これとカラムクロマトグラフィーはどう使い分ければよいのでしょうか。
一般的なTLCは何度も行っているので、目的物質を得るためなら分取TLCの方が容易に思えます。ただ、なるべく多くの目的物質を得たいので、何度も実験をするのならランニングコスト的にカラムクロマトグラフィーを用いた方が良いように思えます。
素人質問で恐縮ではありますが、ご教授いただけましたら幸いです。
よろしくお願いいたします。
ご覧いただきありがとうございます。
一つ目の質問の「シリカゲルの再利用」は可能です。
再利用する場合はカラム上部の高極性の色素沈着したシリカゲル部分はメタノール洗浄でも落ちにくく、全体を汚染する可能性があるため、除去してから再利用することをおすすめします。メタノールや場合によっては水洗後には十分に乾燥させるか低極性溶媒で置換しないと使えないと思います。
経験上はシリカゲルは主にコストと分離能の問題から再利用はほとんどしません。
– 時間と溶媒コストがかかる。
– 論文記載の目的で精密な実験、収率計算を要する場合は実験系外の化合物混入があるため使えない
– 精製の再現性が落ちる
– 分離能が低下する
酢酸エチルのみ程度できれいになる事が予めTLCでわかる場合は使う事があります。正解はありませんので目的と照らし合わせて、可能ならテストをしてみてお考えいただければと思います。
二つ目の「分取TLCとカラムクロマトグラフィーの使い分け」については私的な経験上の判断になりますが
・カラムクロマトグラフィー
主に大容量で(数百mg以上)一般的な精製目的
・分取TLC
・小容量で機械的な高性能分離装置が利用できない、あるいは適さない場合
というように使い分けています。
分取TLCは分離を目視しやすい・並列化できるなど優秀な面も多く一見、理想的ですが、実際に優秀な面も多いのですが、積極的におすすめ、利用しないのは
– コストが高い
– 時間がかかる(という場合に使用することが多い)
– 大スケールに向かない(大量の枚数が必要)
– 高収率・高分離を得るにはスキルを要する
などの理由があるからです。
まとめますと
カラムクロマトグラフィーで使える・十分目的を達成できる場合 → カラムクロマトグラフィーを使用する(工業生産を目指さない大学の研究や化学実験の場合)
他に適する分離方法が使えない、見当たらない、分取TLCを使いたい場合 → 分取TLCを使用する
という感じになります。
ご教授いただき誠にありがとうございます。
オープンカラムクロマトグラフィーを本格的にやるのは初めてなので、不安を払拭させることができました。
恐縮ではありますがもう一点質問させてください。
粗生成物(クルード)を溶媒に溶かす際、何グラムに対して何ミリリットル程度の溶媒に溶かせばよいのでしょうか(何%くらいになれば良いのか)。
あまりに濃いと分離が悪くなるのでしょうか。
ご教授いただければ幸いです。
よろしくお願いいたします。