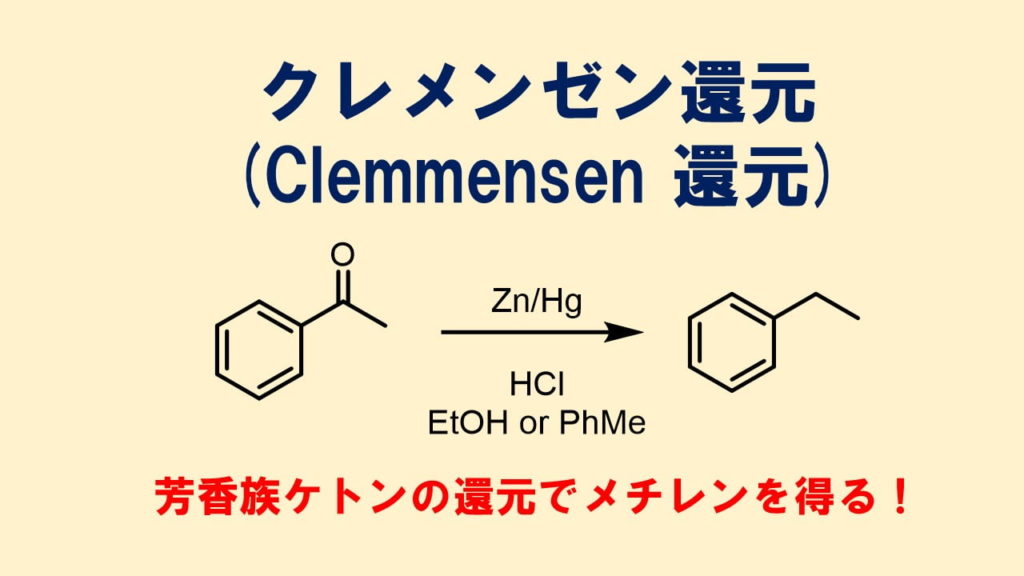
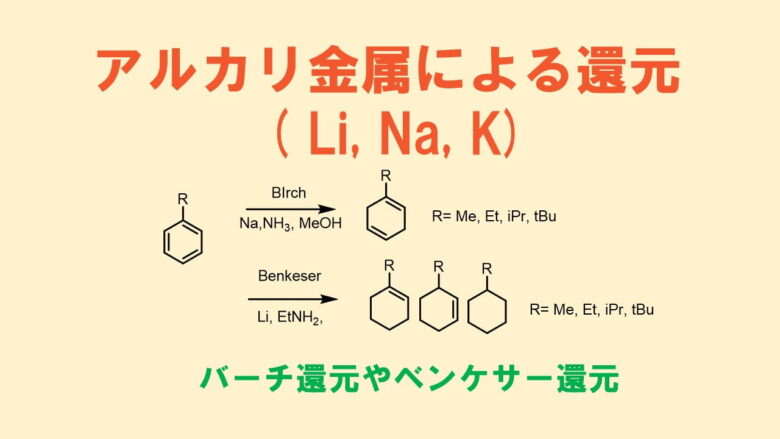
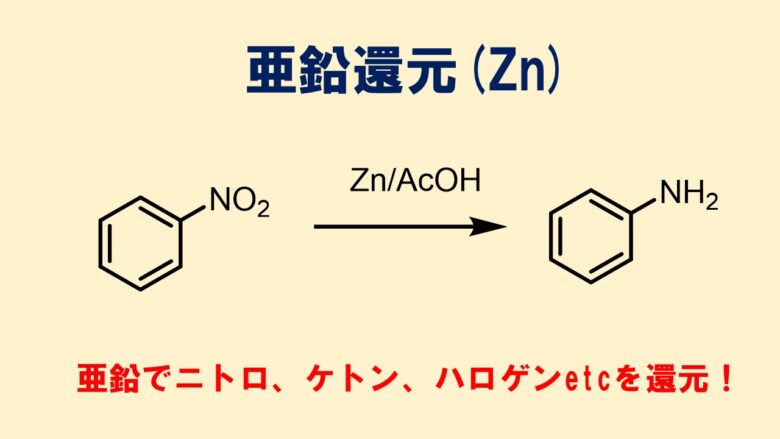
クレメンゼン還元は古典的なケトンの還元方法として有名です。クレメンゼン還元では亜鉛と水銀のアマルガム(合金)を使って還元します。水銀を使うので使う機会は少ないかもしれませんが有名な反応なので概略を押さえておきましょう!
クレメンゼン還元とは?ケトンをメチレンに変換
クレメンゼン還元は亜鉛アマルガムを使った還元反応で、ケトンやアルデヒドをメチレンに変換する反応です。特に芳香族ケトンに対する還元が代表的?のようです。
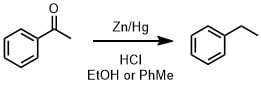
亜鉛アマルガムは亜鉛と塩化水銀水溶液から調製できます。(亜鉛1gに対して5%塩化水銀水溶液(2 mL)を振り混ぜながら加えて1時間後上澄みを除去したら完成です。)亜鉛アマルガムの量は過剰に使います。原料の重さに対して2-10倍量の亜鉛を使います。
塩酸/加熱還流のため酸に弱い基質は使用できません。
反応は塩酸に溶けるエタノールやTHFなどの溶媒を使って一層でやる方法が古典的ですが、しばしば飴状の生成物が金属を覆って反応進行が妨げられるのでトルエンなどを加えた二相系で反応を行うのがおすすめです。原料の溶解性が悪いときもよくあるので、水層に溶けなければ、酢酸やエタノールを加えて溶解度をあげてやると反応が進行しやすいです。
反応後の亜鉛アマルガムはラネーニッケルと同様にろ過除去したときに乾燥させると発火することがあるので表面を濡らして置く必要があります。
クレメンゼン還元の反応条件
一般的な条件
亜鉛アマルガムと塩酸、二相系ならトルエンやエーテルなどを加え、原料を加えます(水溶性が悪ければアルコールや酢酸に溶かす)。混合物を加熱還流し、反応時間が長い場合適宜濃塩酸を追加する。ろ過後(発火に注意)、濃縮後(アルコール分が多い場合)、中和、抽出により還元体を得ます。
改良法
塩酸での加熱還流は多くの官能基を損なう可能性があるので避けたいです。塩酸あるいは無水酢酸を含むジエチルエーテル中で反応させる方法では0℃、短時間(数時間)で進行させることができるので、酸に弱い官能基の還元に適しています(ニトリル、アリールエーテル、エステル等)。
クレメンゼン還元の反応機構
クレメンゼン還元の反応機構についてはまだ不明のようです。提唱されている反応機構としては、
プロトン化したケトンが亜鉛によって一電子還元を受けた後、有機亜鉛中間体を生じます。その後、脱水、亜鉛による還元を受けて生じたアニオンがプロトン化し、亜鉛とプロトンが交換してメチレンが生成する機構です。