がんの治療法としては大きく分けて手術、薬剤療法、放射線治療法が知られています。今回はその中でも放射線治療法の一種として新たに注目されているホウ素中性子捕捉療法について説明します。
ホウ素中性子捕捉療法(BNCT)とは
ホウ素中性子捕捉療法: Boron Neutron Capture Therapy (BNCT)は、がんの新たな治療法として注目を集めている中性子捕捉療法の中でも、特に中性子増感元素としてホウ素を利用した治療法のことです。
中性子捕捉療法(NCT)とは
中性子捕捉療法: Neutron Capture Therapy (NCT)とは、原子炉などからの中性子と癌組織に取り込まれた中性子との反応断面積が大きい元素との核反応によって発生する粒子放射線によって、選択的に癌細胞を殺すという原理に基づく癌治療法(放射線療法)です。この治療法に用いられる中性子増感元素としてはホウ素(10B)、ガドリニウム(157Gd)等が考えられています。
なぜがん細胞だけを殺傷できるのか?
中性子捕捉療法では10B(質量数10のホウ素:天然存在比は約20%)と熱中性子との間で起こる核反応で生じるエネルギーを利用してがん細胞を殺傷します。核反応というと恐ろしく感じるかもしれませんが、この方法で生じるα線は5~14マイクロメートルまでしか到達しません。この範囲はちょうど細胞一つの直径と同じくらいであるため、がん細胞だけにホウ素を取り込ませることができれば、取り込んだガン細胞のみを破壊できます。逆にいえば、中性子捕捉療法で重要なのはいかにホウ素化合物(ホウ素薬剤)をがん細胞だけに取り込ませることができるか?ということになります。このようにある細胞だけに薬物を届ける仕組みをドラッグデリバリーシステム(DDS)といいます。
[chat face=”kome” name=”” align=”left” border=”gray” bg=”none” style=””]ここに文字を入力してください[/chat]核反応を引き起こすような熱中性子を身体に放射するのは危険なのでは?
熱中性子はがん治療に利用される従来の化学療法や放射線療法と比べて正常な細胞への損傷は少ない点が注目されています。
ホウ素中性子捕捉療法に利用されるホウ素薬剤
最近話題になってきているので、ホウ素中性子捕捉療法(BNCT)は新しく登場したものかと思われるかもしれませんが、実はKrugerらによって1940年に初めてBNCTを使った抗がん効果が確かめられています。
[chat face=”komeyaniro.png” name=”” align=”left” border=”gray” bg=”none” style=””]意外と昔からBNCTは存在していたんですね![/chat]
その後脳腫瘍患者などにもBNCTが効果があることが確かめられています。
しかし、BNCTは熱中性子源として原子炉が必要であることから、研究できる場所が限られる点と抗がん効果が期待よりも低かったことから研究があまり進みませんでした。
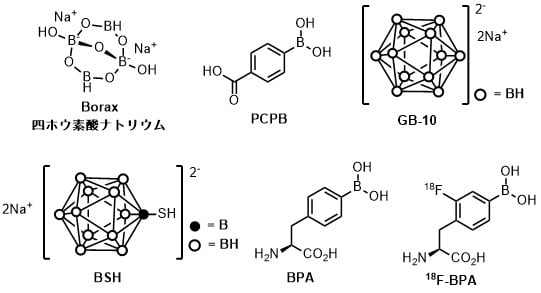
その後の研究で開発されたBSH、BPA等は日本で積極的に臨床研究が行われ、高い治療効果があることが報告されています(5年生存率60%以上)。
フッ素の同位体を用いた18F-BPAはフッ素のPETを用いることにより、ホウ素蓄積量を見積もることができます。BNCTは蓄積されるホウ素濃度が重要であるためこのような化合物が作られています。
BPAはフェニルアラニンの誘導体ですが、このようにアミノ酸がベースとなっているのはがん細胞への取り込みを促進させるために生体内物質の構造を模倣しています。
なぜホウ素が使われるか?
10Bは中性子補足しやすい原子であり、天然に20%も存在しているという点が利点です。さらに中性子補足しやすい元素はキセノン、ガドリニウム、サマリウムなどがありますが、入手しにくく、炭素との結合も作りにくいので分子デザインが乏しい点が欠点です。
- 天然に豊富(20%)
- 放射能を持たない
- α線の飛距離が小さい
- 炭素と結合形成が可能で分子デザインが豊富
- 毒性をもたない
などの利点が挙げられます。これらの利点を兼ね備えているためホウ素は中性子補足療法に利用されています。
より効果が高いBNCT療法のために
BNCTが普及しにくい理由として、熱中性子発生源が必要であることが挙げられます。またより高い治療効果を上げるためにはがん細胞中にホウ素化合物をミリモル濃度と高濃度のホウ素化合物を要する点です。高いホウ素濃度を達成するためにはBSHなど、ホウ素を10個含むホウ素クラスター分子を利用する手がありますが、がん細胞へ選択的に集積するのが難しいです。ホウ酸基BPAなどのホウ酸基を含む化合物はホウ素含有量は少ないですが、様々な分子に導入できるメリットがあります。
BSHのがん細胞への選択性を上げるための改良も研究されています。水溶性ポルフィリンが結合したBSHはがん細胞への集積能が向上することがわかっています。
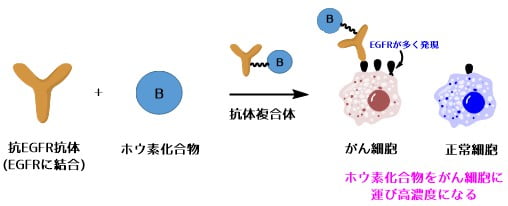
とあるターゲットに対して特異的に結合するのが得意なのは抗体です。がん細胞に選択的に結合する抗体(抗EGFR抗体:セツキシマブ)をホウ素化合物と結合させることによって、がん細胞にホウ素化合物をデリバリーするシステムが報告されています2)。
DDSでも注目を集めているリポソームを使用する戦略も検討されています。リポソームはリン脂質から形成された人工の脂質二重膜を持ったカプセルです。リポソームはEPR効果によりガン組織に留まりやすくなります。BSHに高級脂肪酸エステルを導入したリン脂質模倣化合物を合成することにより、ホウ素化合物が結合したリポソームを作ることに成功しています。
参考文献
1)中村浩之. “ホウ素化合物・薬剤の歴史と現状.” RADIOISOTOPES 64.1 (2015): 47-58.
2)Wu, Gong, et al. “Site-specific conjugation of boron-containing dendrimers to anti-EGF receptor monoclonal antibody cetuximab (IMC-C225) and its evaluation as a potential delivery agent for neutron capture therapy.” Bioconjugate chemistry 15.1 (2004): 185-194.