目次
バイヤー・ビリガー酸化
ケトンおよび環状ケトンを過酸で処理することでエステルおよびラクトン、ヒドロキシ酸に酸化する反応をバイヤー・ビリガー酸化といいます。
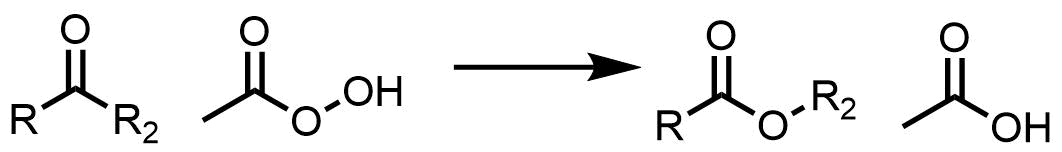
バイヤービリガー酸化
過酸を使った反応として有名です。ケトンをエステル化する反応として使われます。対象ケトンであれば選択性を気にせずにエステルに変換できますが、非対称ケトンの場合はどのアルキル基が転位しやすいのか?を考える必要があります。一般にかさ高いアルキル鎖が転位します。
バイヤー・ビリガー酸化の特徴
- 分子内に多くの官能基が存在しても問題なく、例えばα,β-不飽和カルボニルが存在していてもC=C結合ではなくカルボニル基が選択的に反応します。
- 位置選択性にかんしては、二つのアルキル基の転移のしやすさに依存していて、非環状化合物では、一般的に第一級、第三級アルキル基がビニル基が転位します。
- 非対称ケトンの場合では、転移のしやすさは第三級アルキル>第二級アルキル>アリール>第一級アルキル>メチルの順になります。
- 転位した立体中心は保持されます。
- 酵素、あるいはキラルな遷移金属触媒を用いるとラセミやキラルなケトンを不斉制御した酸化を行うことができます。
バイヤービリガー酸化は1899年にA.BaeyerとV.Villigerにより報告されました。反応中間体の名前にもなっているCriegeeによって1948年に反応機構の提唱が行われ、その機構の妥当性は1953年にDoeringとDorfmanらによる標識実験により証明されました。
反応機構
反応機構は過酸のプロトンによりカルボニル酸素がプロトン化することによってはじまります。活性化されたカルボニル基は過酸アニオンによる求核付加反応を受けます。これにより生成した過酸のgemジオールエステル(Criegee付加体)はアルコールのカルボニル化に伴い、結合が弱い過酸のO-O結合が切断され、カルボン酸が脱離するのと同時に電子不足な酸素に対してアルキル基が転位します。これによってエステルが生成します。この過程は協奏的に起こります。
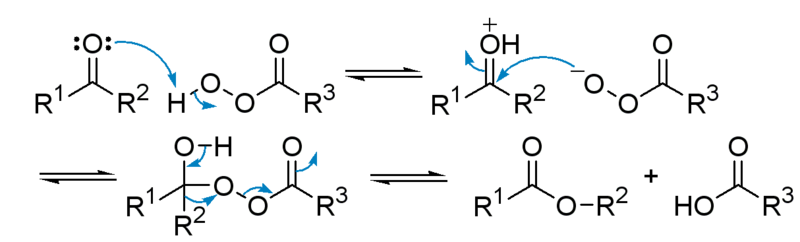
バイヤービリガー酸化の反応機構 from wikipedia public domain