炭酸カリウム (K2CO3)はカリウムの炭酸塩で、炭酸ナトリウムと同様の性質をしめす無機塩基です。炭酸ナトリウムと比べて炭酸カリウムは溶解性の高さが特徴です。工業的にも炭酸カリウムは広く利用されています。
炭酸カリウムとは?
炭酸カリウム (K2CO3)はカリウムの炭酸塩です。
炭酸カリウムの製造は、水酸化カリウムに二酸化炭素を吸着させて炭酸カリウムに変換して得ます。
2KOH + CO2 → K2CO3 + H2O
無水炭酸カリウムは吸水性が高く、溶媒の脱水剤として利用されます。
炭酸カリウムのプロパティ
- 分子量: 138.205 (無水物)
- 化学式: K2CO3
- 融点 : 891℃
- 密度 : 2.29
- 溶解度 : 水への溶解度112g /100 mL (20℃)、グリセリンにも溶解
脱水剤としての利用
無水炭酸カリウムは溶媒の脱水剤に利用されます。炭酸カリウムは、アルコール、ケトン、エステル、ニトリル、アミン類の脱水剤として利用されます。特に塩基性であるため、アミン類の脱水に利用されます。
逆に炭酸カリウムと反応するような、フェノールやカルボン酸などの酸性物質、塩化水素などの酸性ガスは利用できません。また、エステルやアミドなど加水分解するような溶媒も避けたほうが良いです。
脱水能力はそこまで高くありませんが、安価で取り扱いやすいので利用しやすいです。予備脱水に利用します。塩基性条件での脱水縮合にも向いているかもしれません。
水和した炭酸カリウムも200℃くらいに熱して脱水すれば無水物に戻すことができます。
炭酸カリウムの反応
炭酸カリウムの反応は炭酸ナトリウムと同様ですが、有機溶媒への溶解性が炭酸ナトリウムよりも高いことから、有機合成では炭酸カリウムをよく利用します。フェノール、アミンのアルキル化、エステルの加水分解、ジケトンのマイケル付加など基本的な塩基を利用した反応に広範に利用可能です。塩基性を高めたり、有機溶媒への溶解性を上げるのに、クラウンエーテル (18-crown-6)を利用します。クラウンエーテルはカチオンを環状エーテル内に捕捉し、炭酸イオンを裸にするので塩基性が高くなります。18-crown-6はカリウムイオンを捕捉するのに利用されています。
エステルの加水分解
炭酸ナトリウムと同様に炭酸カリウムもエステルの加水分解に利用されます。溶媒は対応するアルコール中で行います。炭酸カリウムは塩基に少し不安定だと予想される化合物を加水分解する場合のファーストチョイスとなります。
β-ケトエステルのアルキル化
βケトエステルとそれに対応する求電子剤との反応は炭素-炭素結合の形成反応として重要です。炭酸カリウムを利用した場合はO-アルキル化は進行しにくく、C-アルキル化が選択的に進行します(BARCO, A. S. Benetti & G. P. Pollini. Synthesis, 1973, 316: 510)
ウィッティヒ反応
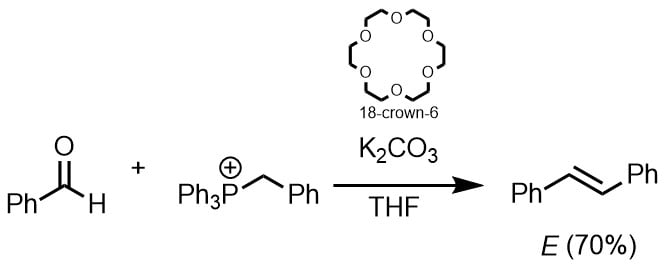
通常ウィッティヒ反応はブチルリチウムや水素化ナトリウムなどの強塩基を利用することが多いですが、炭酸カリウムでもクラウンエーテルを利用することで良好な収率で進行します。炭酸カリウムを使用した場合、E体のアルケンが選択的に得られます(Le Bigot, Y. et al, Synthetic Communications, 1982, 12.2: 107-112.)。