アルカリ金属やアルカリ土類金属はイオン化傾向が大きく電子を放出しやすいため、還元反応に利用できます。有名な還元方法としては溶媒として液体アンモニアを使用するバーチ還元があります。ここでは様々な1,2族元素を利用した還元方法をまとめます。
アルカリ金属を使った還元とは?
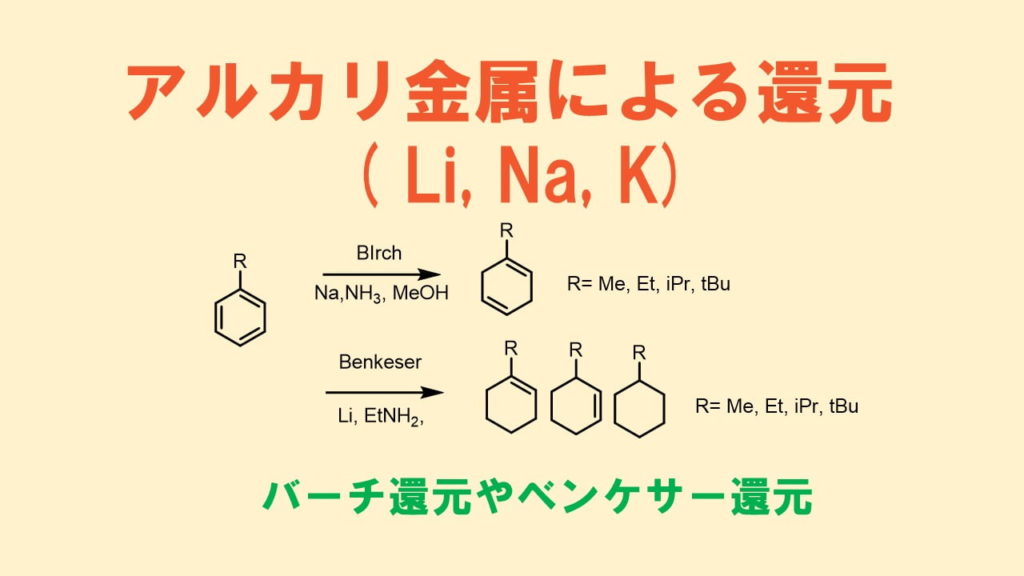
金属を使った還元方法は一般的で、様々な金属、金属塩を使った還元反応が報告されています。そのうちアルカリ金属を使った還元でもっとも有名なものはアンモニア中ナトリウムやリチウムを溶して還元させるバーチ還元だと思います。
- 液体アンモニア+Na or Li +(エタノール等): バーチ還元
- 第一級アミン(メチル、エチルアミン2)やエチレンジアミン3))+Li or Ca:Benkeser還元(ベンケサー還元)
- HMPA+t-BuOH + Na
HMPAや第一級アミンを使った方法はバーチ還元の変法です。液体アンモニアは沸点が-33℃のため温度が挙げられませんが、第一級アミンを使ったベンケサー還元は温度を室温以上に上げられる利点があります。エチレンジアミンは他のアミンよりも金属Liを溶解しやすく、さらに100℃程度まで温められる利点があります。
HMPAとtert-ブチルアルコール中ではNaの還元力が大きく上がることが報告されており、こちらも還元力の高い方法として利用されいます1)。
HMPA+tBuOH+Na法による還元の反応条件
反応はNa(2.5 eq), HMPA(1 mol/L)に溶かした後 tBuOH(2.7 eq)をゆっくり加えて数分撹拌した後、基質をHMPAに溶解させたものを滴下して加えます(青色が消えないようにゆっくりと加える)。室温で十数時間くらい反応後、反応液を氷水にあけて、分液操作で目的物を得ます。
論文では多くのオレフィンが還元可能であることを示しています。特に還元しにくい4置換オレフィンの還元も可能です。この方法は毒性の高いHMPAを使うので気をつけましょう。
1)G. M. Whitesides and W.J. Ehmann. 1970. “Reduction of Olefins Using Sodium-Hexamethylphosphoramide-t-Butyl Alcohol1.” Journal of Organic Chemistry , 35, Pp. 3565-3567.
2) R.A. Benkeser, R.E. Robinson, D.M. Sauve, O.H. Thomas, J. Am. Chem. Soc. 77 3230 (1955)
3) L. Reggel, R.A. Friedel, I. Wenden, J. Org. Chem. 22 891 (1957) Whitesides, G. M. J. Org. Chem, 1970 35 3565
アルカリ金属還元の反応性・選択性について
アルカリ金属還元の反応性についてはLi>Na>Kの順番に強くなると一般的には言われています。アルカリ金属による還元は
- 多重結合の還元(アルキン、アルケン、カルボニル等)
- 還元的開裂(C-XやC-O結合)
- 芳香環の還元
3つに分類できます。アルカリ金属還元といえば芳香環の還元が有名です。
芳香環の還元
バーチ還元ではベンゼンは1,4-シクロヘキサジエンに還元されますが、ベンケサー還元ではモノオレフィンまで還元されます。一般的にベンケサー還元のほうが還元力が強いです。
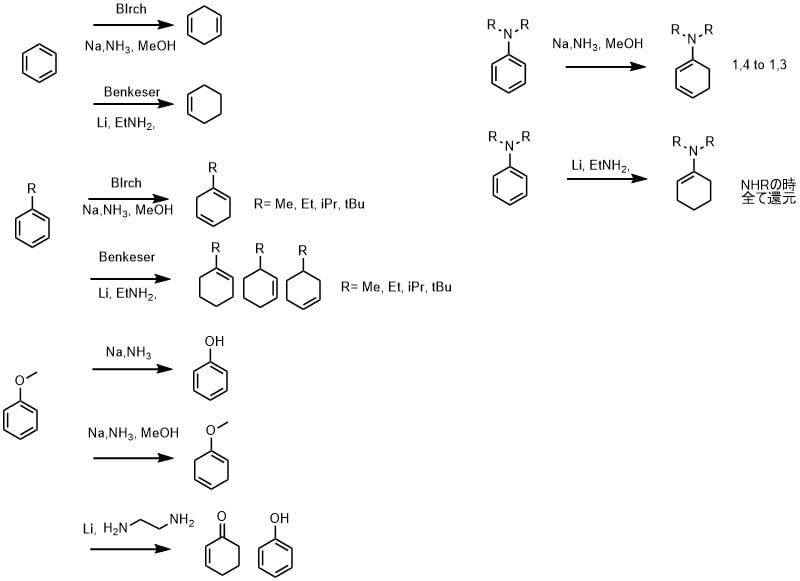
アニリン類の還元はバーチ条件では1,4から異性化して1,3が得られます。生じたエナミンは酸加水分解によってケトンに変換できます。
還元的開裂(C-ヘテロ結合[還元的脱ハロゲン化])
通常のバーチ還元条件で炭素ーハロゲン結合を開裂すると複雑な混合物が生じることが多いが、t-BuOH+THF+ Na条件で還元を行うとC-ハロゲン結合が還元、水素化されます。
参考) P. Bruck, D. Thompson and S. Winstein; Chem. Ind. (London), 1960
通常のC-O結合は開裂しにくいですが、ベンジル位のC-O結合は開裂します。ベンジル基の脱保護にバーチ還元条件が利用されることもあります。ベンジルアルコールは通常のバーチ還元条件でトルエンに還元されます。アリールエーテルなども開裂します。
ジスルフィドもバーチ還元及びベンケサー還元条件で開裂してチオールとアルカンが生成します。
多重結合の還元
アルキンの還元はPd/Cなどと言った還元とは異なりtrans-アルケンが得られます。
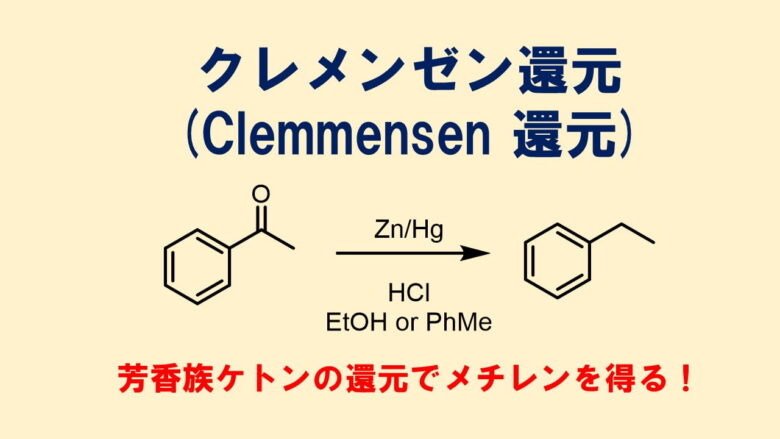
ケトンは還元されてアルコールが生成しますが、脂肪族アルデヒドはバーチ還元条件では還元されません(アルコールとアセタールを形成するため?)。芳香族アルデヒドは還元を受けて、アルカンまで還元されます。
エステルは還元されてアルコールが生成します。これはバーチ還元、ベンケサー還元両方で起こります。溶媒をアルコールとしたブーボーブラン還元はより選択性の高い還元方法として有用です。
参考
液体アンモニアはアンモニアガスボンベのアンモニアガスをドライアイスなどで冷却して液体として反応に用います。ボンベ内にある鉄が反応に影響を及ぼす可能性があるため、ガス化したアンモニアを酸化バリウムなどの乾燥剤を通して精製してから使用したほうが良いです。また撹拌子はバーチ還元専用とした方がよいです(ガラス撹拌子等)。
ベンケサー還元ではNaを使わずにLiやCaを使う。これはNaでは重合が起こりやすいためです。
液体アンモニア中の青色は何の色?
アンモニア中にアルカリ金属が溶解すると青色を呈するのは金属から離れた溶媒和電子によるものです。電子が吸収する光によってあの青色が見えています。
https://www.jstage.jst.go.jp/article/yukigoseikyokaishi1943/26/1/26_1_81/_pdf/-char/en