TLC(薄層クロマトグラフィー)の検出法の一つにニンヒドリンを用いる検出があります。今回はこのニンヒドリンを用いる検出の原理を解説します。
ニンヒドリンで検出できるもの
一般的にはアミノ基、特に一級アミノ基(R-NH2)と二級アミノ基(R1-NH-R2)の検出に使用されます。他の含窒素化合物も場合によっては検出できます。一級アミノ基は紫色、二級アミノ基は黄色に焼けます。他の含窒素化合物、特にアミドの場合は酸+熱によって分解してアミンが生成するので、やける時間が少し遅いですが紫色に焼けます。ヒートガンとかを使って高温で焼く場合は、すぐ焼けてしまうのでアミドと一級アミノ基の違いは分かりにくいです。またニンヒドリンはよくアミノ酸やタンパク質を呈色するのに用いられており、皮膚のタンパク質とも反応するので皮膚につかないように手袋をしましょう。洗っても取れません。。。
ニンヒドリンで検出できる原理
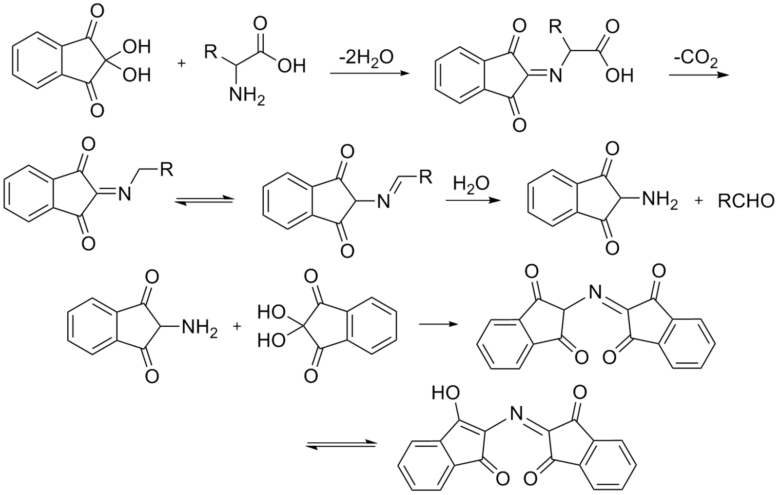
ニンヒドリンはアミンと反応することでルーへマンパープルという紫色の化合物になります。この時1級アミンでは反応機構として基質となるアミンのアミノ基が外れ後、再度もう一分子のニンヒドリンと反応して二量体のルーへマンパープルになります。しかし2級アミンの場合では二量体になることができずに、別の化合物になります。その結果2級アミンの場合は黄色を呈色します。

下の機構ではα-アミノ酸をニンヒドリンで呈色した場合の機構を記載しています。一番下に示したルーヘマンパープルは共役化合物になっており、この共役によって特定の吸光度を有することから紫色に呈色します。
実験方法
レシピとしては以下のように、ニンヒドリン、ブタノール、酢酸を入れて混ぜるだけです。混ぜた後にTLCを浸漬させて少し乾かし、200℃程度の熱で焼きます。一般的な焼き方としてホットプレートとヒートガンがありますが、先ほども書いた通り速度でも何となく官能基の予測ができるので、ニンヒドリンに関してはゆっくり焼けるホットプレートの方がオススメです。
ニンヒドリン試薬のレシピ
- ニンヒドリン 300mg
- 酢酸 3ml
- n-ブタノール 100ml
ちなみにブタノールはエタノールに変えても問題なく呈色できます。個人的にはブタノールは臭いのでエタノールにしています。ただエタノールの方が飛びやすく濃度が変わりやすいので気を付けてください。
またニンヒドリン試薬がすでに作ってあるスプレーも販売されているので、そちらを噴霧した後に焼いても問題なく呈色できます。
ニンヒドリンスプレーは200mL, 4800円(和光純薬工業)で購入できるので作るのが面倒な場合は購入してみてもよいです。スプレーは試薬調製の必要がなく楽です。欠点としては、飛び散って周りを汚しやすいということと、ディップ式と比べて塗りムラがでやすいことです。
また、ドラーゲンドルフ試薬もアミンの発色試薬としてよく利用されます。こちらは第三級、第四級アミンに対してよく発色するので、第一、第二級アミン向けのニンヒドリンと相補的に利用できると思います。
全てのTLCの記事は以下のリンクから!