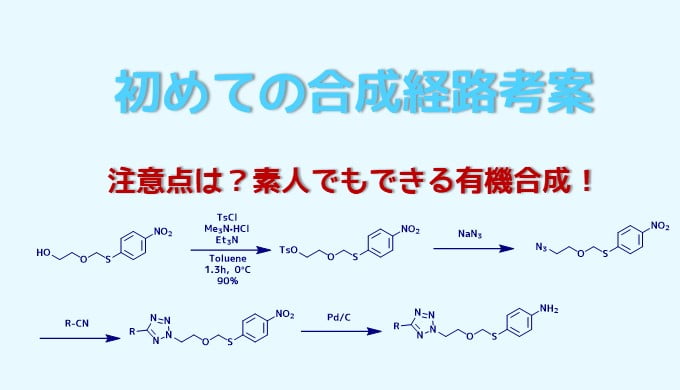
合成経路を考えるのは、初めてだとどうやってやるんだろうという不安な気持ちになるかもしれませんが、なれてくるとこの上なく楽しい作業でもあります。
そんな合成経路を考えるときの注意点をざっと上げて見ました。さっとかいたので随時更新・修正していく方針です。
合成経路を考えるときの注意点は?
目的物の入手を最優先に目指す。改良はその後でも遅くない
目的物の入手を最優先にしましょう。収率改善などがやりたくなってしまうことも多いですが、反応の最適化は目的物が得られてからでも遅くありません。
もちろんあまりにも収率が低いとか、参考の文献と比べて悪すぎるという場合は検討すべきです。
とにかく目的物が得られてからでも反応の最適化は遅くありません。そのため(保護基をつかう、無理にワンステップでやらない。収率を目指しすぎない)
不斉点は不要なら無くす減らす
不斉炭素は不必要なものであるならば、なるべく作らないようにしましょう。軸不斉などもあるので注意です。
光学異性体は判別や分離が困難です。エナンチオ選択的合成はこれまでに多くの報告がありますが、高選択的な反応はそれだけで困難です。不斉が生じる場合は予め光学純度の高いビルディングブロックを用いるか、不斉のものジアステレオマーに誘導したりする工夫が必要です。
最終物を自分である程度変更できる場合は不斉が生じないような工夫を行いましょう。二環性の化合物なら左右対称にするなどがあります。
一直線の合成経路は避ける
複数のステップに渡るような反応のときは一直線の合成経路にせず、うまく分岐できるように工夫すると後で合成経路の変更などの修正がききやすいです。
例えば、目的物ABCDを得る時
A→AB→ABC→ABCDが一直線の合成なら
A→AB、C→CD AB+CD→ABCDが分岐する合成経路です。
Aの構造を少し変えたいなと思っても最初の一直線の合成経路では最初から作り直す必要がありますが、下の分岐経路ではCDの合成はそのまま利用できます。
保護基を使いすぎない、が避けすぎない
初めて合成経路を考える時保護基を使いすぎる傾向があります(全く使わない人も…)。保護基を一回使うと、保護、脱保護で2ステップも無駄にします。時間と収率をその分失います。
慣れてきた場合は逆に不必要に避けすぎないことも重要です。保護基は確立されている最も信頼性の高い反応群の一つです。収率も高いものも多いです。
反応するかも?ぐらいなら保護しておいたほうが無難です。また精製も楽になることも多いです。複雑な分子の場合は慎重に保護基を選択しましょう・
NMRの読みやすさを考えてみる
低分子有機化合物の構造決定は主にHNMRで行います。そのためNMRが見やすいように分子構造を考えるのも重要だったりします。
例えば、1,4-置換ベンゼンはNMRがシンプルでみやすいです。
芳香族化合物がベースなら水酸基の保護にベンジル基を避けてTBS基にするとか工夫をしてみる。スペクトルが被らないように工夫します。
分子の極性は低めに抑えておく
分子の極性は低めが良いです。高極性の状態(N,O,S,CO2Hなどが裸の状態)はなるべく少なくしましょう。極性が高いと副反応が起きたり、精製が難しくなります。また有機溶媒に溶けにくくなると反応性も低下します。
最新反応にこだわりすぎない
最新の反応は何かと優れているように見えますが、高価だったり先例が少なかったりしてデメリットも多いです。古典的な反応のほうが何かと良い結果を与えることも多い。もちろん必要なら最新の反応を使います。
量上げ(再合成)はなるべく減らす
絶対な自信がある時以外はスケールは最終物の想定よりも大きめにつくっておきましょう。たまに何度も再合成している人がいますが、大抵はスケールが小さく、上手く合成が行ったときの理論収量で計算しているので全然足らなくなります。合成は上手く行かないことのほうが多いです。多めにかけておくと後々役立ちます。
反応スケールの大きさを意識する
反応の段階によって反応スケールは変化します。10ステップもあれば最初の反応はグラムスケールでも最後にはミリグラムスケールになっています。
スケールの大きさによって適する反応と適さない反応があります。
大スケールでやる場合は適さない合成方法もある(高価な試薬、反応性が高い試薬)。その逆もあります。特に反応性の高い試薬を大スケールで使用する時は注意が必要です(LiAlH4とか)は。経済的かどうかも重要です。
合成経路は必ず人に見せて相談する
合成経路は必ず人に見せて相談するのを心がけましょう。
同期でも後輩でも先輩でも良いです。なるべく多くの人とディスカッションしましょう。
思わぬ見落としや発見があることが多いです。人が一人でできることには限りが有ることを学びましょう。
炭素が一つ足らないとかも結構あります。もっと良い方法が見つかるときもある。
これはイカねーだろという反応をやってることも結構あります。
知識や気付きを増やすためにお互いのためだと思ってやりましょう。相談すると相談してくれるようにもなります。
文献を必ず参考にする
必ず文献を参考にしましょう。自信があっても、簡単なものでも独断で決めない。
各ステップ、反応が進行しなかったことを想定しておく
反応がうまくイカなかった時を考えておきます。つまり、代替案を考えるということです。このステップが進行しなかったらもう方法がないというような博打はなるべくなくしましょう。
経済性を考える
意味のない高価な試薬の使用は控えましょう。お金も限りがあります。また、高価な試薬は精神的に影響を与えることを覚えておきましょう(ズボラな人ならあまり問題ないかも?)
安価な方法なら何度も検討できるので成功確率は高くなりやすいです。
高価な試薬方法は検討回数が必然的に低下し、予想よりも得られる量が少なくても頑張って次に行って結果的に再合成が必要になるパターンもあります。上手く行かなかったときの別経路への切り替えもしにくいです。
精製容易さを考える
物質の結晶性を考えて保護基を選択すれば、再結晶で精製しやすくなります。再結晶で精製できると大スケール精製や高純度にするのが簡単になります。
また、Boc基のように脱保護後は濃縮のみで精製不要なもの。分液だけでキレイになるものなど精製が簡単な手法で合成すると楽です。
当たり前ですが高収率だと原料を分離しなくても済むので楽です。
溶解性を考える
有機合成は有機溶媒に溶けないと反応も進行しにくいですし、カラムなどで精製も困難になります。
多環で平面性が高めの分子で変に分極?したヘテロ環(あるいはニトリルとかアミドとか)を含んだりすると溶解性が悪く、DMSOなどにしか溶けなくなったりします。
経験が無いと分子の溶解性はわかりにくいので経験豊富な人に相談しましょう。基本的にSP3系(アルキル鎖とか)を含む分子運動が大きいものは溶けやすくなります。
構造展開性を考える
全合成など最終物が決まっている場合は別ですが、最終物を様々に作るタイプの合成では最終物から別の分子に誘導していくことを想定した構造を合成するのも重要です。場合によっては途中経路のものを目的物として組み立てることも可能です。(ニトリル体→アミド体→エステル体→カルボン酸体全てを最終目的物とするなど。)
危険な試薬は控える(爆発性、自然発火性、毒性)
メチル水銀など毒性が高いものは使用を控えましょう。毒物指定されているものも避けます。
また自然発火性のものや爆発性を持つものがあります。例えば、tert-ブチルリチウムやジアゾメタンなどがあります。
使用せざる負えないこともありますが、積極的に使いに行くいものでありません。
失活しやすい試薬は控える
湿気や酸素に弱い試薬は特に初心者の場合は控えたほうが無難です。反応が進行しない理由が、試薬が失活しているからか、下手くそなのか、重大なミスをしているのかわかりにくいからです。デリケートな試薬は細かいチューニング的な検討を要するものが多いです。
失活のしやすさは酸素や湿気に敏感なもの、名前がややこしいもの、有機金属錯体、高価なものなどの特徴があります。