ニトリルはアミン、アミド、カルボン酸など多くの官能基の前駆体として有用です。ニトリルは還元によってアルデヒドを合成することが可能です。
目次
ニトリルを部分還元
カルボン酸誘導体のニトリルはアルキルハライドとシアン化物イオンによる求核置換により簡単に合成できます。
ニトリルを完全に還元すればアミンになりますが、途中で止めればアルデヒドが得られます。
ニトリルの部分還元にはDIBALがよく使われます。
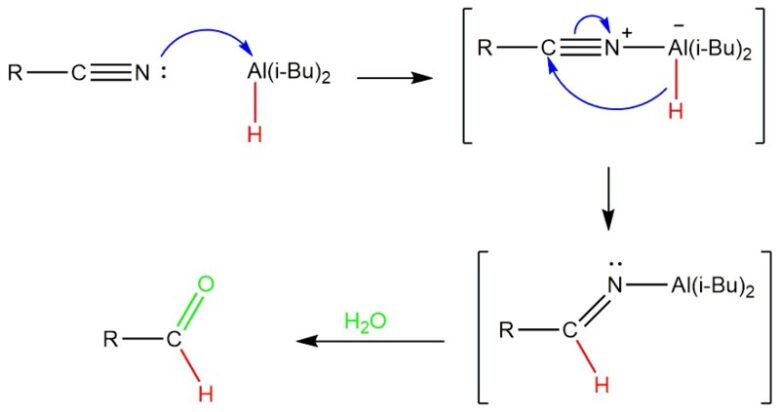
ニトリルのDIBALによる部分還元反応機構 from wikipedia Aw4809 [CC BY-SA 4.0 ]
スティーブンアルデヒド合成 (Stephen synthesis)
古典的なニトリルの部分還元としてスティーブンアルデヒド合成があります。
基本的な方法では塩化水素ガスが必要なので実験室レベルでは使いにくいですが、様々な官能基を持つアルデヒドが合成可能です。
スティーブンアルデヒド合成は塩化スズ(II)と塩酸により生成したイミニウム塩を加水分解してアルデヒドを合成します。

スティーブンアルデヒド合成の反応機構 from wikipedia Fabian.z [CC BY-SA 4.0 ]
スティーブンアルデヒド合成法は基本的に芳香族アルデヒドの合成に利用します。
一般的な合成方法
ニトリル(1mmol)に対して(2~6eq)塩化スズ(II)を加えてエーテルに懸濁し、塩化水素ガスを通じて飽和させ反応。生じた沈殿を集めて塩酸で加水分解すればアルデヒドが得られる。
塩化水素ガスがない場合は、塩化スズ(II)の4倍当量のアセチルクロライドと水を加えて塩化水素を発生させて反応させる方法もあります。
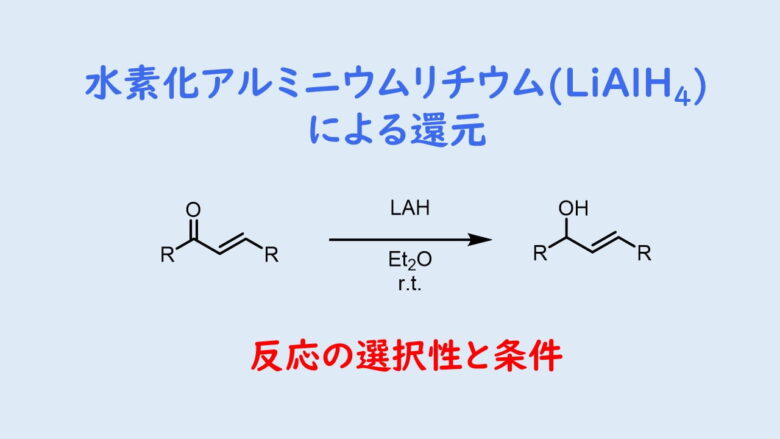
ヒドリド還元
ヒドリド還元によるニトリルの部分還元ではDIBALが最もよく利用されます。LiAlH4の当量を調製して還元することも可能です。他にはラネーニッケルやRed-Alを使う方法もあります。
DIBALをつかったニトリルの部分還元
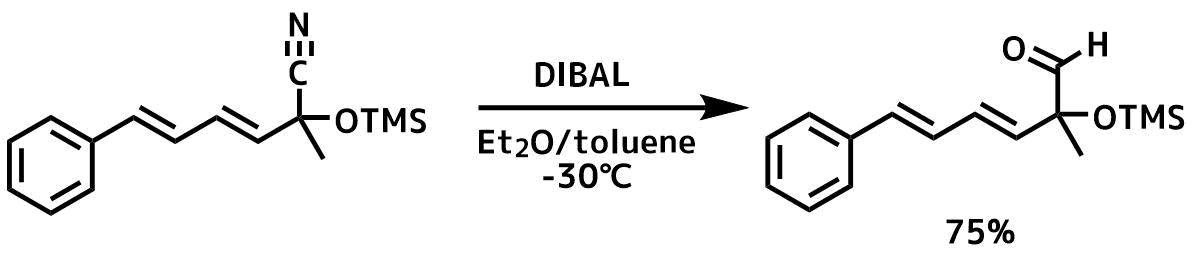
Zeng, Xing-Ping et al Journal of the American Chemical Society, 138(1), 416-425; 2016
ニトリル体(271.0 mg、1.0 mmol)脱水Et2O(4.0 mL)溶液を-30℃に冷却した後、水素化ジイソブチルアルミニウム(トルエン中1.5M、1mL)を25分間かけて滴下した。 反応後、飽和NH4Cl(10 mL)をゆっくりと加えて反応を停止させて抽出、カラム精製により目的物を75%で得た。(90%ee)
DIBALを用いた還元がニトリルの部分還元のファーストチョイスだと思います。
DIBALによる還元は-78℃で反応させることが多いです。嵩高いニトリルなどではそれよりも高い温度で実施することもあります。
反応は結構速く、3時間以内に終わることが多いです。溶媒はジクロロメタン、THFがよく使われます。
Red-Alを使ったニトリルの部分還元
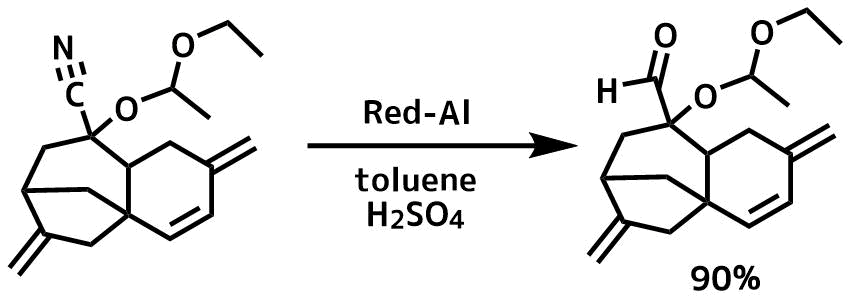
Nicolaou, K. C. et al Journal of the American Chemical Society, 130(39), 13110-13119; 2008
トルエン(10 mL)に基質(550 mg、1.84 mmol)を溶解し-20℃でRed-Al®(トルエン中65%、2.80 mL、9.18 mmol)の溶液を滴下しました。反応混合物を室温で6時間撹拌した。次に、5%H2SO4水溶液を0℃で加え、得られた混合物を室温で30分間撹拌しましたエーテル抽出し、クルードをカラムクロマトグラフィーで精製して90%で得た。
Red-Alもニトリルの部分還元に使えます。
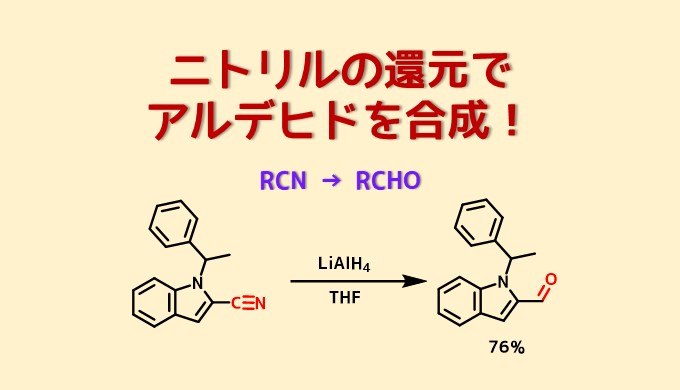
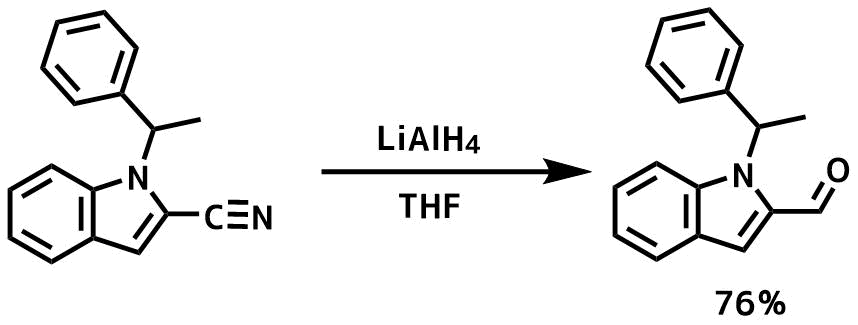
LAHを使ったニトリルの部分還元
Golantsov, N. E. et al Chemistry of Heterocyclic Compounds (New York, NY, United States), 41(10), 1290-1299; 2005
酢酸エチル(1.2 ml、12 mmol)とTHF(1 ml)の混合物を水素化アルミニウムリチウム(0.3 g、8 mmol)THF(2.5 mL)の懸濁液にアルゴン雰囲気下、0〜10℃で加え、そのまま30分間撹拌し、THF(1.5ml)に溶解したニトリル体(1g、4mmol)の溶液を0〜5℃で加えて1時間撹拌した。反応後、硫酸(5N、20ml)を加え5分間撹拌した。反応後エーテル(3×30ml)で抽出した。通常の後処理を行い、カラム精製により目的物を76%の収率で得た。