ショッテン・バウマン反応について
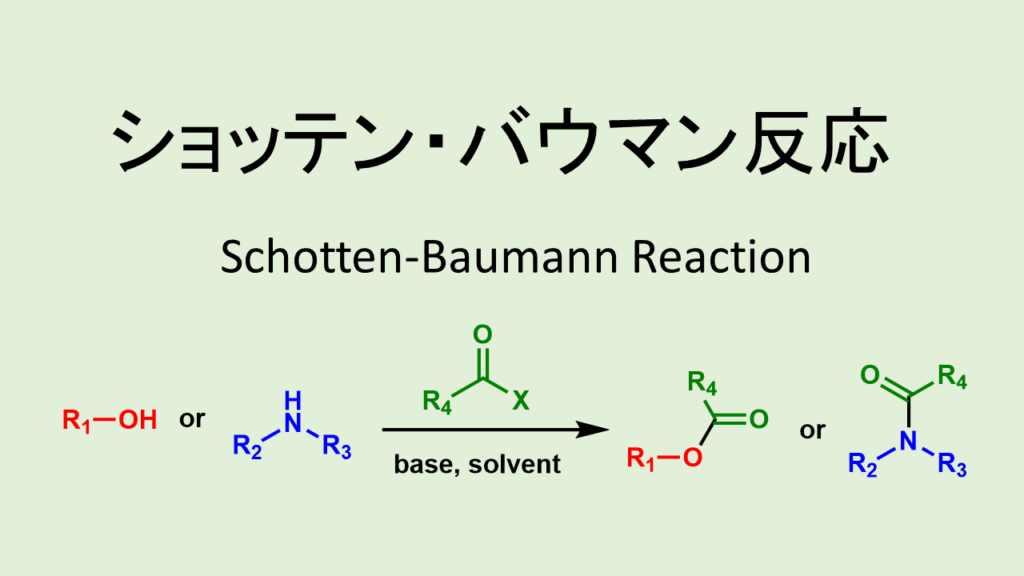
アルコール(alcohol)やアミン(amine)を無機塩基性水溶液中で酸ハロゲン化物(acyl halide)や酸無水物(anhydride)と反応させ、エステルやアミドを合成する方法をSchotten-Baunmann反応と言います。
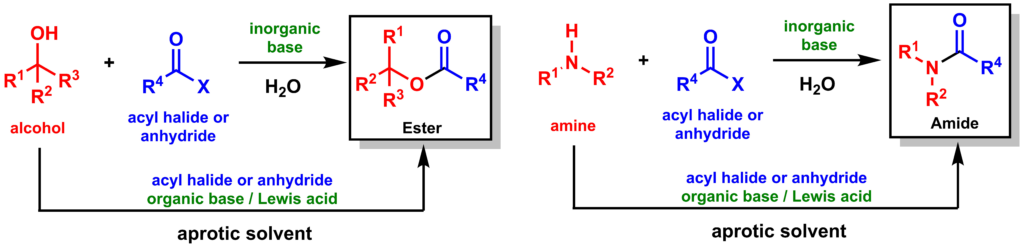
有機塩基(organic base) やルイス酸(Lewis acid)でも同様の反応が行えますが、その場合非プロトン性有機溶媒 (aprotic solvent) が用いられます(現在ではこちらの方が主流で使われています)。
ショッテン・バウマン反応の特徴
ショッテンバウマン反応は特にアミド合成によく利用されています。
ショッテンバウマン反応の利点
その他のアミド合成法と比較してショッテンバウマン反応にはいくつかの利点があります。
ショッテンバウマン反応の利点
- 有機塩基(トリエチルアミン)と比べて安価な無機塩基(NaOH,NaHCO3)が使える
- 工業的な大スケールでも利用可能
- 副反応が少なめ
- 後処理が楽
- 高極性水溶性アミンに適する
などの特徴があります。
無機塩基が使える
トリエチルアミンなどの有機塩基はどちらかと言えば高かったり、臭いがあったりして扱いにくい面があります。有機溶媒に溶けることから分離が少々面倒な場合もあります。
一方で炭酸水素ナトリウムなどの無機塩は安く、臭いもなく、有機溶媒に溶けないので後処理が簡単です。
高極性水溶性アミンに適する
しばしば、アミン類は高極性で水やメタノールにしか溶けないものもありますが、ショッテンバウマン反応では水を使うので水に溶かして反応できます。その点で高極性アミンはショッテンバウマン反応に向いています。
水に混和しない溶媒を使えば二相系で反応できます。しばしば混和するTHFなどを使います。逆にアミンが水に溶けにくい時に使ったりします。
わりと何でも有りなので、ショッテンバウマン反応は「塩基性水溶液を添加する方法」とでも考えたらよいかもしれません。
アルコールおよびアミンについて
エステル化におけるアルコールの反応性は通常通りです(第一級>第二級>第三級)。
アミンの場合は第一級、第二級が反応しやすいです。
一般に反応性の低い酸ハロゲン化物を用いると、水による迅速な加水分解を受けないため、よい収率で生成物を与えます。芳香族酸ハロゲン化物は脂肪族酸ハロゲン化物より含水条件下で安定なため、Schatten-Baumann反応によるアシル化に適しています。
第二級および第三級アルコールのアシル化には塩基が必要ですが、第一級アルコールのアシル化には塩基は必須ではありません。
第一級アルコールは副生成物であるハロゲン化水素によって生成したエステルが加水分解を受け難いため塩基を加えなくてもよいです(入れたほうが反応性は高い)。
アミンのアミド化には塩基の存在は必須です。副生物の酸がアミンを塩にして反応性を低下させるからです。
塩基について
使用する塩基は基質のアミンよりも強塩基でなければいけません。立体的に込み合った基質のアシル化のために、種々の改良法が開発されていおり、現在ではアシル化は主として非プロトン性有機溶媒中、ピリジンやDMAPなどの有機塩基やLewis酸を用いて行うのが一般的です。
塩基は報告初期の条件ではNaOHを使用していたようですが、HClのトラップができればよいので、もう少し弱いNaHCO3、Na2CO3などの炭酸塩で十分です。実際に炭酸水素ナトリウムは良く利用されています。塩基は水に溶かして加えます。
酸ハロゲン化物および酸無水物について
ショッテンバウマン反応では酸塩化物は、塩化アセチルなどの低分子の脂肪族酸塩化物は加水分解しやすいので不向きである可能性がありますが、芳香族を始め多くの酸塩化物はショッテンバウマン条件を利用できます。
溶媒について
溶媒は二層系でトルエンやジクロロメタン、ジエチルエーテルを使います。アミノ酸など水溶性が高いアミン類はより極性が高く水と混和するTHFやジオキサンを使うことが多いです。二相系にこだわる必要は無いです。
酸塩化物が意外と溶媒に溶けず、滴下する時に困るので溶けやすいものを選ぶとよいです。
反応の歴史
1884年にC. Schottenは、ピペリジンと塩化ベンゾイルを水酸化ナトリウムの存在下に水中で反応させ、N-ベンゾイル、ピぺリジンを得る効率的方法を報告しました。
1886年にはE. Baumannは、この反応条件がアルコールと塩化ベンゾイルから安息香酸エステルを合成する方法として適していると報告しています。
実験手順
適当な溶媒に溶解させた酸塩化物1当量を氷浴したアミン(1当量)+飽和NaHCO3水溶液(適当、過剰)+適当な溶媒の混合溶液に滴下して加えて、徐々に室温に戻しながら数時間激しく撹拌し、反応が完了したらそのまま分液して濃縮してアミド体を得ます。
塩基は理論的に1当量あれば十分ですが、特に厳密に量ることなく加えても問題ないです。副反応の懸念がある場合は1~2当量分の塩基を加えて反応させても良いです。
二相系の場合は激しく撹拌します。