核酸の構造、DNAとRNAの違い、核酸の合成方法、グリコシル化反応について説明しています。また、ヌクレオシド類縁体の合成や、核酸研究の歴史についても紹介します。
核酸とは
ヌクレオチド(塩基、糖、リン酸)が重合したポリマーのこと(DNAやRNA)。遺伝情報を保存、伝達する役割があり、遺伝子はタンパク質をつくる設計図のようなものである。
ヌクレオチドは糖、塩基、リン酸で構成される
核酸の構成単位はヌクレオチドであり、さらにヌクレオチドを分解すると1. 糖、2. 塩基 3. リン酸の部位から構成されている。
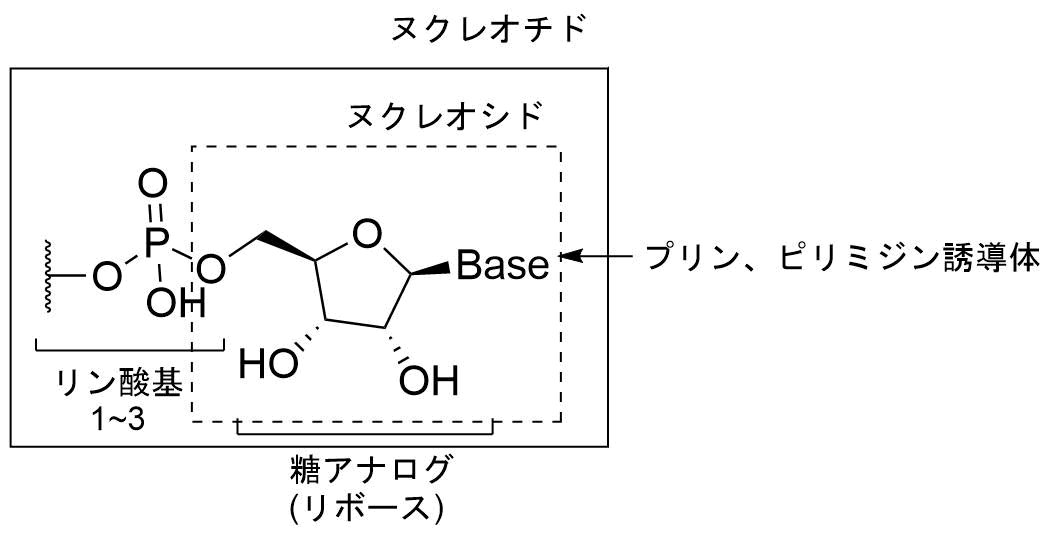
ヌクレオチドの基本構造
よく耳にするATPはヌクレオチドであり、塩基がアデニンのリボースでリン酸基が3つ結合した分子です。
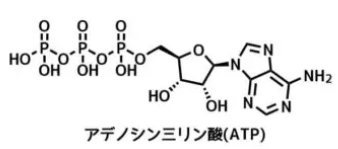
ATPの構造
ちなみにAMPはMonoリン酸のためリン酸基が1つだけのものです。
糖の種類はリボース、デオキシリボースがあります。
- 糖:リボース、デオキシリボース
- 塩基:塩基はプリンとピリミジンの二種類に大別される。
- プリン骨格:アデニン(A)、グアニン(G)
- ピリミジン骨格:シトシン(C)、チミン(T)、ウラシル(U)
ヌクレオシドとヌクレオチドの違い
ヌクレオチドのリン酸基が無い、糖と塩基からなる物質をヌクレオシドと呼びます。リン酸はすべて共通な構造であるため、特徴的なのはヌクレオシド部分と言えます。
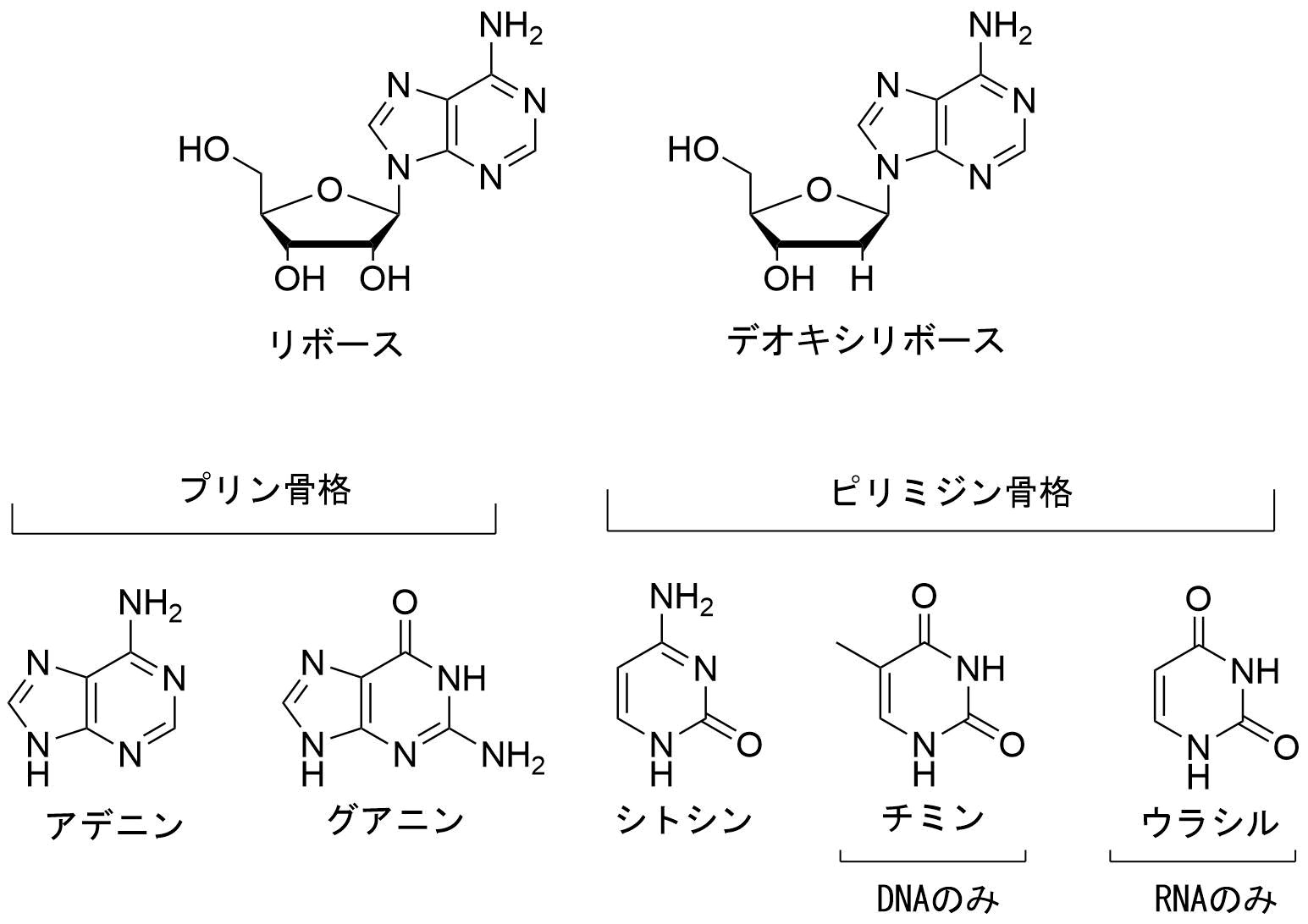
ヌクレオシドの構造一覧
- ヌクレオシド:糖+塩基 (アデノシン、チミジン…)
- ヌクレオチド:糖+塩基+リン酸
- ATP (アデノシン三リン酸)…
- GDP (グアノシン二リン酸)…
核酸 DNAとRNA
「DNAとRNA」とヌクレオチドとの間にはどのような関係があるでしょうか。
DNAの二重らせん構造 from wiki PD
DNAは糖部がデオキシリボース、RNAは糖部がリボースからなるヌクレオチドが二重らせん状に連なった構造になっているポリマーです。
- DNA:糖がDeoxyribose、塩基がA,G,C,T
- RNA:糖がRibose、塩基がA,G,C,U
核酸の構造
DNA、RNAの伸長は、どちらも5’位のリン酸と3’位の水酸基とリン酸ジエステル結合を形成するため向きがあります。(5’→3’)
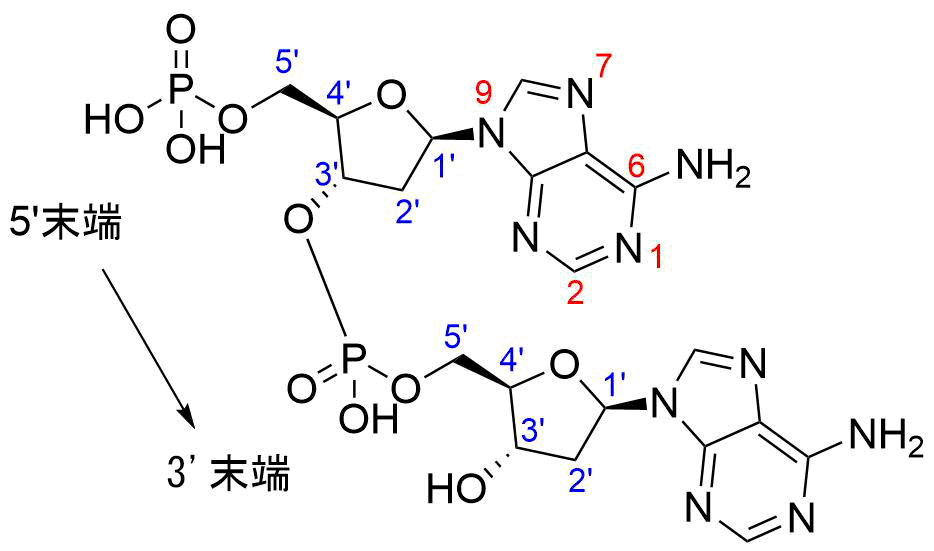
5’末端と3’末端
DNAは一本鎖の塩基同士が対を形成し、右巻きの二重らせん構造をとる。この時に対をなす塩基は決まっており、相補的(A/T,G/C)です。
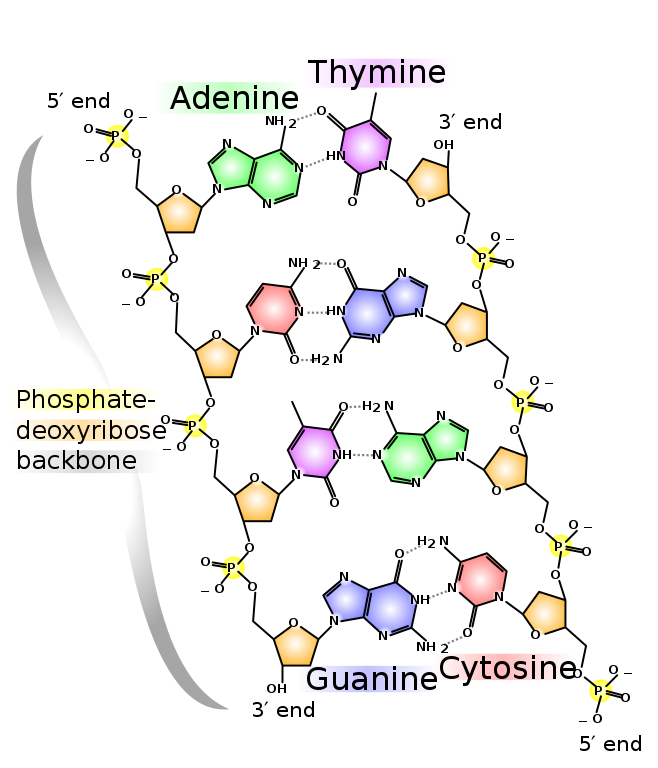
DNAの構造 Madprime (talk · contribs) / CC0
1869 :Johannes Friedrich Miescherが細胞内からリン酸豊富な化合物を単離「ヌクレイン」と命名
1885 :Albrecht Kosselがアデニン、チミン、シトシンを発見
1909 :Levene がRNAを発見
1928 :Griffithがバクテリアの形質転換についての論文を出版
1929 :LeveneがDNAとRNAの二種類の核酸があることを示す。
1935 :KleinとThannhauserがDNAを単離、結晶を取り出す事に成功する。
1944 :Averyらは肺炎双球菌を用いてDNAが形質転換を引き起こす原因物質であることを証明。遺伝子の正体がタンパク質ではなくDNAであることを示唆した。
1950 :Toddは化学合成によってヌクレオシドの構造決定を行う。
1952 :HersheyとChaseは放射性同位体ラベル(32Pと35S)したファージを使いDNAが遺伝子の原因物質であることを証明した。(ノーベル賞受賞)
1953 :Watson、Crick、WilkinsらはDNAの二重らせん構造を明らかにした(ノーベル賞)
1956 :Kornbergは初めてDNA合成酵素であるDNAポリメラーゼⅠを発見(ノーベル賞)
1959 :Iodoxuridineが世界初のヌクレオシド系抗ウイルス薬として認可(単純ヘルペスウイルス)
1964 :AZTが抗がん剤として合成された
1969 :Cytarabineが抗がん剤として有効であることが明らかになった
1977:Aciclovir抗ウイルス薬として開発された
1980s:AIDSの原因ウイルスがHIVであることが同定された。
1985 :AZTに抗HIV活性があることが明らかになった。
1990-:生物活性を有するヌクレオシド類縁体が多数発表(抗がん剤、抗ウイルス薬、免疫抑制剤、抗原虫薬、高心臓病薬[1])
[1] ホスホジエステラーゼ阻害薬→cAMP濃度上昇→細胞内Ca濃度上昇
核酸合成の軌跡
1950年代までは核酸の構造、機能等の解析、同定などが中心に研究されてきました。
1960-1990まではいくつかのヌクレオシド系の化合物が抗ウイルス、抗がん剤に有効であることが明らかになり、医薬品としての有効性が示されています。1990年代に入ってからは医薬品としての開発が積極的に行われてきました。
ヌクレオシド類縁体の合成
一部の構造改変することにより、機能を変化させたヌクレオシド類縁体の合成が行われています。特に抗ウイルス薬、抗がん剤としての利用例が多いです。
ヌクレオシドの変換例を以下に示します。
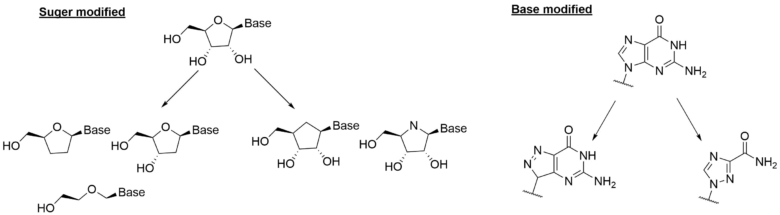
ヌクレオシド変換例
ヌクレオシドの変換は糖の変換と塩基の変換の二種類に分けられます。
糖の場合は糖骨格のアセタール原子を炭素などに置換する。あるいは、アルコールを省略する、あるいはフッ素などの置換基を導入するなどのバリエーションがあります。
塩基の場合は環の構造を省略したり、ヘテロ原子の位置や数を変えたものなどが作られています。
ヌクレオシド合成の問題点
ヌクレオシドは糖の持つ複数の立体中心と塩基と糖由来の極性の高さなどから取り扱いが難しく、ヌクレオシドの合成は、その豊富なヘテロ原子数と立体制御を要するため、簡単な官能基変換でも多段階な合成経路になる場合が多いです。
・合成戦略
基本骨格がヌクレオシドの構造に近い場合は、アデノシン、シチジン等のヌクレオシドを原料に合成を行います。ヌクレオシドのままでは合成が難しい場合は、糖と塩基を結合するグリコシル化を行って合体させます。アノマー位は立体中心であるため、立体制御が必要です。合成方法によってはプリン環を後から構築するという方法もあります。
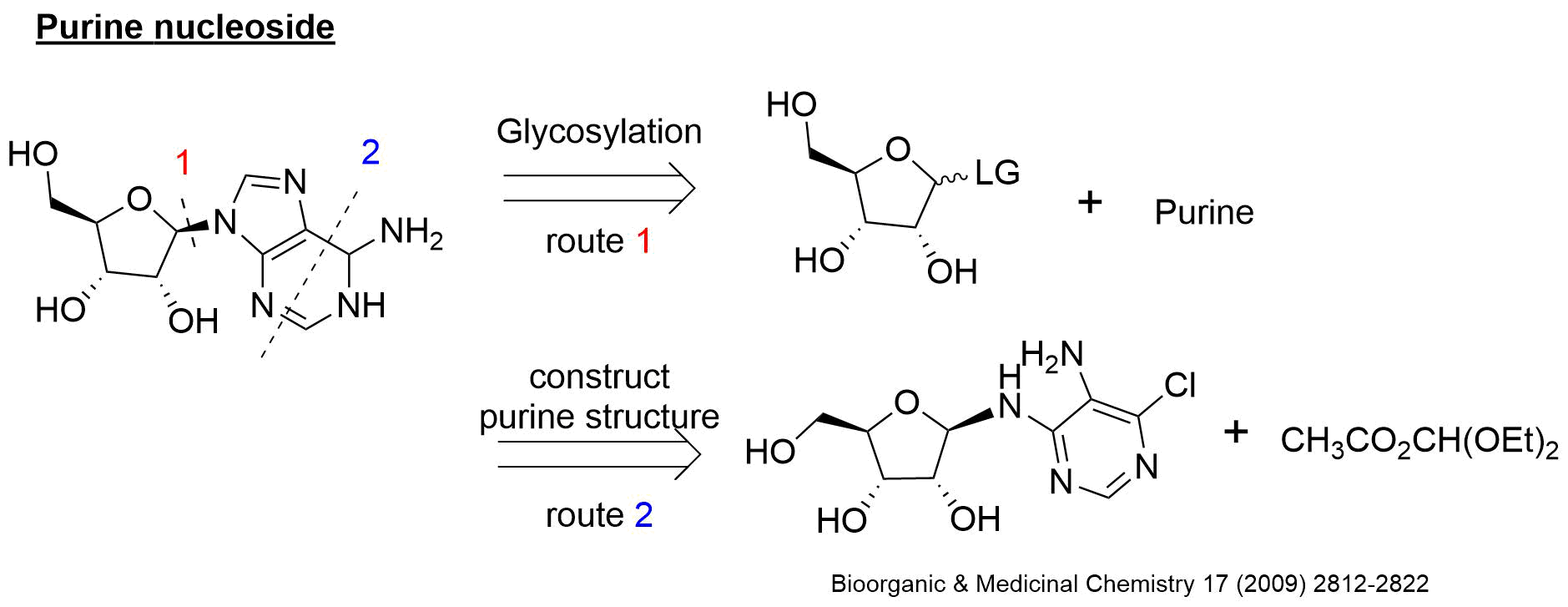
グリコシル化反応の概要
グリコシル化
糖のアノマー位においてO, N, C -アセタールを形成する反応をグリコシル化反応といいます。
天然のヌクレオシドはN -グリコシドです。例えば脱離しやすいプリン塩基の安定性を向上させるために、塩基の側の原子を炭素(C-グリコシド)にしてより強固にするという戦略があります。
ヌクレオシド合成において、アノマー位の立体制御が鍵となっています。
1948年の初のヌクレオシド合成(Toddら)から現在に至るまで多数の立体選択的グリコシル化反応の論文が発表されています。
ヌクレオシド合成において、アノマー位の立体制御が課題です。
1948年の初のヌクレオシド合成(Toddら)から現在に至るまで多数の立体選択的グリコシル化反応の論文が発表されている。
アノマー位とは?
糖の1位の塩基が結合する位置をアノマー位と呼びます。
アノマー位は、最も大きい番号を有する不斉炭素上に結合している水酸基と互いにシスであればβ-アノマー、トランスであればα-アノマーと呼びます。
選択的Nグリコシル化反応
Todd、Fischerらが報告した古典的なNグリコシル化反応では水銀塩を使用して立体選択性を出しています。
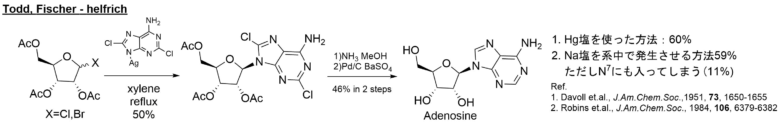
Nグリコシル化反応 todd, fischer
また隣接基効果を利用して立体選択的にグリコシル化反応を行う方法も報告されています。
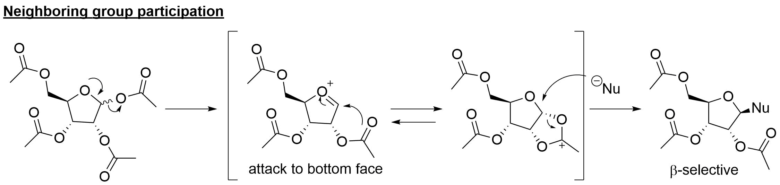
隣接器関与を利用した選択的グリコシル化
QA表
Q: ヌクレオチドとは何ですか?
A: ヌクレオチドは、塩基、糖、およびリン酸から構成されるモノマーであり、これらが重合して核酸(DNAやRNA)を形成します。
Q: DNAとRNAの主な違いは何ですか?
A: DNAの糖部はデオキシリボース、RNAの糖部はリボースであり、また、DNAの塩基はA, G, C, Tで、RNAの塩基はA, G, C, Uです。
Q: グリコシル化反応とは何ですか?
A: グリコシル化反応は、糖のアノマー位でO, N, C -アセタールを形成する反応を指します
登場する専門用語
ヌクレオチド
ヌクレオシド
グリコシル化反応
アノマー位
プリン骨格
ピリミジン骨格
関連する現象と概念:
関連する概念
核酸の合成
DNAの二重らせん構造
核酸研究の歴史
立体選択的グリコシル化反応
抗ウイルス薬や抗がん剤の開発



