Fries転位は酸触媒下フェニルエステル(アシルフェノール)のアシル基の移動によって芳香族ケトンを生成する反応です。
目次
Fries転位とは?
Fries転位はフェニルエステルを塩化アルミニウムなどのルイス酸触媒下で分子内および分子間でアシル転位をおこして芳香族ケトンを生成する反応です。
フェノールは求電子置換反応を起こしやすいので合成的な有用性は低いかも?
反応機構
フリース転位の機構は複数の機構が関わっているとされ、完全には解明されていません。
塩化アルミニウムがカルボニルに配位し、アシリウムイオンを生成、これに芳香族求電子置換反応を起こしてケトンが生成します。
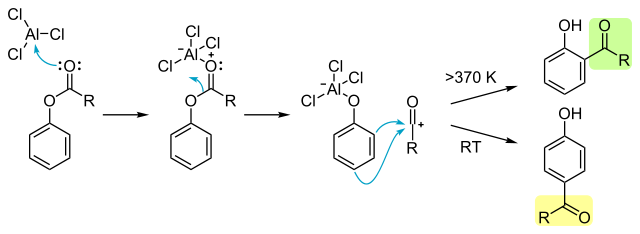
フリース転位の反応機構 from wikipedia public domain
この機構を見ると自身のフェニルエステルを求電子剤としてフリーデルクラフツ・アシル化反応が進行しているとも言えますね。
Fries転位は光によるラジカル機構でも起こることが報告されています(光フリース転位)。フェニルエステルに対して245-330nmの紫外線を照射するとラジカル開裂を起こしてアシルラジカルが再結合によりアシル化が進行します。ラジカル機構では電子不足な芳香環に対しても進行し、オルト位が優先的にアシル化されます。

ラジカル機構によるFries転位 from wikipedia public domain
反応条件
反応はフェニルエステルのオルト位またはパラ位で起こります。
パラ位が生成しやすい反応条件としては
- ルイス酸濃度が高い
- 溶媒の極性が高い
フリース転位の利点
フリース転位はtert-ブチルケトンの導入に有用です。
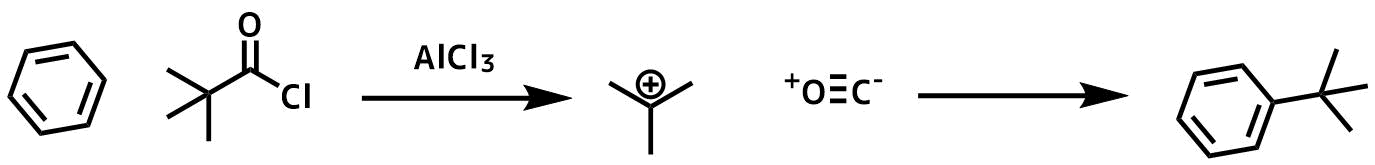
ピバルクロリドを使って通常の条件でフリーデルクラフツ・アシル化を行おうとすると、一酸化炭素を出して分解し、生成したtert-ブチルカチオンに対してフリーデルクラフツ・アルキル化が進行して、ケトン体は得られません。
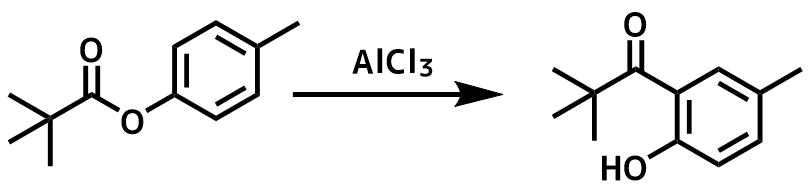
ピバルエステルのフリース転位
一方でtert-ブチルエステルをFris転位させるとヒドロキシフェニルケトンが得られます。