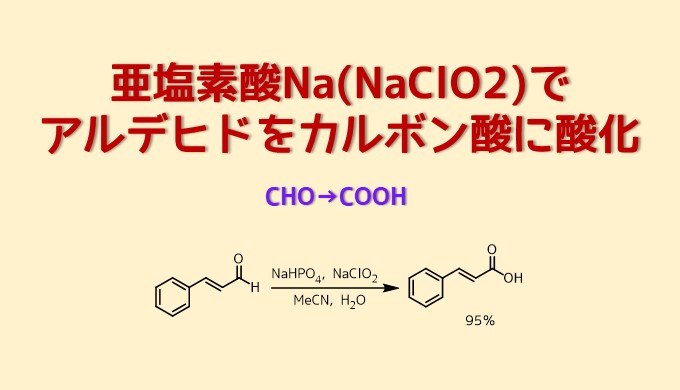
亜塩素酸ナトリウム(NaClO2)は脂肪族から芳香族のアルデヒドをカルボン酸に変換する酸化剤として有用です。
本記事では亜塩素酸ナトリウムを使ったアルデヒドからカルボン酸への変換について紹介します。
アルデヒドを穏やかに選択的に酸化してカルボン酸に変換
亜塩素酸ナトリウムはアルデヒドを容易にカルボン酸に酸化する試薬として良く利用されています。穏やかなため全合成などでもよく用いられています。
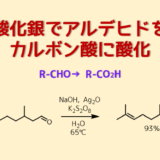
特に、アルコールからカルボン酸に変換する際は、ジョーンズ酸化や過マンガン酸カリウム酸化など強力な酸化を嫌って、アルデヒド、カルボン酸と二段階酸化を行うことが多いです。
亜塩素酸ナトリウム酸化の特徴
亜塩素酸ナトリウムによるアルデヒドの酸化はいくつかのアドバンテージがあります。
- 安価
- アルデヒド選択的
- 穏やか(室温)
- 中性
などがあげられます。
反応条件
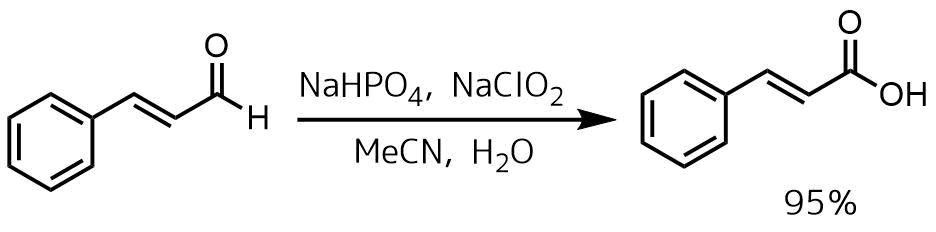
E.Dalcanale et al, J.Org.Chem., 51, 567, (1986)
NaClO2(0.07 mmol)の水(70mL)をシンナムアルデヒド(0.05mmol)、NaHPO4(1.6g) in 20mL水、35%H2O2(0.05mmol)、アセトニトリル(50mL)の溶液に10℃を保つように2時間かけて加えたのち、1時間攪拌を続け、亜硫酸ナトリウムを加えてクエンチ、10%の塩酸を加えて酸性にして沈殿をろ過して収率95%で得た。
亜塩素酸ナトリウム+過酸化水素を加えた条件です。過酸化水素は酸化剤でもありますが、次亜塩素酸のスカベンジャーとして機能します。
HOCl + H2O2→HCl + O2 + H2O

Radspieler, Alexander “Studies on the Synthesis of Diazonamide A and Phorbazol A and C” 2007
ジオキサン40 mL中のアルデヒド(10.0 mmol)の溶液に、NaH2PO4 1.679 g(14.0 mmol)およびH2O 20 mL中の1.361 g(12.0 mmol、H2Oの30%溶液)H2O2の溶液を10℃に冷却しながら加え、続いて水5mLに溶解したNaClO2 (12mmol)の溶液を激しく攪拌しながら滴下し、室温で1.5時間攪拌した。約0.4 mLのNaHSO3溶液(10%)を注意深く添加してクエンチし、反応混合物を2 N塩酸でpH = 3に酸性化し、沈殿した生成物を濾別した。溶液を濃縮して半分量にしてEtOAcで抽出し後処理をして再結晶により精製して目的物を89%で得た。
こちらも過酸化水素を加えています。

Goff, Dane et al patent. 2013116491, 08 Aug 2013
テトラヒドロフラン-t-ブタノール(7:3、10 mL)のピリジンカルボキシアルデヒド(0.370 g、1.01 mmol、1.0 eq)の溶液に、亜塩素酸ナトリウム(0.136 g、1.52 mmool、1.5 eq)水(5 mL)中のスルファミン酸(0.147 g、1.52 mmol、1.5 eq)の水溶液を加えた。反応物を室温で20分間撹拌した後、EtOAc(70mL)とブライン(50mL)で分液した。後処理をして目的物を85%で得た。
スルファミン酸を加えて副生する次亜塩素酸をトラップしています。
亜塩素酸ナトリウムから副生する次亜塩素酸の副反応を防ぐ
アルデヒドに対して酸化すると副生成物として次亜塩素酸(HOCl)が生成します。この次亜塩素酸は塩素を発生させたり、二重結合と反応したりすることが問題で不飽和アルデヒドの酸化に適さない問題がありました。
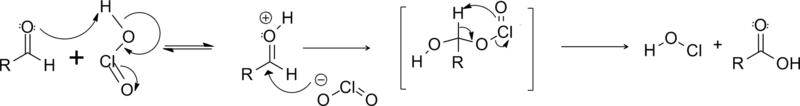
from wikipedia public domain
そこで考えられたのが反応しやすいアルケンをあらかじめ入れてしまうという方法です。
その代表例が2-メチル-2-ブテンです。
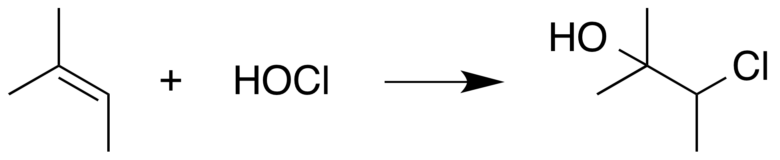
2-メチル-2-ブテンと次亜塩素酸との反応 from wikipedia public domain
これを入れることによって副生した次亜塩素酸と代わりに反応してくれることによって副反応を低減できます。
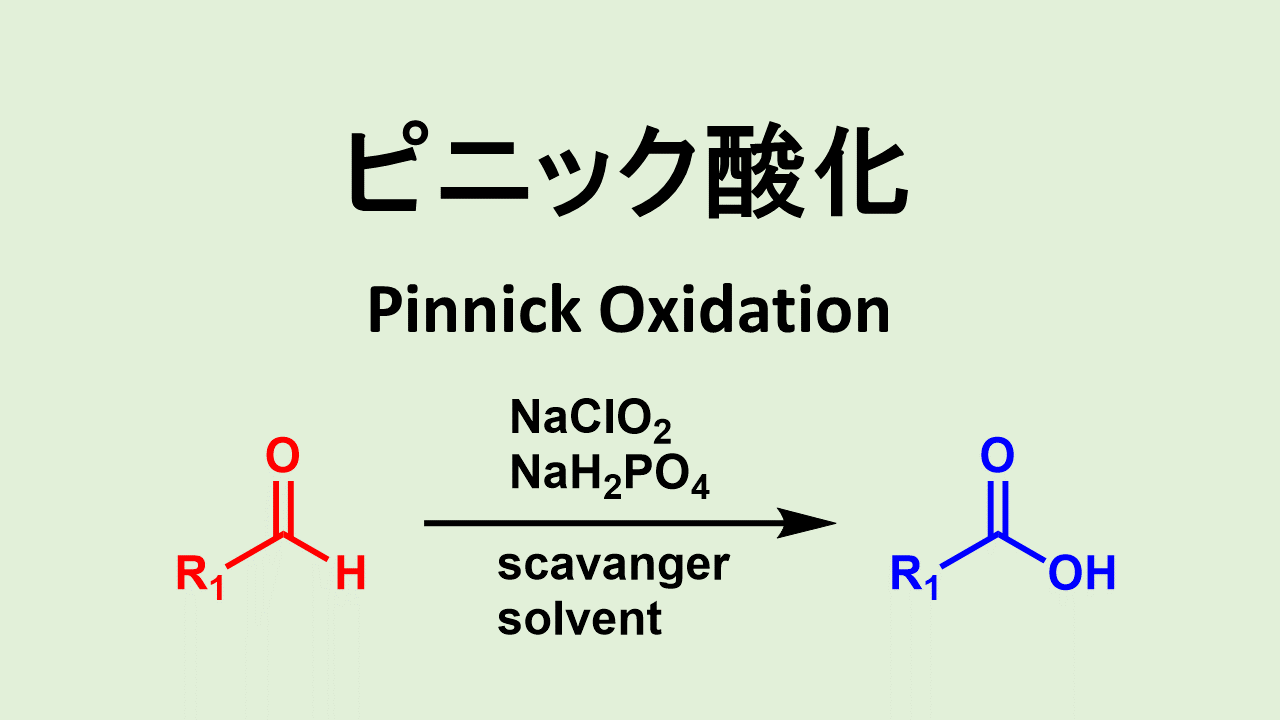
ちなみにこの2-メチル-2-ブテンを加えた条件は「ピニック酸化」という人名反応になっています。