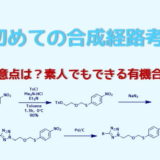
逆合成解析とは?
逆合成解析とは目的の化合物を得るための合成手順を考える方法のことです。
なにが”逆”なのか?というと、通常の合成手順が「小さいブロック→大きいブロック」に組み立てていく方向ですが、
逆合成は「大きいブロック→小さいブロック」を見つけ出していくので、通常の合成と方向性が逆だからだと思います。
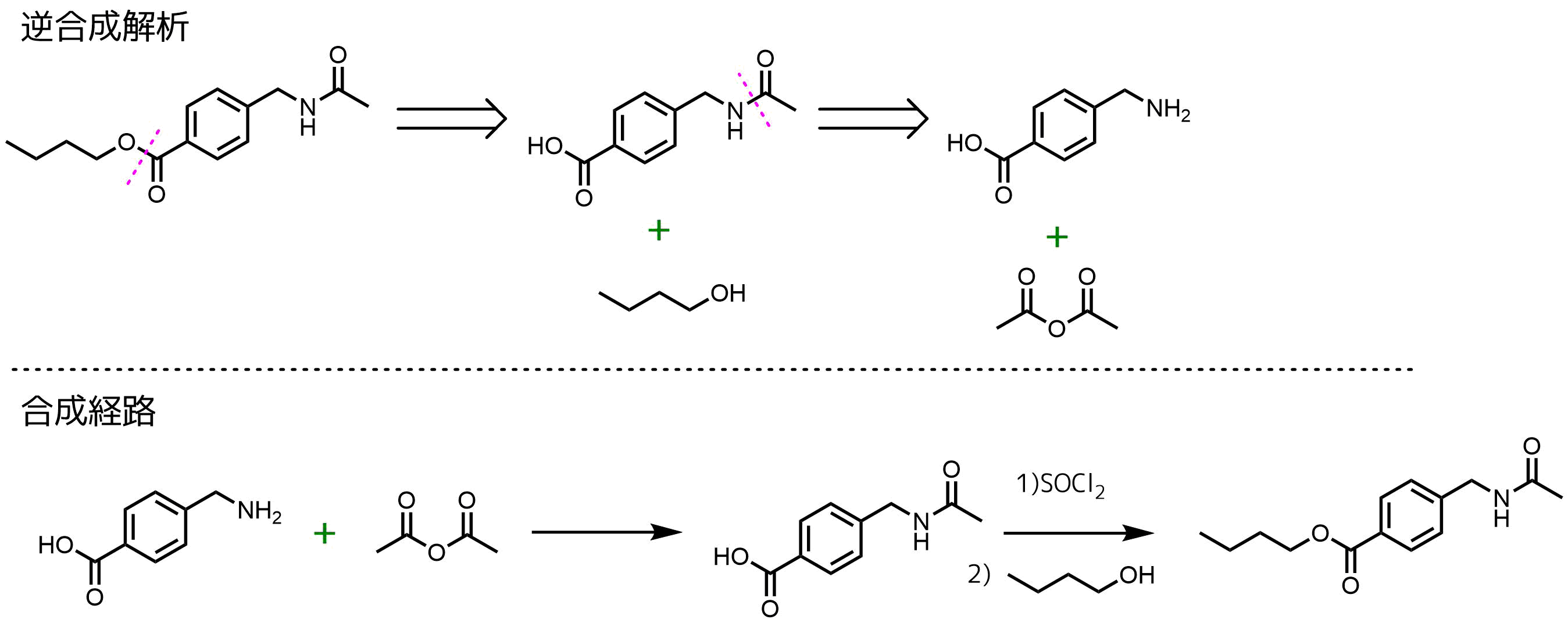
逆合成解析の例と合成経路の決定
逆合成解析の結果は無数にありますが、目的は標的化合物を合成するための合成計画を導き出すことにあるため、実用性が高いものでなければなりません。
そのため、逆合成解析には「反応の知識」が不可欠です。そのうえで
- 反応収率が高いか(競合する箇所・反応、精製の容易さ)
- 原料は入手容易か
- 中間体の再利用性
- 安全性の高さ
- 合成経路のコストは低いか
- 代替案はあるか
- ステップ数を短縮できないか
- 反応の信頼性は高いか(参考文献や知見・経験は豊富か?)
- 立体化学の制御
などを考慮した上で適切な経路を考えていきます。
切断する箇所だけでなく、組み立てる順番も考慮する必要があります。
実際に合成経路を考えるときは「どのような目的で合成するのか?」も重要です。選択すべき反応や経路が異なってきます。
例えば工業的に大量に合成する場合は爆発したり、繊細な手技あるいは非常に高価な試薬を要する反応は不向きです。
機能性を調べる場合は特定の部位は類似した別の構造に置き換え可能かもしれません。また、中間体から類似の化合物を大量に合成できる経路が好ましいかもしれません。
逆合成解析のやりかた
シントンから合成等価体を考える
シントンは逆合成解析の際に結合を切断したときにできる仮想的な構造単位のことです。
ヘテロリシスで結合切断を起こすとマイナスとプラスの構造単位が生まれます。
プラスとマイナスは2通り考えられますが、このうちどちらが現実的か?を考えます。
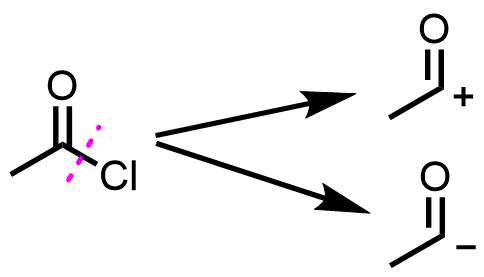
カルボニル炭素は+と-どちらが現実的?
下記の例ではカルボニル炭素が+になるパターンと-になるパターンが考えられますが、カルボニル酸素が陰性であるため炭素上にマイナスがのっかる構造よりもプラスのほうが自然です。そのため上のシントンの組み合わせを反応を考えていきます。
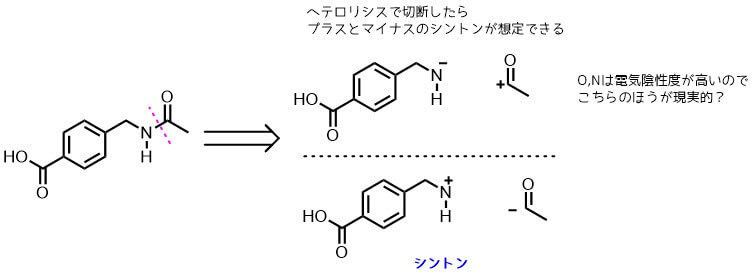
元の化合物の結合を切断し部品を考える
カルボニル炭素が+になる求電子剤としては無水酢酸や塩化アセチル、活性エステル(スクシンイミジルエステル)などがあります。これらは構造や反応性などは異なりますが、合成上どれも同じ役割(同じシントン)を与えるため、合成等価体と呼びます。
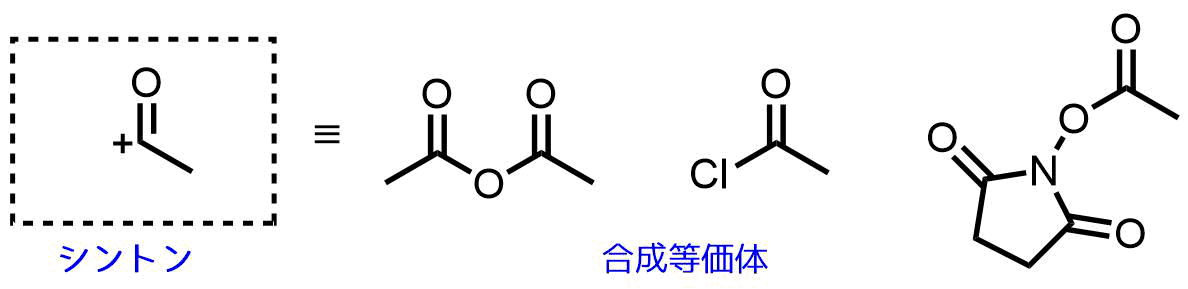
カルボニル炭素が+になる合成等価体
もう片方の相手はアミン(-NH2)ですが。アミンは中性のままで求核性があるためNH2で反応します。
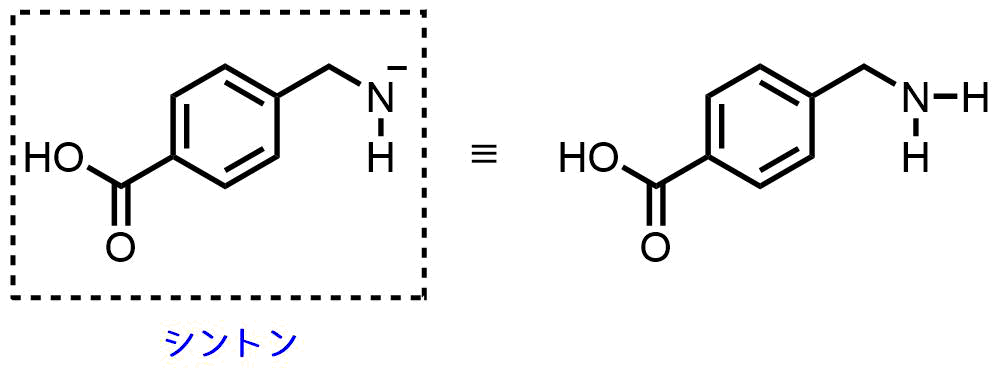
逆合成解析の戦略
環(ベンゼン環)を中心に考える。
標的化合物中に環構造を含む場合、特にベンゼン環がある場合はベンゼン環周辺の結合を切断していく。
ベンゼン環の結合をぶった切るような逆合成解析は基本的には行わない。
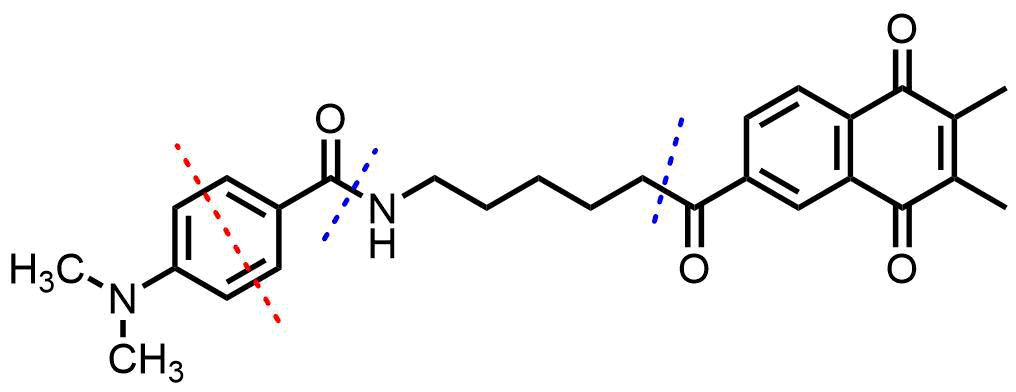
赤線のようなベンゼン環の結合切断は行わず、青線のような環周辺の結合を切断
ベンゼン環周辺の結合を切断していくと最終的にベンゼンから合成するような形になりますが、別にベンゼンから合成する必要はありません。それ以前の中間体で入手可能な安価な原料があればそこから合成していけば良いです。
官能基に着目!FGI (官能基相互変換)を行う
結合を切断して合成を考えると下記のような形になりますが、こうした結合切断だけではアイデアに限りがあります。
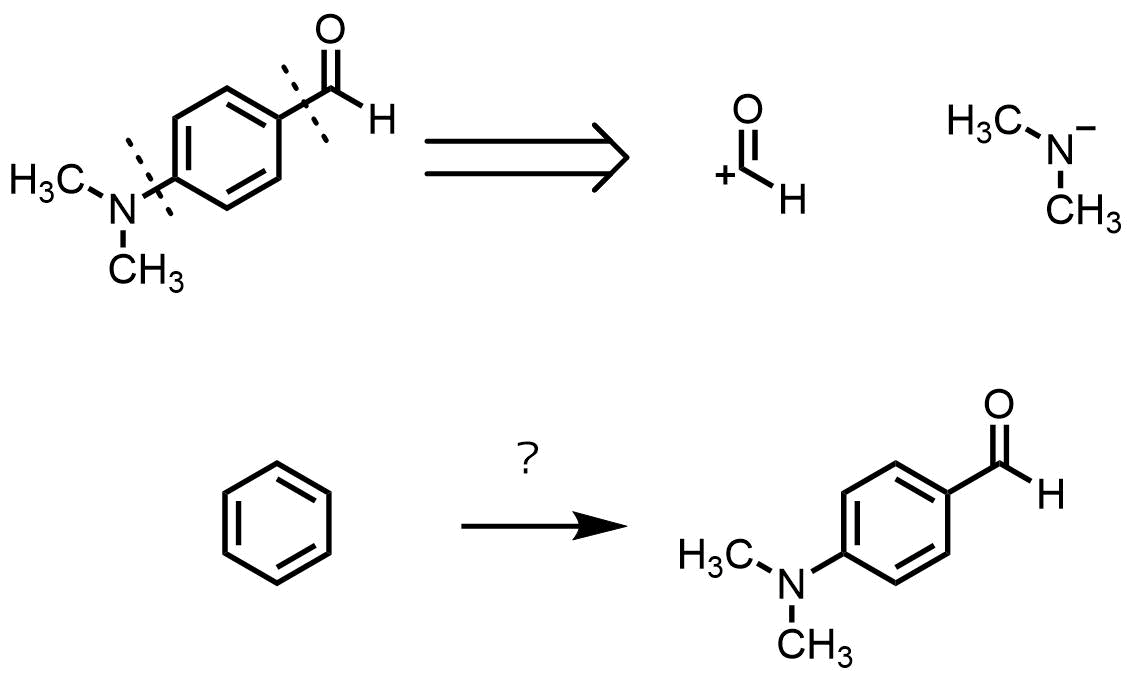
ベンゼン環から作るべき?
例えば下記のような出発物質?
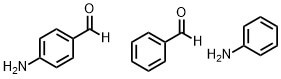
そんな時は化合物の官能基に着目します。
官能基は酸化・還元反応等によって官能基Aから官能基Bに簡単に変換できるものがあります。
これを逆合成解析の用語でFGI(官能基相互変換)と呼びます。
例えば、下記のようにアニリン(-NH2)はニトロ基(-NO2)の還元により簡単に得ることができます。ニトロ基の還元は信頼性の高い反応、かつニトロ基は安定なのでよく使われます。
一方アルデヒドはアルコールの酸化から得られますが、芳香族化合物の場合はトルエンのCH3から酸化してアルデヒドに変換することも可能です。
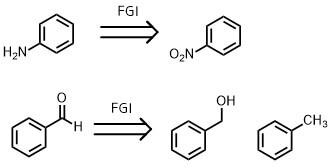
FGIの例
これでニトロベンゼン、p-ニトロトルエンも原料の候補に入ります。ベンゼン環への窒素の導入法としてニトロ化はごく一般的で信頼できる反応であるためよく使われます。
ベンゼンからトルエンの合成は必要ありません。トルエンは原料として安価に入手可能ですし、ベンゼンは毒性があるという観点からもトルエンを使う方が好ましいです。また、基本的に炭素-炭素結合形成反応は炭素-ヘテロ元素結合形成よりも難しいため避けられるのなら避けます。
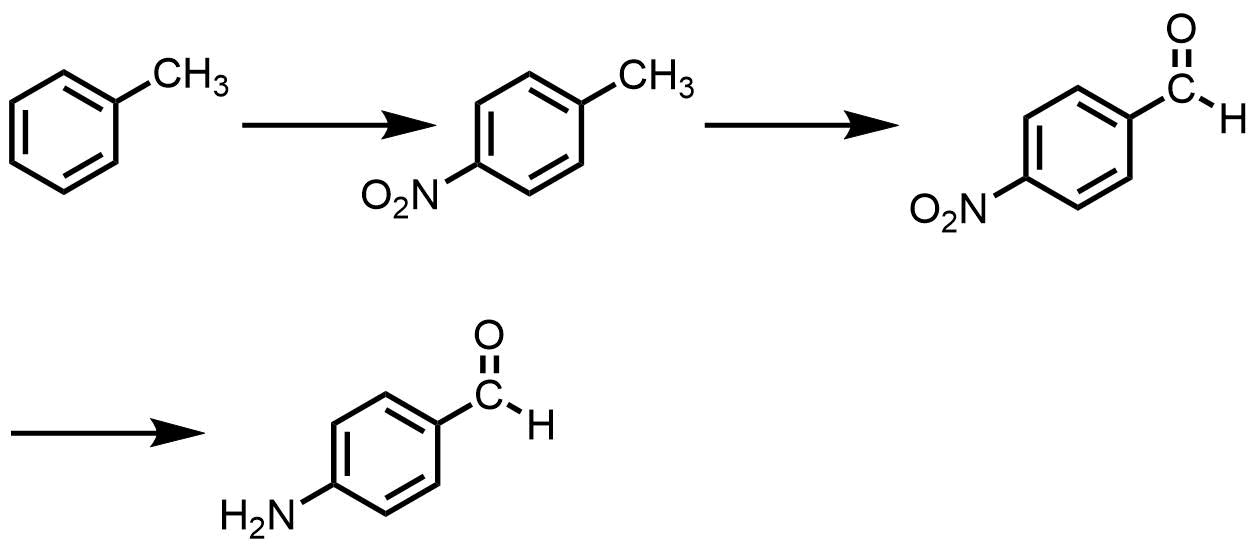
合成例 トルエンからp位をニトロ化して、メチル基を酸化してアルデヒドとしたあとニトロ基を還元してアミンにする