希ガスは化学的に安定な物質の象徴
希ガスは周期表の一番右側にある第18族元素で化学的に安定な特徴を持つ単原子ガスです。
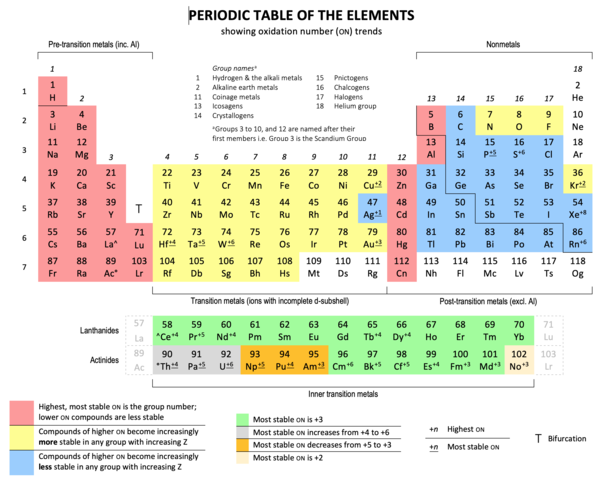
Sandbh [CC BY-SA 4.0 (https://creativecommons.org/licenses/by-sa/4.0)]
希ガスの特徴をまとめてみました
- 化学的に不活性→他の元素と化合物を作りにくい
- 無色・無味・無臭
- 閉殻
- 単原子ガス
Arは不活性ガスとして電球内に封入したり、実験室ではフラスコ内の空気を置換して酸素や水蒸気に敏感な化合物から保護するのに用いられます。
原子のサイズが大きくなると正電荷をもつ原子核との距離が離れることにより電子が受けるクーロン力が減少して電子が原子から離れやすくなります。画像のように周期が大きくなるほどイオン化エネルギーが低下しています。
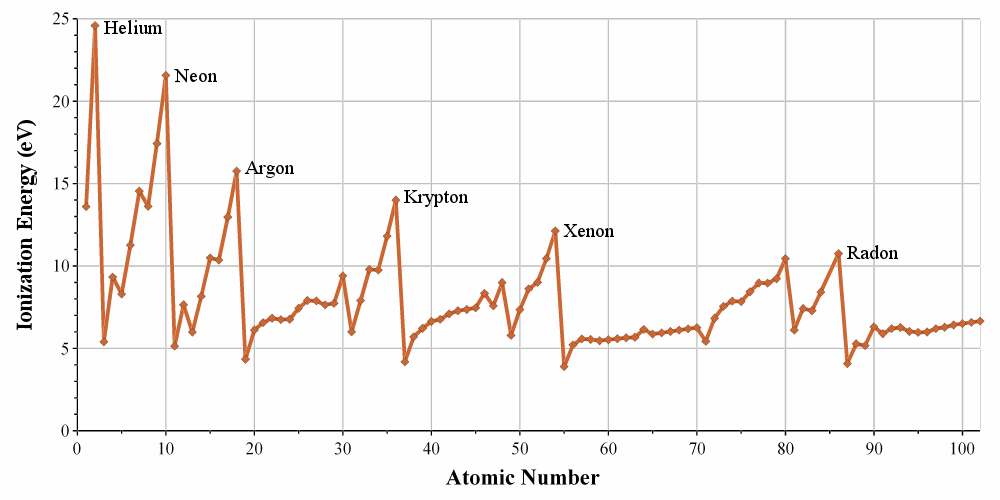
RJHall, Public domain, via Wikimedia Commons public domain
キセノンはフッ化キセノンなどいくつかの元素と化合物を作ることが知られています。
より軽い希ガスも化合物の生成が確認されていますが、イオン化エネルギーが高いため不安定です。
希ガスが安定な理由
希ガスが化学的に安定なのは電子が原子から離れにくい状態になっているからです。
電子が原子から離れないは原子核の核電荷が電子を引き寄せているからです。
イオン化エネルギーの表を見ると希ガスのNeやHeと比べてLiやNaのイオン化エネルギーが極端に小さくなっているのがわかります。
これは希ガスと比べて、LiやNaの最外殻電子が受ける核電荷が減少しているから電子原子核から離れやすくなっていると考えられます。
これは遮蔽効果で説明することができます。
電子殻がうまった状態(閉殻)になると原子核の電荷が遮蔽されて外側にある電子が感じる核電荷が小さくなります。
原子軌道と遮蔽効果
原子核を球状の、電子を砂鉄のように考えてみます。
磁石に砂鉄は無限に引っ付くわけではなく、磁石から離れた位置についている砂鉄ほど剥がしやすいはずです。これは原子核から離れた電子ほど離れやすいというのと近いですね。
砂鉄と違って電子は負電荷を持っており、同じ負電荷同士は反発するためもっとくっつにくいでしょう。
とはいえ、実際の原子をみてみるともっと複雑です。
なぜなら電子がいると思われる位置は離散的(飛び飛び)であることが実験的にわかっているからです。
これはまるで太陽の周りを惑星が特定の軌道上を公転しているのに近いですが、電荷を持った電子が原子核の引力に引っ張られながら円運動をしているモデルではいつかエネルギーを失って原子核に落下してしまうはずですが、これもまた原子が安定に存在している事実と反しています。
そこで、電子には粒子としてではなく波動としての性質も持つという考え方が導入されました。