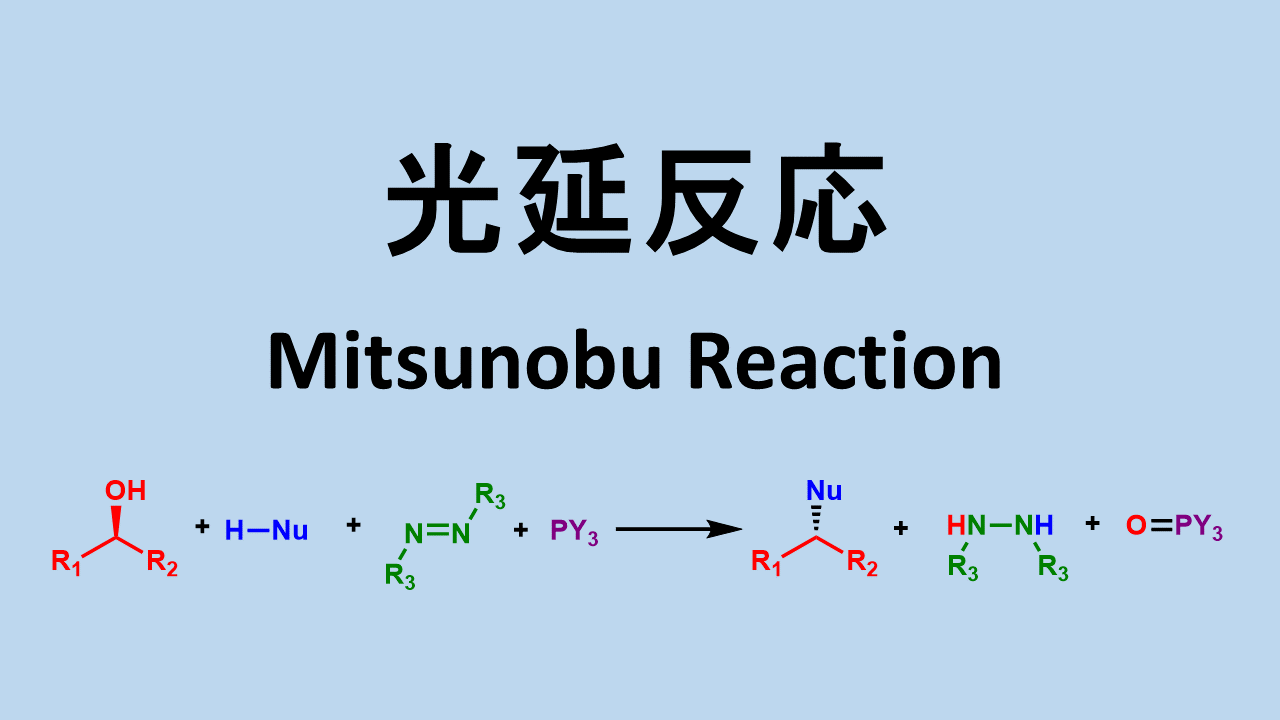
光延反応はアルコールの脱離能を上げてカルボキシラートによる求核置換反応によりエステル化を行う方法です。
光延反応では様々な求核剤を利用できますが、本記事ではカルボキシラートを求核剤としてエステル化反応に注目して紹介します。
光延反応を使ったエステル化
カルボキシラートを求核剤とした光延反応ではアルコールからエステルを作ることができます。
ハロゲン化アルキルとカルボン酸との反応と基本原理は同じです。
光延反応ではDEADとトリフェニルホスフィンにより、アルコールを脱離能の高いアルコキシトリフェニルホスホニウム塩に変換します。
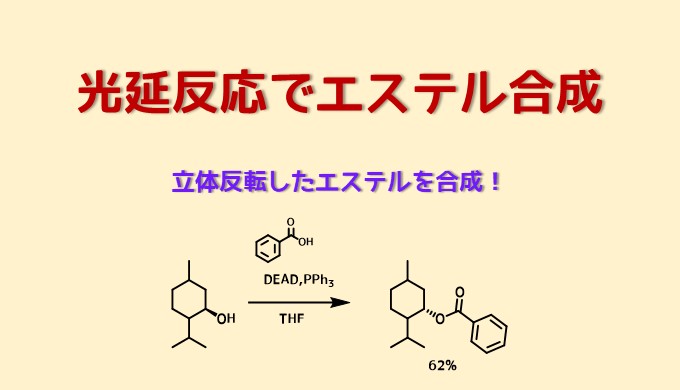
光延反応を使ったエステル化のメリットはキラルな第二級アルコールを立体反転を伴ったエステル化できることです(エステルを加水分解すればアルコールを立体反転できる)
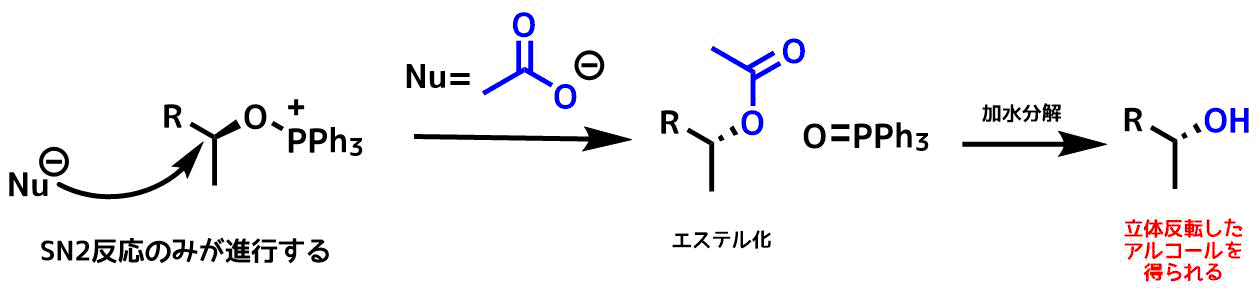
他のエステル化と比べたメリットとしては
- アルコール→脱離基に変換→エステル化を1段階で可能
- 中性・室温という穏やかな条件
- 第二級キラルアルコールは立体反転したエステルが得られる
があります。
アルコールをハロゲン化アルキルわざわざ変換しなくても位置段階で脱離基にでき、そのまま置換反応が進行します。
欠点は
- 副生成物(トリフェニルホスフィンオキシド)の除去が面倒
- 第三級アルコールのエステル化は基本的に進行しない
などがあります。
収率も中程度となることも多い印象があります。
単純なエステルやアキラルなアルコールであれば他のエステル化法(カルボン酸側の活性化法等)を使ったほうが良い結果が得られる気がします。
反応条件
第二級アルコールとカルボン酸の反応では立体反転したエステルが得られます。
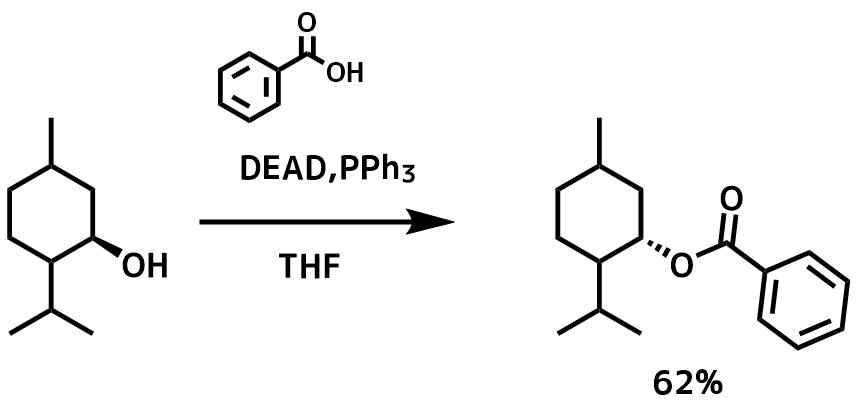
光延反応でエステル化反応例1, Samia Guezane Lakoud, et al, Arabian Journal of Chemistry, 9, 2016, S889-S892
0°Cの窒素雰囲気下アルコール(1.0当量)を脱水THFに溶かしたカルボン酸(1.1当量)およびトリフェニルホスフィン(1.1当量)の溶液に滴下して加え、溶液にアゾジカルボン酸ジエチル(1.1当量)を滴下して加えたら、室温に戻して撹拌した。反応後濃縮、クルードをカラム精製して目的物を得た。
収率はあまり高くありませんが、立体反転したものが得られています。光延反応によるエステル化は立体障害にあまり強くないです。
最新の論文:ニトロソベンゼンをアゾ試薬の代わりに使用する光延反応
アゾ試薬は毒性と試薬の安定性、爆発性などの危険性などの問題があります。これの代替としてニトロソベンゼンが利用可能であるという論文がACS Omegaに2019年に報告されました。
Pokluda, Adam, et al. “Nitrosobenzene: Reagent for the Mitsunobu Esterification Reaction.” ACS Omega 4.3 (2019): 5012-5018.
カルボン酸の酸性度と光延反応によるエステル化の収率の関係
4-ニトロ安息香酸やクロロ酢酸など、カルボン酸の酸性度が高いほうが光延反応によるエステル化の収率が高いことが知られています。
一方でアゾ試薬とトリフェニルホスフィンからなるホスホニウム塩中間体対してカルボン酸がアルコールに変わって攻撃するとアゾ試薬の窒素がアシル化される副反応が起きます。
この反応はカルボン酸の酸性度が低いほど起きやすいため、酸性度の高いニトロ安息香酸などが収率が高い原因の一つであると報告されています。
酢酸などの脂肪族カルボン酸はアゾ試薬をアシル化しやすいことが光延反応での脂肪族カルボン酸のエステル化収率が低くあまり利用されていない原因であると考えられます。
Hughes, David L., and Robert A. Reamer. “The effect of acid strength on the Mitsunobu esterification reaction: carboxyl vs hydroxyl reactivity.” The Journal of organic chemistry 61.9 (1996): 2967-2971.
4,4′-アゾピリジンをアゾ試薬として利用したエステル化
アゾピリジンは除去が容易であり、高収率で光延反応によるエステル化を行うことが報告されました。
Iranpoor, Nasser, et al. “Easily prepared azopyridines as potent and recyclable reagents for facile esterification reactions. An efficient modified Mitsunobu reaction.” The Journal of organic chemistry 73.13 (2008): 4882-4887.
アゾピリジンを使った光延条件でのエステル化は脂肪族アルコール、チオール、フェノールで進行します。
この報告での検討は芳香族カルボン酸が中心ですが、脂肪族カルボン酸とベンジルアルコールとで高収率で反応が進行しています。
この方法でも立体障害により収率は低下しますが、第二級アルコールで中程度の収率でエステル化できています。
アゾピリジンはsigma-ardrichで販売されていますが、自分で簡単に調製することも可能です。
基本反応条件
アゾピリジン(1.2mmol), カルボン酸(1mmol)、アセトニトリル(3mL)にPPh3(1.2mmol)とアルコール(1.3mmol)のアセトニトリル溶液を加えて数時間還流した後、ヒドラジンを濾過除去、濃縮してカラム精製で目的物を得た。