HSAB則は無機化学を学ぶ上で重要な概念の一つで、「ルイス酸(金属カチオン等)とルイス塩基(ハロゲン等)の間の錯形成のしやすさの分類に関する規則性」で、例えばFe3+はCN–とよりもCl–のほうが錯形成しやすいです。これには規則性があり、各イオンの性質を捉えることによって、どのイオンの間で錯形成しやすいかを予測することができます。
HSAB則とは?
HSAB則は「Hard and Soft Acids and Bases」の略で酸と塩基(ルイス酸・塩基)は各々、
- 硬い
- 軟らかい
- その中間
に分類することができ、硬い酸と塩基同士、軟らかい酸、塩基同士で錯形成しやすい(錯体が安定)という傾向がHSAB則です。この考え方はR.G.Pearson(ピアソン)という人によって生まれました。では一体、硬いと軟らかいは一体どんな違いがあるのでしょうか?
HSAB則における硬さと軟らかさとは?
HSAB則における硬いと軟らかいとは、
- 硬い:原子半径が小さく、分極しにくい分子(イオン)、価数の大きい金属など
- 軟らかい:原子半径が大きく、分極しやすい分子(イオン)
という傾向があります。原子半径が大きい分子は最外殻電子が原子核よりも遠いので分極しやすい傾向があります。
HSAB則による分類
| 硬い | 中間 | 軟らかい | |
|---|---|---|---|
| 酸 | H+,Li+,Na+,K+,Be2+,Mg2+,Ca2+,Al2+,Cr2+,Co2+,Fe3+,La3+,Ti3+,BF33+,B(OH)33+,Si4+,SO3,BF3,AlMe3 | Fe2+,Co2+,Ni2+,Cu2+,Zn2+,Pb2+,Sn2+,Sb3+,Bi3+,Ru+,Os2+,Rh3+,Ir3+,NO+,SO2, BBr3, | Cu+,Ag+,Au+,Tl+,Pd2+,Cd2+,Pt2+,Hg2+,BH3,Br2 |
| 塩基 | NH3,H2O,R2O,OH-,F-,Cl-,ClO4-,NO3-,RO-,AcO-,SO42-,PO43-,NO3-,RNH2, | N2,NO2-,N3-,Br-,Pyridine,SO32-, | H-,CN-,R-,I-,SCN-,R2S,RSH,RS-,R3P,R3As,RNC,CO,C2H4,Benzene |
ハードとソフトはどう覚える?
どれがハードな酸、塩基でどれがソフトな酸と塩基なのか、中間はどれかを覚えるのは結構大変です。ですから各分類のものの代表を覚えておくと良いです。
ハードな酸はプロトンやアルカリ、アルカリ土類金属などのイオンや価数の大きい遷移金属のイオンなどです。中間の酸は覚えにくいですが、原子番号順でFe Co Ni Cu Zn(てこにどあ)の二価イオン、軟らかい酸は11族(銅、金、銀)の一価イオン、白金、カドミウム、パラジウム大きい元素のイオンです。
塩基も同様に電気陰性度の高い元素(F,O,N,Cl)のイオンや分子は硬く、中間はBrなど、軟らかい塩基はリンや硫黄、炭素系(ニトリルやエチレンなど)、ヨウ素やヒ素などの大きい元素などが当てはまります。
塩類を見た時に安定な錯体かどうかを考えると自然と覚えていくと思います。有名な有機金属錯体のPd(PPh3)4は軟らかい酸のPdと軟らかい塩基のリンが結合しているから安定?というように考えると良いかも?
硬いと軟らかいの違いは?
軟らかいものは原子番号が後ろのほうの元素でd軌道が電子をみたされている元素は分極しやすく軟らかいです。逆に原子番号が若い元素は硬いです。
HSAB則は反応位置予測に役立つ!
有機合成でもHSAB則を知っていると役立つ場面があります。
それは複数の反応点があるとき、どの位置で反応が起こるのか?を予想できることです。
有機化学反応においては金属以外の物質の硬い・軟らかいを把握しておきましょう。
- 硬い酸:二酸化炭素、トリアルキルシリル基、プロトン、BF3
- 硬い塩基:アミン、アミドイオン、アルコール、アルコキシド、カルボキシレート、水
- 軟らかい酸:ボラン、カルベン、臭素、
- 軟らかい塩基:ヒドリド、BH4–、カルバニオン、アルケン、ホスフィン、チオール、ヨウ化物イオン、有機銅試薬、有機亜鉛試薬
エノンは反応性の高い分子でカルボニル炭素とβ位が求電子的になっています。つまり、求核剤にとって2つの反応部位があります。
エノンにグリニャール試薬を使用した時どちらが反応するでしょうか?グリニャール試薬は硬い塩基カルボニル炭素は硬い酸です。したがってグリニャール試薬はカルボニル炭素を攻撃します。一方で、ギルマン試薬などの有機銅試薬は軟らかい分子でカルボニル炭素よりも軟らかいβ位の二重結合を攻撃します。
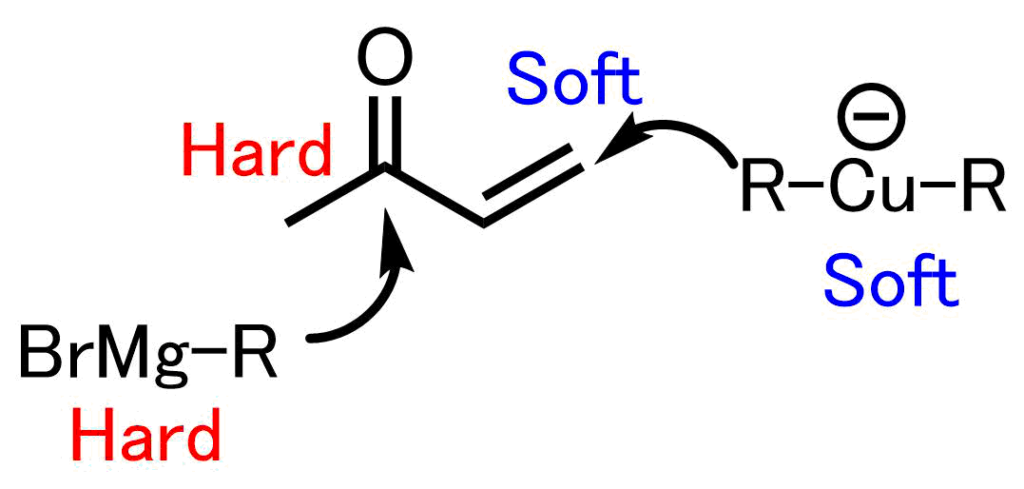
エノンに対する反応選択性
このように分子の硬い・軟らかいを知っていれば反応の予測が可能になります。
アルキル化剤もハードとソフトがあります。
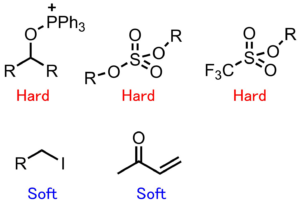
硬い求電子剤と柔らかい求電子剤
アミドのアルキル化を行うことを考えてみると、ヨウ化アルキルのような軟らかい求電子剤を使うと軟らかい窒素のほうを優先的にアルキル化します。一方で、ジメチル硫酸のような硬い求電子剤を用いると硬い酸素原子をアルキル化しやすいです。
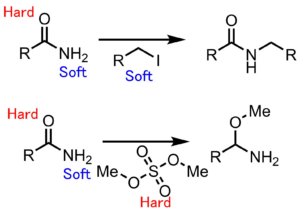
アミドのアルキル化選択性硬い酸素と軟らかい窒素
このように硬い軟らかいを考えることで選択性を与えることができます。
ウィリアムソンエーテル合成ではハロゲン化アルキル(R-Br、R-I)と求核剤(R-O–)との反応によって、エーテル(R-O-R’)を合成します。
例えば、ベンジルブロミド(BnBr)とアルコール(R-OH)の反応では酸化銀(I)を加えることがあります。酸化銀の銀イオンは軟らかい元素で、硬い酸素よりも軟らかいヨウ素や臭素の方と反応しやすく、更に生成したハロゲン化銀は溶媒への溶解度が小さく沈殿します。つまり、酸化銀を加えることにより、ハロゲンと反応しやすい酸化銀がBnBrを活性化することによって反応が進行しやすくなります。