有機合成化学でよく使用するDMFは沸点が高く、除去しにくいために、NMRに混入しやすい非プロトン性極性溶媒です。DMFは溶解力が強く、極性が高いものから低いものまでよく溶かします。そんな有用なDMFの基本的な情報から除去方法、NMRスペクトルなどを紹介します。
DMFの特徴・沸点など
DMFはN,N’-dimethyl formamide(N,N’-ジメチルホルムアミド)という名前の有機化合物で、ギ酸とジメチルアミンが縮合してできたアミドです。
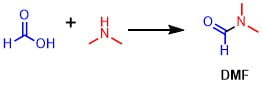
アミド結合は比較的安定な結合であり、求核剤や求電子剤と反応しにくいため有機溶媒として利用されています。メタノールのようにプロトンを放出する水酸基などを持っていないですが、カルボニル基を持つため分極していて高極性です。そのため非プロトン性極性溶媒と呼ばれています。
- 分子式 C3H7NO
- 分子量 73.1
- 沸点 153℃
- 融点 -61℃
- 比重 0.944
- CAS番号 68-12-2
- 価格: 500 mL 2400 円(TCI)
DMFが反応してしまう例
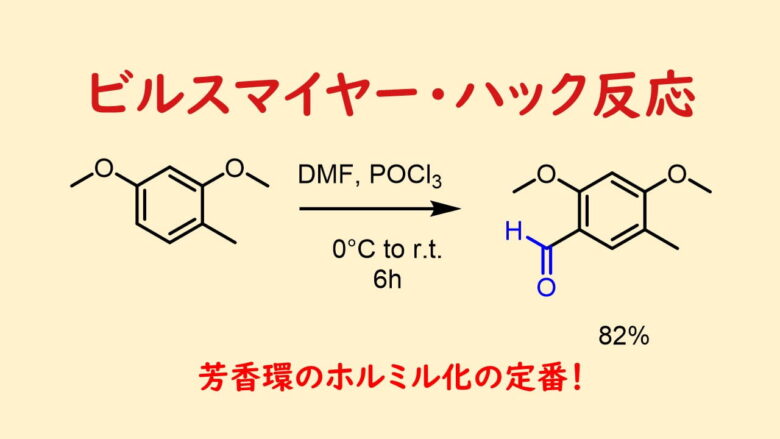
DMFは多くの反応条件下では安定ですが、反応を起こすこともあります。DMFの蒸留は常圧で沸騰させると少しずつ分解していきます。DMFが反応してしまう例としてはビルスマイヤー・ハック反応があります。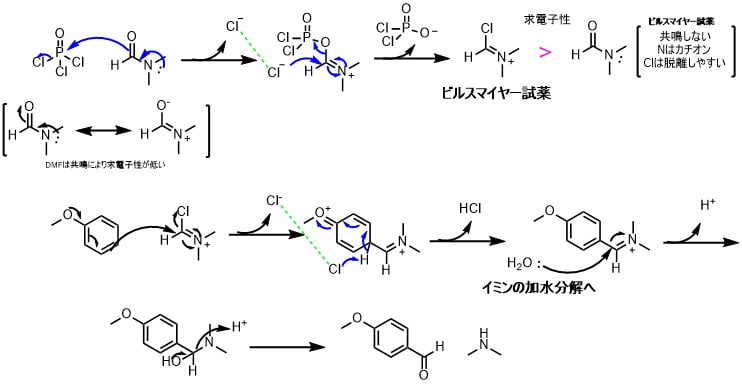
ビルスマイヤー・ハック反応は塩化ホスホリルとDMFが反応することによって生成するビルスマイヤー試薬によって進行します。DMFはアミドの窒素と酸素間の共鳴から求核剤に対しては不活性な溶媒とされていますが、酸素上の求核性は高くなっており、塩化ホスホリルのような優れた求電子剤とは反応します。
DMFの蒸留・精製方法
DMFは割と分解しやすい化合物です。塩基や酸存在下で常温でも分解していきます。また、高温で分解するので、減圧蒸留します。
DMFの脱水はCaH2で脱水も可能ですが、硫酸マグネシウムやモレキュラーシーブで乾燥後に減圧蒸留(70℃~80℃)で精製します。
- 蒸留したいDMFに硫酸マグネシウムあるいは活性化モレキュラーシーブを加えて一晩静置させます。
- 減圧して溶液を70℃~80℃に温めて減圧蒸留します。
- 初留は除去し、本留をとります。蒸留は蒸留容器が空になるまえにストップします。
- 活性化モレキュラーシーブス4Aが入った保存容器に入れて保存します。
DMFのNMRスペクトル
DMFは溶媒としてよく利用し、沸点も高いことからNMRスペクトル中に混入しやすい溶媒の一つです。DMFはホルミル基の水素が9ppm付近と、ジメチルの3Hが2本ピークとしてでてきます。下にはH-NMRの予測スペクトルを載せました。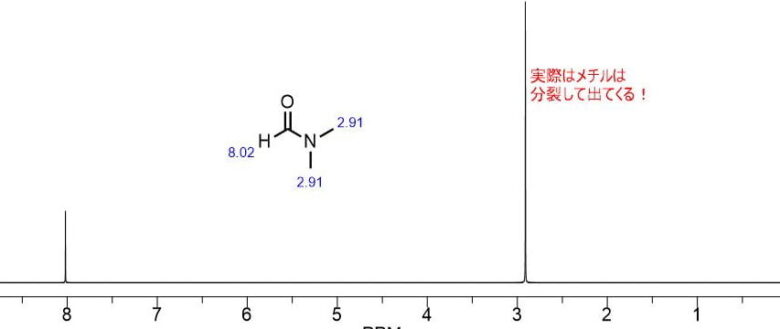
メチル基は予測では重なって表示されていますが、実際は分裂してでてきます。
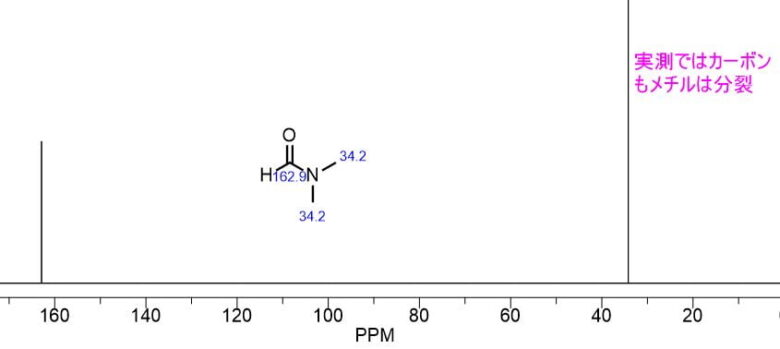 13Cでも同様にメチル基は分裂してでてきます。
13Cでも同様にメチル基は分裂してでてきます。
実測のNMRについてはAISTのSDBSで確認してみてください
DMFの除去方法
DMFは沸点が高い溶媒なので除去が難しい場合があります。DMFの除去方法としては
- 留去する(熱を60℃くらいかければエバポレーターでも飛ばせる)
- 分液する(目的物が水溶性でなければ水を多めにいれて有機溶媒で抽出する)
- 共沸除去する(トルエンやベンゼンを使って共沸除去するそれほど熱をかけなくても飛ばせる50℃くらい?)
などの方法があります。スケールが大きいときは分液するのは一苦労なので留去するのが良いと思います。逆にスケールが小さいときは有機溶媒で抽出できれば分液をやるのが手っ取り早いです。DMFを使うときは極性の高い化合物であることが多いと思うので、分液ができなければ油圧ポンプなど強力なポンプで引いて除去しましょう。熱をかけにくいのであればトルエンやヘプタンを加えて共沸させると除去しやすいかもしれません。