生物学的等価体(bioisostere)を知っていれば知っているほど医薬品候補化合物の構造活性の検討に有用です。
そこで今回はアミド結合の生物学的等価体についてまとめてみます。
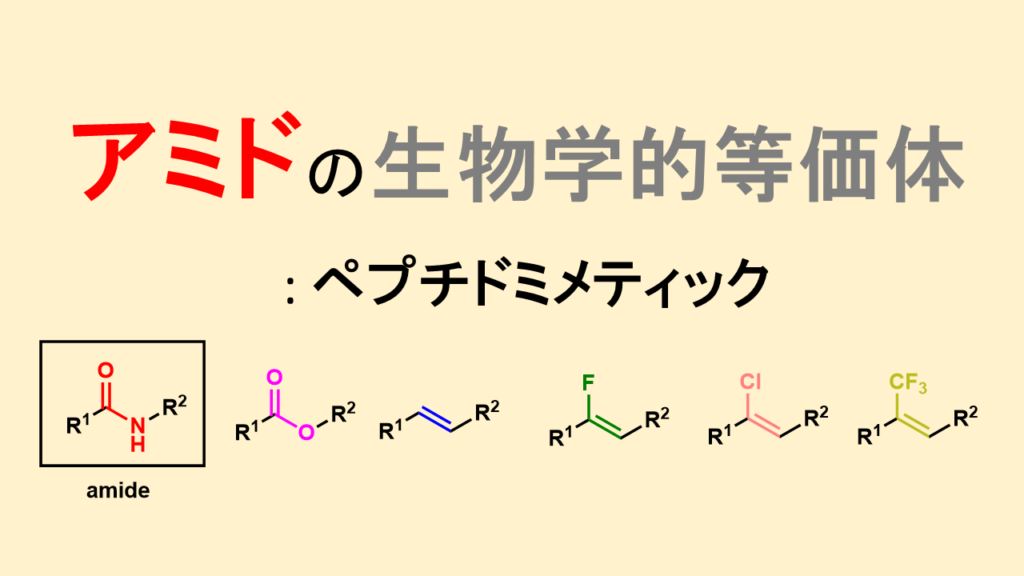
アミドの生物学的等価体について
アミド結合は化学式R1-C(=O)-NH-R2で表される有機リンカーであり、生体内でもタンパク質あるいはペプチドのリンカーとして豊富に存在しています。アミド結合の中でもタンパク質あるいはペプチドを構成するようなα-アミノ酸を繋げるものは、ペプチド結合と呼ばれます。
また、このペプチド結合を模倣した生物学的等価体についてはペプチド等価体(ペプチドミメティック)と呼ばれます。ペプチドミメティックは大きく分けて、ペプチド結合の基底状態に基づいてデザインされた基底状態模倣型ミメティック(ground state mimetic)と酵素と基質の遷移状態に基づいてデザインされた遷移状態模倣型ミメティック(transition state mimetic)の二つがあります。1)
アルケン型イソスター
アミド結合は二重結合性を有していることから、同様に二重結合の代表であるアルケンはアミドの生物学的等価体になりえます。アルケン型のイソスターとしては単純な(E)-アルケン以外にもメチルアルケン型、フルオロアルケン型、クロロアルケン、トリフルオロメチルアルケンなど種々のイソスターがあります。その中でも特にフルオロアルケン型はその中でもペプチド結合をフルオロオレフィンに置換したフルオロアルケン型は、全原子中で最大の電気陰性度を有するフッ素原子の存在により、他の等価体に比べ静電的相同性が高いことや、
フッ素原子のファンデルワールス半径が酸素原子とほぼ同程度で構造的相同性も高いことから天然のペプチドを模倣するのに適したイソスターとして考えられています。
エステル
トリアゾール
オキセタン
参考文献
[生化学 第82巻 第6号,pp.515―523,2010]
http://www.jbsoc.or.jp/seika/wp-content/uploads/2013/10/82-06-08.pdf
https://pubs.acs.org/doi/pdfplus/10.1021/jo981057v