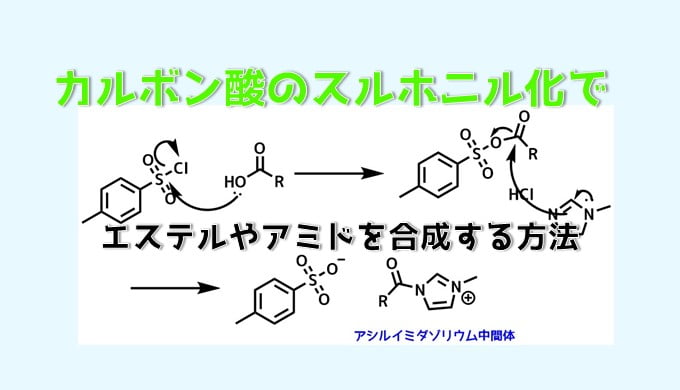
スルホニル化を経た縮合反応
縮合剤はカルボン酸を活性化させることによってアルコール及びアミンと脱水縮合反応を起こさせる試薬のことです。
特にアミド化はペプチド合成において重要であるため、たくさんの縮合剤が開発されてきました。
代表的な縮合剤は
- カルボジイミド系(DCC、EDCI)
- CDI
- 山口法(山口ラクトン法)
- 向山法
- BOP試薬
- DPC法
- DPTC法
- MNBA法
- BBDI法
- 光延反応
などがあります。第3級アルコールを立体反転させてエステル化できるPH2PClおよび2,6ジメチル-1,4-ベンゾキノンもあります。
中性の縮合剤
向山法、コーリー・向山法(2-PyS)2/PPh3)、正宗法(Hg-(O2CCF3)2), 光延反応、山口法、Hannessian法(Bu2SnO)、Keck法(DCC/DMAP)、椎名法(DCC,MNBA/TEA/DMAP)が確立している。
Me2NSO2Clを用いたカルボン酸活性化法
Me2NSO2Clはアルコール共存下でカルボン酸選択的に反応して無水物をつくります。
安価なメシルクロライドでも同じように反応は進行しますが、メチルの水素が脱離したスルフェンの発生のため、メシルクロライドを多めに加える必要があり、副反応が進行しやすい欠点があるので、Me2NSO2Clがのほうが良いです。
Me2NSO2Clの特徴はα,β不飽和カルボン酸の縮合が異性化せずに進行することです。
生成した活性カルボン酸はエステル・アミド化ともに進行します。アミド化ではDMAPを加える必要があります。
TsCl / N-メチルイミダゾール法
Me2NSO2Clを使った反応よりも一般的なスルホニルクロライドであるトシルクロライドを用いたカルボン酸の活性化方法も有用です。
N-メチルイミダゾール法は反応性が高く、安価であるという特徴があります。チオエステル化も進行します。
アミド化はMe2NSO2Clと比べて高収率で進行します。第三級アルコールはエステル化しないです。
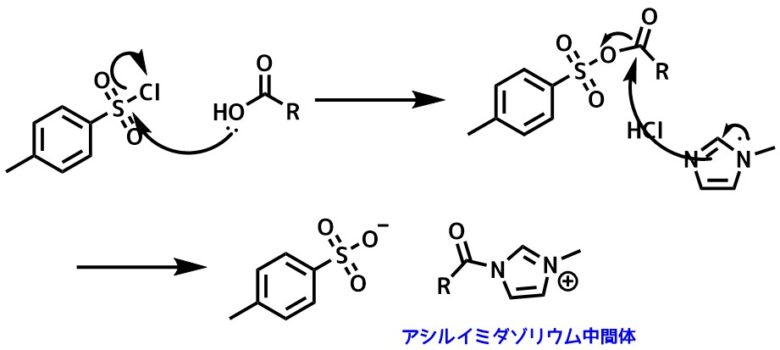
TsCl_イミダゾール中間体
1)田辺陽, et al. “エステル化・スルホニル化・アミド化・シリル化: 汎用反応の実用的合理化.” 有機合成化学協会誌 62.12 (2004): 1249-1259.