メチルエステルやエチルエステルはカルボン酸の保護基あるいは、アルコール及びアルデヒド合成の中間体として利用される重要な分子です。
他のエステル合成とは多少向いている反応が違うためこの記事ではメチルエステルやエチルエステルに着目してその特性や合成方法をまとめます。
メチル・エチルエステルの用途(保護・中間体)
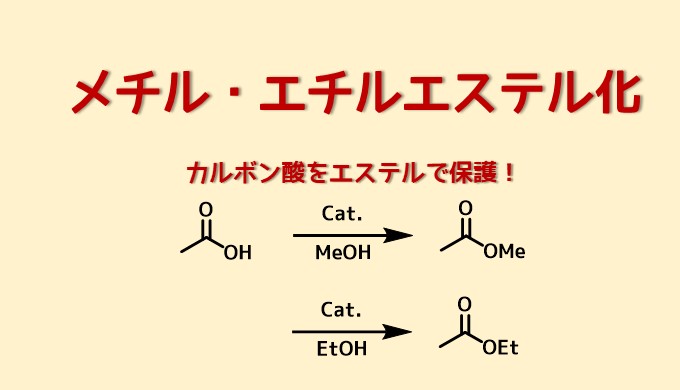
カルボン酸は極性が高く、酸性のため精製が困難になったり、副反応を起こすことがあるため、メチルエステルやエチルエステルとして保護する事が多いです。
メチルエステルは大きく極性を低下させ、塩基性・ヒドリド還元条件以外では比較的安定であり、脱保護も容易であるため一時的な保護に有効です。
また、カルボン酸を還元すればアルデヒド、アルコールを得ることが可能ですが、エステルを還元したほうがキレイに反応が進行するので中間体として良く利用されています。
メチルエステルとエチルエステルは基本的に同じなのでこれ以降はメチルエステルと表記しています。
メチルエステル合成は他のエステル合成とは違う?
どちらもエステル合成なので基本は同じですが、単純アルコールは安価であるため、大量使用できる点が異なります。
そのため、一般的なエステル合成でよく利用されるDCC / DMAPなどはあまり使いません。
メチルエステル化は複雑な分子にも使うことが多く、副反応の少ない合成方法も検討されています。
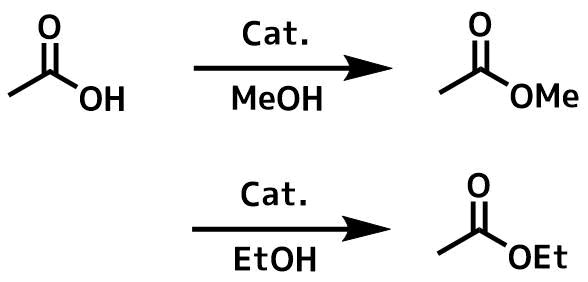
もちろん酸に安定な原料合成には単純なフィッシャーエステル化(硫酸/アルコール)でOKです。
メチルエステルの合成方法
比較的単純な脂肪族や芳香族のカルボン酸
エステルやアミド(特にアセチル基)やアルキン・アルケンなど分解しやすい構造を持たない化合物であれば古典的なフィッシャーエステル化でOKです。アルコール中に触媒量の硫酸(1~2%MeOH重量)を滴下して加えて還流するだけです。
そのまま蒸留するか、分液すればエステル化が得られます。

陽イオン交換樹脂を酸触媒として利用
Amberlist-15やDowexなどの陽イオン交換樹脂は固相表面にスルホン酸が修飾してあり、酸性を示します。
濾過によって簡単に除去できるので、陽イオン交換樹脂+アルコールで加熱することでエステル化が達成できます。
塩酸や硫酸を用いるよりも簡便で安全な方法です。ラセミ化、エピメリ化
この方法はメチルエステル以外のエステル化にも利用できます。
実験手順
溶媒量のメタノールをカルボン酸に加えて溶けるなら溶かしてから陽イオン交換樹脂を適量(カルボン酸重量の1/10くらい?反応の様子を見て足してく)加えて穏やかに撹拌します。反応後は濾過して濃縮します。
イオン交換樹脂は再利用可能です。活性化しなくても50回くらい使えるようです。
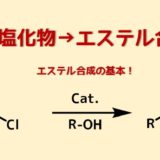
HCl-MeOHを利用する
塩酸(HCl-H2O)をアルコールに加えるよりもHClガスをメタノールに溶かしたほうが水が混入しないため、反応効率や副反応の面で有利です。さらにHCl-MeOHは反応性が高く低温でもエステル化が進行します。
HCl-MeOHは販売されていますが、自分で調製することも可能です。
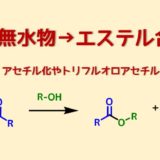
変法として、塩化チオニル、塩化アセチルなどのHCl源をメタノールと反応させる事によって、発生した塩化水素がアルコール溶液にそのまま溶け込むので、HCl-MeOHを簡単に調製できます。(MeOHの5-10%程度)
TMSCl法はカルボン酸に対して2-4当量のTMSClを滴下して加えた後、メタノールを滴下して加えて室温で撹拌します。
Jiabo Li and Yaowu sha, Molecules 2008, 13, 1111-1119
反応はカルボン酸に対してHCl-MeOHを適当量加えて撹拌するだけです(0℃→rt)
通常脱水剤は不要で、還流もいらないことが多いです。加熱すると副反応が起こる場合、長時間反応(7daysとか)をすることがあります。(HClも飛んでくため)
長鎖脂肪酸など立体障害で反応性が低いカルボン酸
一般的には末端の反応点に対してアルキル鎖が長くなるほど反応性が低下します。
脂肪酸にも同じことが言えます。HCl-MeOHはよく使われますが、不飽和脂肪酸などアルケンがある場合付加反応を起こすことがあるため塩酸を避けたいところです。
長鎖脂肪酸にはBF3がよく使われるようです。BF3をメタノールの10%程度加えます。長鎖脂肪酸の場合は溶解させるためにベンゼンやトルエンなどを加えることがあります。
実験方法
25mgのカルボン酸に10%BF3-MeOHを2mL加えて(脱水剤としてDMPを加えても良い)を室温または、60℃で10分ほど加熱し、濃縮、あるいは水を加えて分液してエステルを得る。
ジアゾメタンを利用する
ジアゾメタンは強力なメチル化剤です。ジアゾ基は窒素分子の生成を伴うため非常に良い脱離基です。
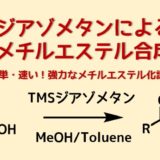
ジアゾメタンによるメチルエステル化は中性条件で進行し、早く、選択性が高いです。
一方で、ジアゾメタンの毒性と爆発性の問題があります。現在は爆発性がなく、毒性も低い代替品であるTMSジアゾメタンを用いることが多いです。
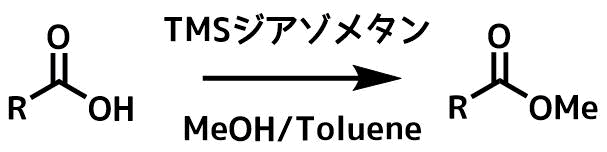
TMSCHN2(TMSジアゾメタン)は少々高価ですが市販されており、分析のための誘導体化試薬としても利用されている信頼性の高い試薬です。
反応は数時間以内に完結することが多く、立体障害の大きいカルボン酸にも有効です。反応後は濃縮するだけでエステルが得られる事が多いおすすめの試薬です。
欠点は高価であることから大スケールに使いにくい点です。酸に弱い基質、貴重な原料、他のメチルエステル化が進行しないといったときに試す価値のある方法です。