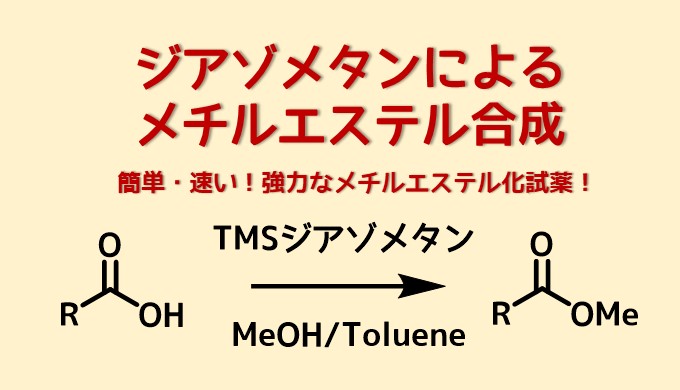
ジアゾメタンはカルボン酸と反応してメチルエステルを生成します。この反応は中性条件下素早くメチルエステルに変換可能なため、最も有用なメチルエステル化法ともいます。致命的な欠点はジアゾメタンの爆発性・毒性です。
本記事ではジアゾメタンを使ったメチルエステル合成法を紹介します。
ジアゾメタンを使ったエステル化の特徴
ジアゾメタンはその名前の通りにメチルエステルのみ合成可能です。ジアゾ基は最も強力な脱離基であり、立体障害も少ないです。
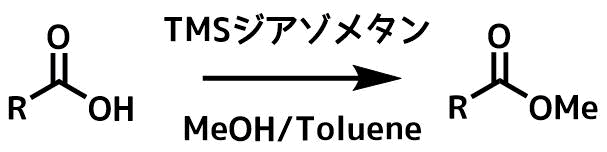
ジアゾメタンの特徴はその反応性の高さと中性条件で進行することです。
酸に不安定な分子はフィッシャーエステル化などは使いにくいですが、ジアゾメタンであれば中性条件下素早く定量的にメチルエステルに変換できます。
他の方法では立体障害やて反応性のため上手く進行しないメチルエステル化もジアゾメタンを使うと進行する可能性があります。
欠点は爆発性と毒性です。
まんまのジアゾメタンは爆発性が高く、高濃度になると危険です。通常はジアゾメタン発生試薬から気体のジアゾメタンを発生させてエーテル中に溶解させた溶液を用います。
近年はジアゾメタンの危険性を減らしたTMSジアゾメタンが開発されています。
TMSジアゾメタンが有用な代替試薬
ジアゾメタンは前駆体から発生した気体のジアゾメタンをエーテルに溶かしこんで利用していましたが、ジアゾメタン、前駆体両方の毒性や爆発性が問題でした。
TMSジアゾメタンの利点は
- 熱安定性が高く爆発性も無い
- 発がん性などの毒性は無い
- ジアゾメタンと同等の反応性
- エステル化の条件ではオレフィン、水酸基、ケトンは反応しない
が挙げられます。
欠点は
- 高価(TMSCHN2 1050円/1mmol, diazald[前駆体]35.8円/1mmol :TCI)
- メタノールを加える必要がある
- アミノ基は保護しないと収率が低下する
が挙げられます。
一方でTMSジアゾメタンは爆発性がなく、熱安定性が高く、発がん性も無い安全性の高い試薬でありながら従来のジアゾメタンと同等の反応性をもつことから、ジアゾメタンの有用な代替試薬として利用されています。
TMSジアゾメタンを使ったメチルエステル化はメタノール溶媒中TMSジアゾメタンをカルボン酸と反応させることによって達成されます。
TMSジアゾメタンによる反応ではメタノールを加える必要があります。溶媒としては他の溶媒を利用可能です。
TMSCHN2では二重結合、フェノール・アルコール、ケトンは反応せずにカルボン酸選択的に反応します。アミノ基があると収率が低下するので、アミノ酸をメチルエステル化するときはアミンを保護したほうが良いです。
例えばL-フェニルアラニンは保護しないと収率42%程度ですが、アミンを保護すると定量的に進行します。
TMSジアゾメタンの調整法
強力なメチルエステル化試薬で大量合成にも使えるTMSジアゾメタンですが、市販品は高価なため大スケールでの利用には結局使いにくいのが最大の欠点です。
購入すると高いですが、自前で作れば少しは費用を抑えられるはずです。
TMSジアゾメタン調製に必要な材料
- DPPA 25g 6700 5g 2500円
- クロロメチルTMS 25mL 7500円
- Mg
- 1,2-ジブロモメタン(Mg活性化)
- 脱水エーテル
です。全部試薬を揃えると結構高価になるかもしれません。DPPAはアジ化ナトリウムとジフェニルホスホリルクロリドから作ることもできます。
合成法
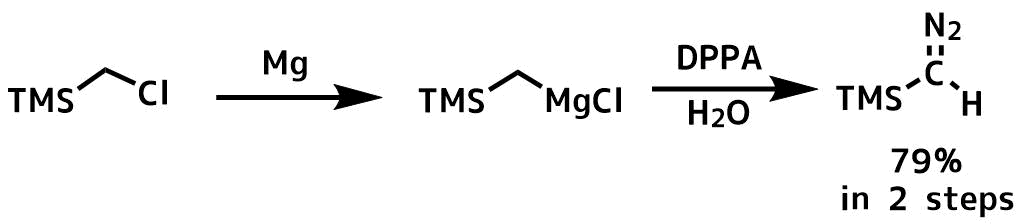
TMSジアゾメタンの調整法
グリニャール試薬の調整
マグネシウム(1.46g,60.0mmol)を20mLの脱水エーテル、20μLのジブロモメタンを加えて15分間撹拌してマグネシウムを活性化した後、クロロメチルTMS(6.13g、50.0mmol)を20mLのエーテルに希釈した溶液の1/10量を一気に加えて、撹拌して反応が始まったら残りの溶液を反応して穏やかに沸騰している状態を維持する速さで滴下して加えます。全て入れたら、40℃で還流を1hします。
TMSCHN2の合成
DPPA(12.4g、45mmol)を50mLの脱水エーテルを溶解し、NaCl-アイスバスで-10℃に冷却してから調整したグリニャール試薬を0℃を超えないように滴下します。全て加えたら0℃で2時間撹拌し、氷浴上で一晩放置します。-10℃に再度冷却して5mLの氷冷水を滴下して加えて生じた沈殿を濾過して、冷却したエーテルで何度か沈殿を洗います(濾液受けは氷浴で冷却しながら)その後、濾液を冷水で分液して、硫酸ナトリウムで脱水し、280 mMのTMSジアゾメタン-エーテル溶液を得ます(79%)。蒸留精製で1Mまで濃縮できる。また、4℃保存で6ヶ月は分解なしに保存可能。
ちゃんとできたかどうかはメチル化を行って確かめてみます。
Presser, Armin, and Antje Hüfner. “Trimethylsilyldiazomethane–a mild and efficient reagent for the methylation of carboxylic acids and alcohols in natural products.” Monatshefte für Chemie/Chemical Monthly 135.8 (2004): 1015-1022.
反応条件
1.3eq TMSCHN2, 20%MeOH-Solvent(benzen等)にカルボン酸、を加えて室温で撹拌し、濃縮すればエステルが得られます。
一般的な反応条件
カルボン酸(1mmol)に対して10mLのトルエン:メタノール(3:2)の溶液に溶解し、TMSジアゾメタン(1.1~1.5eq)を滴下して加えます。加えている間黄色のTMSジアゾメタン溶液が無色になりますが、反応溶液が黄色になるまで加えます。30~1時間室温で撹拌した後、濃縮すればメチルエステルが得られます。
反応例1
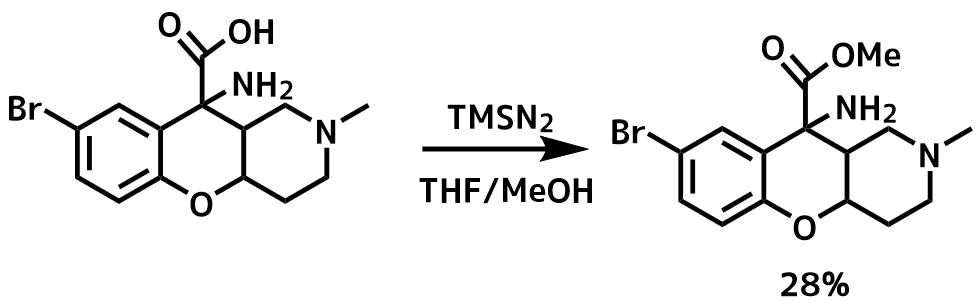
ジアゾメタンによるメチルエステル化 Hunt, Kevin W. et al patent. 2012040641, 2012
THF/MeOH(1:1)の溶液13mLにカルボン酸(1.62mmol)を溶かして、2MのTMSCHN2(13mmol)を加えて室温で12時間撹拌し、さらに8eqのTMSN2を追加して16時間撹拌し、さらに5eqのTMSCHN2を加えて19時間撹拌した。バブリングが収まるまで氷を入れたのち、濃縮し、炭酸水素ナトリウム、食塩水を加えて25%IPA/DCMで抽出し、後処理をして目的物を28%を得た。
反応が進行しにくい場合はTMSCHN2を追加します。しかし、立体障害が大きい第三級のカルボン酸はTMSCHN2を使ってもメチルエステル化が難しいです。特にこの分子はα位にアミノ基があるため収率が低下しやすいです。アミンを保護すれば収率は向上が見込めます。
アルコールは場合によってはメチルエーテル化する可能性があります。
また、嵩高いカルボン酸で反応が進行しにくい場合メチルトリメチルシリルエステル化する場合もあります。
Hueso-Falcon, et al, European Journal of Medicinal Chemistry, 46(4), 1291-1305; 2011
ピリジン環を有するニコチン酸誘導体もメチルエステル化可能です。
Patnet. 2012003544, 2012
TMSジアゾメタンはリン酸に対してもメチルエステル化できます。アミドはO-メチル化することがあります。
TMSジアゾメタンの反応機構
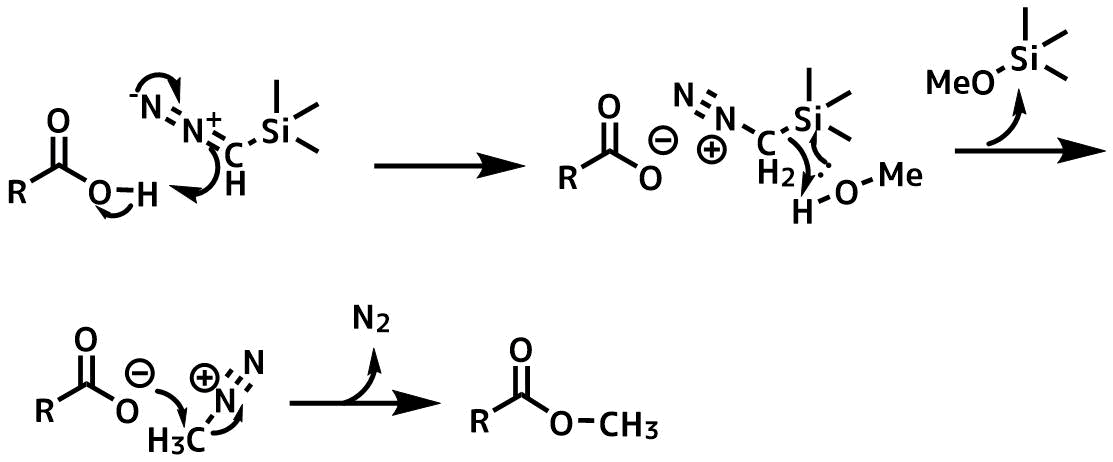
TMSジアゾメタンの反応機構
TMSジアゾメタンの機構はメタノールが関与するように欠かれています。メタノールによってジアゾメタンが発生し、それがカルボン酸と反応していると考えられています。
参考
塩入孝之, and 青山豊彦. “トリメチルシリルジアゾメタン.” 有機合成化学協会誌 44.2 (1986): 149-159.
青山豊彦, and 塩入孝之. “トリメチルシリルジアゾメタン: 危険なジアゾメタンにかわる安全な反応剤.” ファルマシア 20.8 (1984): 762-764.