芳香族アルデヒドは様々な官能基の前駆体となる重要な物質です。
芳香族アルデヒの合成法として、芳香環メチル基のC-H結合を酸化してアルデヒドを得る方法があります。
通常不活性なC-H結合ですが、ベンジル位に相当するC-H結合は比較的活性で酸化を受けることが知られています。
この記事では、これまでに報告されている芳香族メチル基の酸化によりアルデヒドを合成する方法・特徴を紹介します。
メチル基の酸化でアルデヒド合成
アルカンは様々な他の官能基と比べて安定で多くの条件下で反応を受けませんが、特定のポジションでは酸化を受けます。その一つがベンジル位です。
ベンジル位は芳香環の共鳴や電子効果による影響を受けやすいため、他の位置と比べて圧倒的に酸化を受けやすいです。
ベンジル位は実際にラジカルやアニオン、カチオンといった不安定核種が安定化されて生成しやすいことが知られています。
メチル基の酸化方法
石油中には豊富に含まれる炭化水素を利用できるため、特に工業においてメチル基の酸化は重要な反応です。
ベンズアルデヒドはトルエンを原料にコバルト触媒を使って生産されています。
今回は実験室用途で用いられる反応について紹介します。
三酸化クロム+硫酸
クロム酸は代表的な酸化剤であり、芳香環のメチル基も酸化できます。しかし、三酸化クロムは強力な酸化剤であるため、生じたアルデヒドはさらに酸化してカルボン酸に変換されてしまいます。
アルデヒドを得るには、無水酢酸を加えて生じたアルデヒドをジアセテートに変換することで酸化から保護します。ジアセテートはその後酸加水分解によってアルデヒドを得ることができます。
三酸化クロムを使用した反応例1
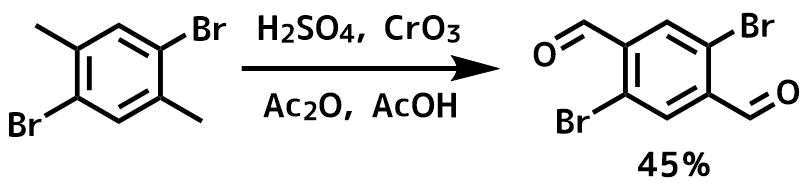
Sun, Jingwei et al Integrated Ferroelectrics, 153(1), 42-47; 2014
硫酸 (14 ml) を 酢酸 (20 ml), 無水酢酸(40 ml), 基質 (4.0 g)の溶液に0°Cで滴下して加えた。CrO3(6 g) を5回に分けて加えて混合物を0℃で5時間撹拌した。反応後、氷水をたくさん加えて生じた固体を濾過、冷メタノールで洗浄し 、アセテートの固体を硫酸 (2 ml), 水 (20 ml) エタノール(20 ml) の溶液に加えて5 h還流して加水分解し、目的物を45%の収率で得た。
クロム酸を使ったメチルの酸化は古くからのスタンダードな反応です。二酸化セレンなどの他の方法では合成が難しいオルトフタルアルデヒドやジニトロトルエンなども変換可能です。フェノール性水酸基はアセチル基などで保護する必要がある他、酸に弱い官能基は耐えないので使えないです。
エタール反応 (Etard reaction) 塩化クロミルによる酸化
三酸化クロムと塩酸/硫酸より調製される塩化クロミルを使った芳香族メチル基を酸化する方法はエタール反応とも呼ばれる方法です。1877年にEtardにより発見された反応です。
Étard, A. Compt. Rend. 1880, 90, 534.
二クロム酸や過マンガン酸などではカルボン酸まで酸化しますが塩化クロミルではアルデヒドを比較的良い収率で得られます。
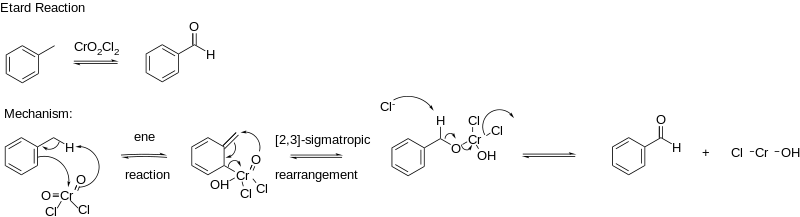
反応機構 from wikipedia Ryconrad [CC0]
塩化クロミルは自前で調製できる他、市販されています(ardrich, wako)。塩化クロミルは一気に加えると爆発することがあるので少量ずつ注意深く反応を行います。
アルケンやケトン、アゾ基などは変換されるので注意します。
反応はメチル基のオルト位に置換基があると収率が低下することが多いです。置換基のかさ高さが影響します。
反応例1
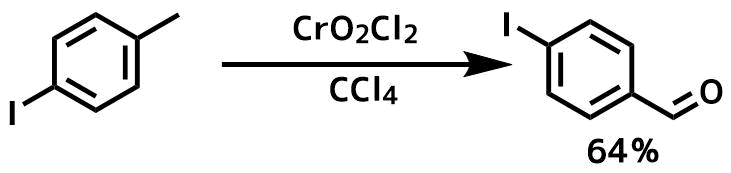
Wheeler, Owen H. Canadian Journal of Chemistry, 36, 667-71; 1958
基質(0.2 mol)を四塩化炭素(150mL)に溶解し、0℃に冷却しながら、四塩化炭素(150 mL)に溶かした塩化クロミル(2eq)を1hかけて複数回に分けて加える。(反応に伴い赤褐色から黒色に変化する)その後室温に戻しながら21時間撹拌した。結晶を濾過し、得られた結晶を少量ずつ少量の水に溶解した溶液を過剰量の飽和亜硫酸ナトリウム水溶液に冷却しながらゆっくりと加えた後、6N塩酸(100mL)を加えて塩基性のクロム塩を溶かして、生じたアルデヒドをエーテル等で抽出します。得られた粗生成物は再結晶や蒸留で精製します。
反応は進行しにくい場合は還流しても良いです。還流すると短い時間で反応が終わります(ものによって室温7daysの場合もある)。
1)Wheeler, Owen H. “ÉTARD REACTION: I. ITS SCOPE AND LIMITATION WITH SUBSTITUTED TOLUENES.” Canadian Journal of Chemistry 36.4 (1958): 667-671.2)塩化クロミルの他の反応について Limberg, Christian. “On the trail of CrO2Cl2 in its reactions with organic compounds.” Chemistry–A European Journal 6.12 (2000): 2083-2089.
DDQによるメチルの酸化
DDQは炭化水素の芳香族化などに使われる試薬ですが、ベンジル位の酸化も可能です。特に電子豊富な芳香環のメチル基は酸化されやすいです。
この性質を利用したのが「p-メトキシベンジル基(PMB基)」のDDQを用いた脱保護です。4位に電子供与機のメトキシ基が結合したベンジル基はベンジル位が活性化されており、酸化されやすくなっているためベンジル基と区別して脱保護可能です。
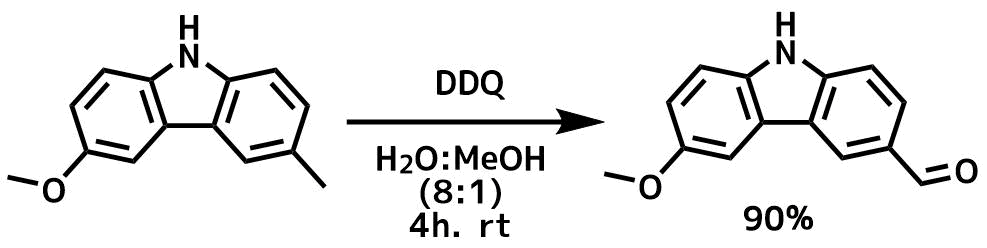
Naykode, Mahavir S. et al ournal of Organic Chemistry, 80(4), 2392-2396; 2015
基質(100 mg、0.473 mmol)をMeOH / H2O(16:2)、DDQ(537 mg、2.36 mmol)溶液に加えて室温で4時間反応後、濃縮し、カラムクロマトグラフィーにより精製して目的物を90%の収率で得た。
コバルト触媒を使ったメチル基の酸化
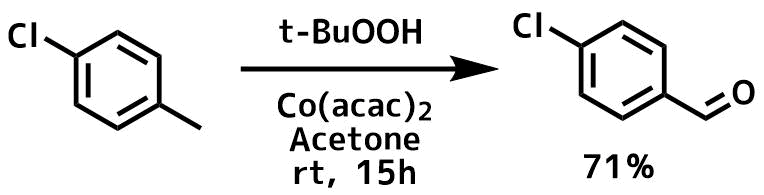
Han, Xiaoqiang et al Synthesis, 45(5), 615-620; 2013
アセトン(20 mL)に溶かした基質(10 mmol)およびCo(acac)2(257mg、1 mmol)の溶液に、TBHP(5.14 g、4.0 mmol、4当量、70%)を滴下し、 混合物を室温で15時間撹拌した。反応混合物にブライン水溶液を加え、溶液をエーテル抽出して、得られたクルードをカラム精製して目的物を71%の収率で得た。
コバルト触媒を使った酸化は工業ではよく利用されます。
ペルオキソ二硫酸カリウムを使った酸化
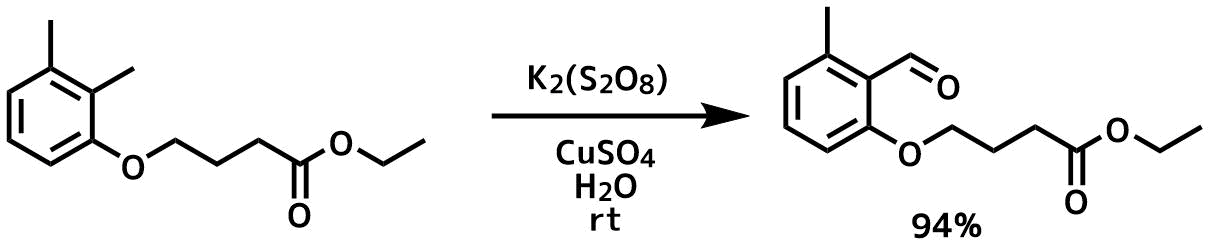
Goodnow, Robert A., Jr. et al Journal of Medicinal Chemistry, 53(9), 3502-3516; 2010
水(396 mL)硫酸銅(II)五水和物(21.98 g、88.06 mmol)とペルオキソ二硫酸カリウム(71.42 g、264 mmol)の混合物を63-65°Cに加熱して、青色溶液を得た。次に基質(20.81 g、88.06 mmol)のアセトニトリル(220 mL)溶液を同温度で加えて、薄緑色の溶液を40分間還流した。次に、反応混合物を5℃以下に冷却して、固体を沈殿させて得られた固体を濾過、ジクロロメタン(1.0 L)で洗浄した。有機層を集めて、水層をジクロロメタンで抽出、ブラインで洗浄し、MgSO4で乾燥、クルードをカラム精製して目的物を94%で得た。
また、ピリジン中で酸化を行うことにより銅塩などの重金属を加えなくても酸化できる方法がY.Huらにより報告されました。
Y. Hu, L. Zhou, W. Lu, Synthesis, 2017, 49, 4007-4016.
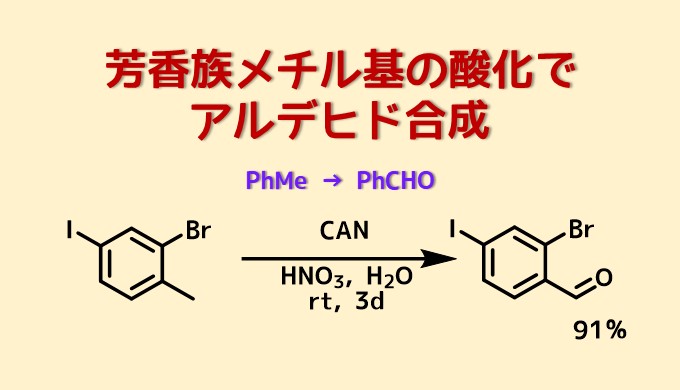
CANを使った酸化
電子不足な芳香環に対しては反応時間が長くなります。
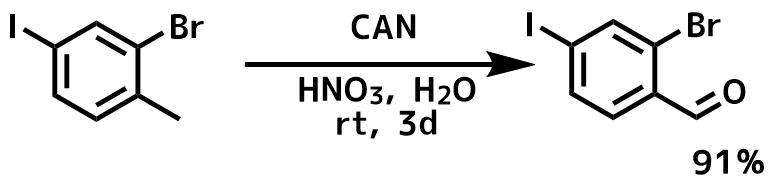
Shultz, David A. and Hollomon, Martha G. Chemistry of Materials, 12(2), 580-585; 2000
8M HNO3(97 mL),基質(5.75 g、19.4 mmol)の溶液を90℃に加熱し硝酸第二セリウムアンモニウム(42.5 g、77.5 mmol)を反応混合物が淡黄色を保つ速度で2日間にわたって少しずつ加えた。 硝酸第二セリウムアンモニウムの添加後、溶液を加熱し、90℃でさらに3日間撹拌した。 (反応が完了すると、溶液は黄色から無色になる)。混合物をCH2Cl2で抽出し、有機抽出物を水(3×50mL)、飽和NaHCO3水溶液(3×50mL)、およびブライン(3×50mL)で洗浄した。 得られたクルードをカラム精製により目的物を91%の収率で得た。
二酸化セレンによる酸化 (ライリー酸化)
二酸化セレンはアリル位やベンジル位、カルボニルのα位を酸化します。アルコールやアルデヒド、カルボン酸を与えます。
二酸化セレンによる酸化はカルボン酸まで進行することがあります。基本的な方法としては、二酸化セレンを加えてジオキサンやアルコール、ベンゼンなどの溶媒中で還流して反応させます。
溶媒はジオキサンを用いることが多いです。
二酸化セレンは試薬の状態によって酸化がスムーズに進行しないことがあり、用事調製したほうが収率が良いです。
t-BuOOHを再酸化剤として加えることも多いです。
二酸化セレンの調整法
金属セレン(wako 25g, 3200円)を1.5倍量(wt.)の濃硝酸中に少量ずつ加えたのち、硝酸を蒸発乾固して得られた固体を乳鉢で砕いて粉末として、少量の濃硝酸で湿らせたものを加熱して昇華により精製する。昇華用の器具がない場合は蒸発皿に漏斗を逆さにして蓋をしてバーナーで加熱すると漏斗の内壁に針状結晶がでてくる。
反応例1
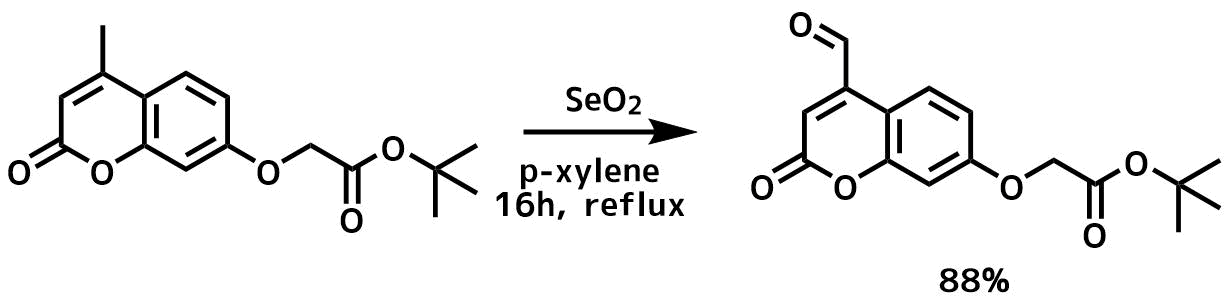
Velema, Willem A. et al ACS Chemical Biology, 9(9), 1969-1974; 2014
SeO2(3.45 mmol、379 mg)を基質(1.72 mmol、500 mg)のp-キシレン(10 mL)溶液に加えて、16時間加熱還流し、反応後温かいまま熱時濾過し、濾液を濃縮して目的物を88%で得た。
二酸化マンガンによる酸化
二酸化マンガンは硫酸や酢酸などとともに用いることによってメチル基を酸化できます。
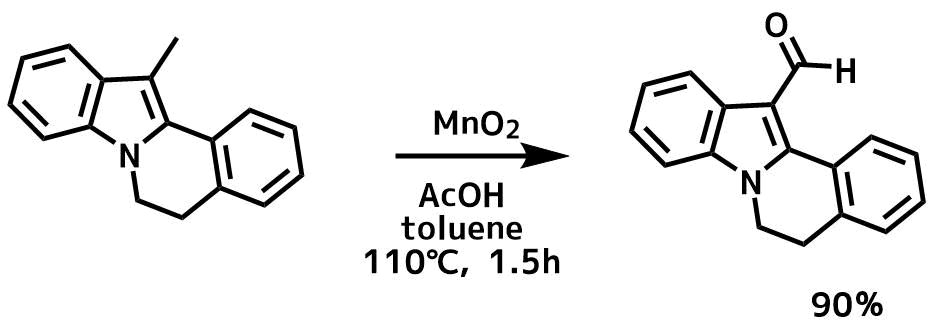
Martin-Garcia, Iris and Alonso, Francisco Chemistry – A European Journal, 24(71), 18857-18862; 2018
IBXによる酸化
酸化反応に使われるIBXは条件によっては芳香族メチル基を酸化することが可能です。金属を使用しない方法として有用です。
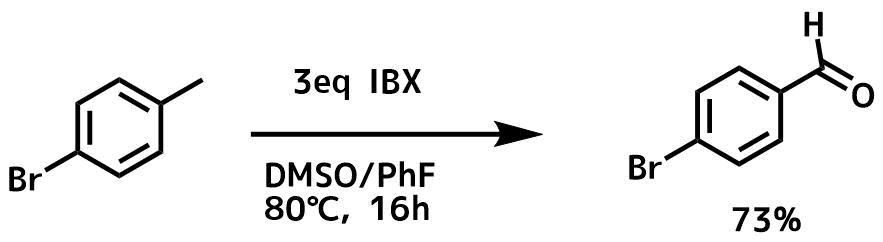
Nicolaou, K. C., et al.JACS, 124.10 (2002): 2212-2220.
ハロゲン化してアルデヒドに変換
ハロゲン化の後、アルデヒドに変換する方法です。
メチルのハロゲン化はNCSやNBS用いたラジカル的臭素化が便利です。
ハロゲン化物は塩化物で十分です。
ソムレー反応 – sommelet反応 (ヘキサメチレンテトラミン)

ソムレー反応の概要 from wikipedia public domain image
sommelet反応はベンジルハライドにヘキサメチレンテトラミンを作用させてヘキサミニウム塩を作ったのちこれを分解してアルデヒドを得ます。
Angyal, S. J., and R. C. Rassack. “The Sommelet Reaction.” Nature 161.4097 (1948): 723.
ソムレー反応は芳香族アルデヒドの合成法として有用ですが、重合しやすい脂肪族・アリルアルデヒドを得る方法としてはあまり適していません。
ニトロ基などの電子求引基があると収率は低下します。
参考 Sommelet reaction - Wikipediaソムレー反応
ソムレー反応の反応機構
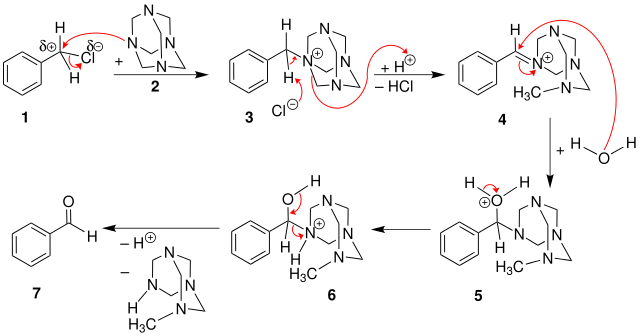
ソムレー反応の反応機構 from wikipedia public domain image
ソムレー反応ではアルデヒドとヘキサメチレンテトラミンが反応して3のヘキサミニウム塩が生じます。
ヘキサミンが嵩高いために、メチル基のオルト位に置換基がある場合は収率が大きく低下します。
ヘキサミニウム塩を分離してから合成する方法
ヘキサミニウム塩は溶解性が悪いことが多いので、クロロホルムなどで固体とすれば精製ができる。特にベンジルハライドの反応性が高くて精製が難しい時、連続的に反応をする場合などはヘキサミニウム塩で一旦精製してから加水分解するのがおすすめです。
クロロホルム中に小過剰の1.1eqのヘキサミンを加えて還流すると反応によりクロロホルムに溶解しない固体が生成してきます(脂肪族の場合は結晶にならないことも多い)。溶解する場合はエーテルやヘキサン、アセトンなどを加えて沈殿させます。
ヘキサミニウム塩は酢酸や濃塩酸で加熱して分解する。脂溶性が高ければ水を加えればアルデヒドが析出してくる。出てこなければ抽出する。ソムレー反応以外に類似した方法としてはKrohnke法、Hass-Bender法がある。
まとめ
後処理の容易さや操作の簡単さなどを考えるとおすすめな方法は二酸化セレンを使ったセレン酸化やDDQ、ペルオキソ二硫酸カリウム、CANなどがおすすめです。
クロム酸を使った方法は単純な化合物を酸化するのに有用ですが、実験室レベルでは入手可能な原料も多く、毒性などを考慮すると合成手法としては微妙かもしれません。
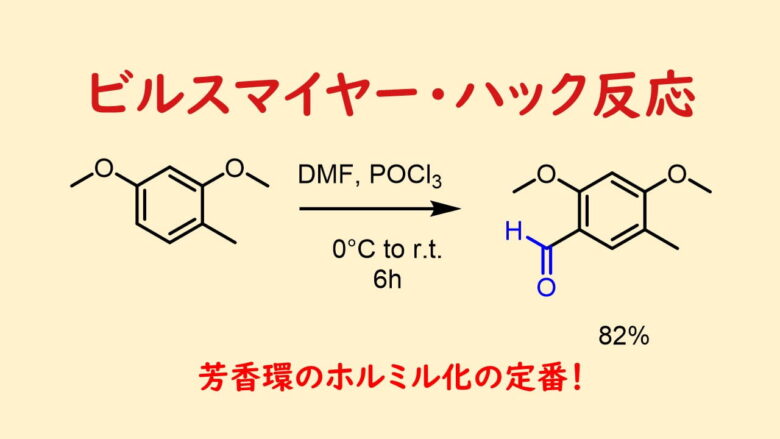
芳香族アルデヒドを得る方法としては別記事で紹介するアルコールを酸化する方法や直接ホルミル基を導入するビルスマイヤーハック反応などが有用です。